Espectroscòpia d'absorció

L'espectroscòpia d'absorció fa referència a les tècniques d'espectroscòpia que mesuren l'absorció de radiació electromagnètica, com a funció de freqüència o longitud d’ona, deguda a la interacció amb una mostra. La mostra absorbeix energia, és a dir, fotons, del camp de radiació. La intensitat de l'absorció varia en funció de la freqüència i aquesta variació és l'espectre d'absorció. L'espectroscòpia d'absorció es fa a través de l'espectre electromagnètic.
Es fa servir l'espectroscòpia d'absorció com una eina en l'anàlisi química. L'espectroscòpia infraroja i l'espectroscòpia ultraviolada són particularment comunes en l'anàlisi. També s'utilitza lespectroscòpia d'absorció en els estudis de física atòmica i molecular, astronomia i sensors remots
Astronomia[modifica]

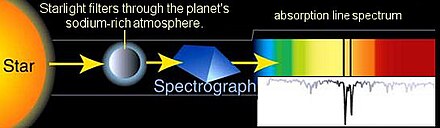
L'espectroscòpia stronòmica és un tipus especial de sensor remot. En aquest cas els objectes són tan lluny de la terra que la radiació electromagnètica és l'única manera possible de mesurar-los. Es fa servir, entre d'altres, per estudiar els planetes extrasolars.
Espectre d'absorció[modifica]

L'espectre d'absorció d'un material és la fracció de la radiació incident absorbida pel material al llarg d'un rang de freqüències. L'espectre d'absorció és determinat principalment[1][2][3] per la seva composició atòmica i molecular
Teoria bàsica[modifica]
Les línies d'absorció es classifiquen normalment per la naturalesa del canvi de mecànica quàntica induïda en la molècula o un àtom. Les línies rotacionals, per exemple, es produeixen quan l'estat de rotació d'una molècula es canvia. Les línies de rotació es troben típicament en la regió de microones de l'espectre. Les línies vibracionals corresponen als canvis en l'estat vibratori de la molècula i es troben típicament en la regió infraroja. Les ínies electròniques corresponen a un canvi en l'estat electrònic d'un àtom o molècula i es troben típicament en la regió visible i ultraviolada. L'absorció de raigs X s'associa amb l'excitació de l'estructura interna dels electrons en els àtoms. Aquests canvis també poden ser combinats (per exemple, l'acoblament rotovibracional, dona lloc a noves línies d'absorció en l'energia combinada dels dos canvis. L'energia associada amb el canvi en mecànica quàntica principalment determina la freqüència de la línia d'absorció, però la freqüència pot ser desplaçada per diversos tipus d'interaccions. Els camps elèctrics i magnètics poden causar un canvi. Les interaccions amb molècules veïnes poden provocar canvis. Per exemple, les línies d'absorció de la molècula en fase gasosa pot canviar significativament quan aquesta molècula està en una fase líquida o sòlida i interaccionar més fortament amb les molècules veïnes. Les línies d'absorció s'han representat com a línies infinitesimalment primes, és a dir, funció delta de Dirac, però les línies observades sempre tenen una forma que es determina per l'instrument utilitzat per a l'observació, el material absorbent de la radiació i la física entorn d'aquest material. És comú per a les línies tenir la forma d'una distribució gaussiana o distribució de Lorentz. També és comú per a una línia que es caracteritza només per la seva intensitat i ample en lloc de tota la forma que es caracteritza. La intensitat obtinguda integrant l'àrea sota la línia d'absorció-és proporcional a la quantitat d'aquesta substància absorbent. La intensitat es relaciona també amb la temperatura de la substància i la interacció mecànica quàntica entre la radiació i l'absorbidor. Aquesta interacció es quantifica pel moment de transició i depèn de l'estat en particular inferior de la transició s'inicia des de l'estat superior i que està connectat. L'amplada de les línies d'absorció pot ser determinat per l'espectròmetre utilitzat per registrar. Un espectròmetre té un límit inherent a l'estretor d'una línia que pot decidir i per tant l'amplada pot ser observada en aquest límit. Si l'amplada és més gran que el límit de resolució, llavors es determina principalment per l'entorn de l'absorbent. Un absorbidor de líquid o sòlid, en el qual les molècules veïnes fortament interaccionen entre si, tendeix a tenir més àmplies línies d'absorció que un gas. L'augment de la temperatura o la pressió del material absorbent també tendirà a augmentar l'amplada de línia. També és comú per diverses transicions veïnes per estar prou a prop entre si que les seves línies se superposen i la línia general resultant és per tant, més ampli encara
Referències[modifica]
- ↑ Modern Spectroscopy (Paperback) by J. Michael Hollas ISBN 978-0-470-84416-8
- ↑ Symmetry and Spectroscopy: An Introduction to Vibrational and Electronic Spectroscopy (Paperback) by Daniel C. Harris, Michael D. Bertolucci ISBN 978-0-486-66144-5
- ↑ Spectra of Atoms and Molecules by Peter F. Bernath ISBN 978-0-19-517759-6
