Glioblastoma multiforme
 Coronal MRI with contrast of a glioblastoma WHO grade IV in a 15-year-old male. | |
| Tipus | astrocitoma i malaltia |
|---|---|
| Especialitat | Neurooncology (en) |
| Clínica-tractament | |
Medicació | |
| Patogènia | |
| Associació genètica | SSBP2 (en) |
| Classificació | |
| CIM-11 | XH7F82 |
| CIM-10 | C71 |
| CIM-9 | 191 |
| CIM-O | M9440/3 |
| Recursos externs | |
| Enciclopèdia Catalana | 0186281 |
| OMIM | 137800 |
| DiseasesDB | 29448 |
| eMedicine | 1156220 i 283252 |
| MeSH | D005909 |
| UMLS CUI | C0017636, C0278878 i C1514422 |
| DOID | DOID:3068 |
El glioblastoma multiforme (GBM) és el tumor cerebral maligne primari més comú i agressiu en humans, afecta les cèl·lules glials, el 52% de tots els casos de tumors cerebrals amb afectació de teixit funcional i el 20% de tots els tumors intracranials. Tot i ser la forma més prevalent del tumor primari cerebral, el GBM es dona només en 2-3 casos per cada 100000 persones a Europa i Amèrica del Nord. D'acord amb la Classificació de tumors del sistema nerviós central de l'OMS, el nom estàndard per aquest tipus de tumor és "glioblastoma"; i presenta dues variants: el glioblastoma de cèl·lules gegants i el gliosarcoma.
El tractament pot incloure quimioteràpia, radioteràpia, cirurgia, radiocirurgia, glucocorticoides, teràpia antiangiogènica[1] i mètodes experimentals com la transferència de gens.
Amb l'excepció dels gliomes del tronc cerebral, el glioblastoma és el que té el pitjor pronòstic entre els càncers del sistema nerviós central, malgrat el tractament multimodal que consisteix en una craniotomia oberta amb resecció quirúrgica de la major quantitat de tumor possible, seguida per la quimioteràpia concurrent o seqüencial, teràpia antiangiogènica amb bevacizumab, radiocirurgia i el tractament simptomàtic amb glucocorticoides. El pronòstic és dolent, amb una mitjana de supervivència d'aproximadament 14 mesos.[2]
Signes i símptomes[modifica]
Encara que els símptomes comuns de la malaltia inclouen convulsions, nàusees i vòmits, mal de cap i hemiparèsia, el símptoma més freqüent és el dèficit progressiu de la memòria, personalitat o neurològic a causa de la implicació del lòbul temporal o del frontal. El tipus de símptomes produïts depenen en gran manera de la localització del tumor. El tumor pot començar a produir els símptomes ràpidament, però a vegades és una malaltia asimptomàtica fins que arriba a una mida molt gran.
Causes[modifica]
El GBM és més comú en els homes, tot i que es desconeix el motiu.[3] La majoria dels tumors de glioblastoma semblen ser esporàdics, sense cap predisposició genètica. No s'han trobat vincles entre el glioblastoma i el tabaquisme,[4] carns curades,[5] o camps electromagnètics.[6][7][8][9] El consum d'alcohol pot ser un possible factor de risc[10] Recentment s'ha descobert l'evidència d'una possible causa viral, el SV40[11] o el citomegalovirus.[12] També sembla que existeix una petita relació entre la radiació ionitzant i el glioblastoma.[13] Hi ha una associació entre el tumor cerebral i la malària, això fa pensar que el mosquit Anopheles, (portador de la malària), pot transmetre un virus o un altre agent que podrien causar el glioblastoma.
Altres factors de risc inclouen:[14]
- Sexe: masculí (lleugerament més comú en homes que en dones)
- Edat: majors de 50 anys.
- Raça: caucàsics, asiàtics.
- Tenir un astrocitoma de baix grau (tumor cerebral), que sovint es converteix en un tumor de grau elevat passat un cert temps.
- Tenir un dels següents trastorns genètics s'associa amb una major incidència de gliomes: neurofibromatosi, esclerosi tuberosa, malaltia de Von Hippel-Lindau, síndrome de Li-Fraumeni o síndrome de Turcot.
Patogènesi[modifica]
Els GBMs es caracteritzen per la presència d'àrees petites de necrosi que està envoltat de cèl·lules anaplàstiques. Aquesta característica, així com la presència de vasos sanguinis hiperplàsics, el diferencia de l'astrocitoma de tercer grau, que no té aquestes característiques.
Hi ha quatre subtipus de glioblastoma.[15] El 97% dels tumors del subtipus "clàssic" tenen còpies addicionals del gen del receptor del factor de creixement epidèrmic (EGFR) i la majoria tenen l'expressió d'aquest receptor més elevada del normal, mentre que el gen TP53, que sovint es troba mutat en el glioblastoma, poques vegades s'hi troba en aquests subtipus.[16] El subtipus proneural sovint presenta alts índex d'alteracions en TP53, i en PDGFRA, el gen que codifica un tipus de receptor de creixement derivat de les plaquetes, i en el IDHI, el gen que codifica l'isocritat deshidrogonenasa -1. El subtipus mesenquimàtic es caracteritza per un índex elevat de mutacions en el NF1, el gen que codifica la neurofibromatosi tipus 1 i poques alteracions en el gen EGFR i menor expressió en el GFR que altres tipus.[17]
Els GBMs generalment es formen en la substància blanca, creixen ràpidament i poden arribar a ser molt grans abans d'originar símptomes. Menys del 10% procedeixen d'una degeneració més lenta d'un astrocitoma de baix grau o d'un astrocitoma anaplàstic. Aquests s'anomenen GBMs secundaris i són més comuns en els pacients més joves (edat mitjana 45 anys versus 62).[18] El tumor es pot estendre per les meninges o per la paret ventricular, la qual cosa comporta un augment de proteïnes en el líquid cefalorraquidi (LCR) (> 100 mg/dL), així com una pleocitosis ocasional de 10 a 100 cèl·lules, majoritàriament limfòcits. Les cèl·lules malignes contingudes al LCR rarament es poden estendre per la medul·la espinal o causar una gliomatosis meningea. No obstant això, les metàstasis d'un GBM més enllà del sistema nerviós central és molt rar. Un 50% dels GBMs ocupen més d'un lòbul d'un hemisferi o són bilaterals. Els tumors d'aquest tipus sorgeixen generalment del telencèfal i rarament presenten una clàssica infiltració a través del cos callós, produint un glioma en papallona (bilateral).
El tumor pot presentar diversos aspectes, depenent de la quantitat d'hemorràgia, necrosi o el temps d'evolució. Una tomografia computada mostra generalment una massa no homogènia amb un centre hipodens i un anell d'augment variable envoltat d'edema. L'efecte de la massa del tumor i l'edema poden comprimir els ventricles i causar hidrocefàlia.
Als glioblastomes, s'hi han trobat cèl·lules canceroses amb propietats similars a les cèl·lules mare (aquesta pot ser una causa de la seva resistència als tractaments convencionals i la seva elevada taxa de reaparició).[19]
Diagnòstic[modifica]
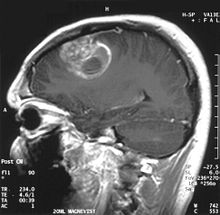
Vistos amb una imatge de ressonància magnètica (RM), els glioblastomes sovint apareixen com lesions en forma d'anell. L'aparença no és específica, i és similar a altres lesions com un abscés, una metàstasi, o una esclerosi múltiple tumefactiva.[20] El diagnòstic definitiu d'un suposat GBM trobat mitjançant una RM o una altra prova requereix una biòpsia estereotàctica o una craniotomia amb una resecció del tumor i una confirmació patològica. Com que la mostra de la biòpsia s'extreu de sobre la part més maligna, la biòpsia o resecció tumoral subtotal poden resultar perjudicials per a la lesió. Les imatges del flux sanguini del tumor mitjançant perfusió de ressonància magnètica i la mesura de la concentració de metabòlits del tumor amb espectroscòpia de RM poden aportar un valor afegit a l'eficàcia de la ressonància magnètica en el diagnòstic de glioblastoma, tot i que la confirmació patològica mitjançant biòpsia segueix sent l'estàndard d'or.
Classificació[modifica]
La classificació OMS de 2016 dels tumors del sistema nerviós central[21] suposa un canvi de paradigma front anteriors classificacions, perquè definix els tumors a més de per la seua morfologia, pel seu perfil molecular. En concret, el glioblastoma es classifica segons l'estat de mutació del gen isocitrat deshidrogenasa (IDH): al·lel-salvatge i mutant.
| IDH al·lel-salvatge | IDH mutant | |
|---|---|---|
| Sinònim | Glioblastoma primari | Glioblastoma secundari |
| Lesió precursora | Identificat de novo | Astrocitoma difús
Astrocitoma anaplàstic |
| Proporció de glioblsatoma | ~90% | ~10% |
| Edat mitjana de diagnòstic | ~62 anys | ~44 anys |
| Ràtio home:dona | 1.42:1 | 1.05:1 |
| Durada mitjana d'història clínica | 4 mesos | 15 mesos |
| Supervivència mitjana | ||
| Cirurgia + radioteràpia | 9.9 mesos | 24 mesos |
| Cirurgia + radioteràpia + quimioteràpia | 15 mesos | 31 mesos |
Tractament[modifica]
Tractar el glioblastoma és un procés complicat a causa de diversos factors:[23]
- Les cèl·lules tumorals són molt resistents a les teràpies convencionals.
- El cervell és susceptible a danys causats per les teràpies convencionals.
- El cervell té una capacitat molt limitada per reparar-se a si mateix.
- Molts medicaments no poden travessar la barrera hematoencefàlica per actuar sobre el tumor.
El tractament dels tumors cerebrals primaris i les metàstasis cerebrals es compon de dos tractaments diferents: simptomàtics i pal·liatius.
El tractament simptomàtic[modifica]
El tractament de suport contra el tumor se centra a alleujar els símptomes i millorar la funció neurològica del pacient. Els agents de suport principals són els anticonvulsius i els glucocorticoides.
- Històricament, al voltant del 90% dels pacients amb glioblastoma se sotmetien a tractament amb anticonvulsius, encara que s'ha estimat que només un 40% dels pacients requeria aquest tractament. Recentment, s'ha recomanat als neurocirurgians que no administrin anticonvulsius de forma profilàctica, cal esperar que es produeixi un atac abans de prescriure'ls.[24] Aquells que reben fenitoïna alhora que són sotmesos a radioteràpia poden presentar reaccions cutànies greus com ara eritema multiforme o la síndrome de Stevens-Johnson.
- Els glucocorticoides (generalment dexametasona) administrats de 4 a 10 mg cada 4 o 6 hores, poden reduir l'edema peritumoral (a través de la reorganització de la barrera hematoencefàlica), disminuint l'efecte de la massa tumoral i reduint la pressió intracranial, amb una disminució del mal de cap o la somnolència.
La teràpia pal·liativa[modifica]
El tractament pal·liatiu en general té l'objectiu de millorar la qualitat de vida i aconseguir un temps de supervivència més llarg per al pacient. Aquest tractament inclou cirurgia, radioteràpia i quimioteràpia. La màxima resecció possible del tumor generalment es combina amb la quimioteràpia i la radioteràpia. La resecció gairebé total del tumor s'associa amb un millor pronòstic.
Cirurgia[modifica]
La cirurgia és la primera etapa de tractament del glioblastoma. Un GBM conté, de mitjana, 1011 cèl·lules, que es redueix a una mitjana de 10⁹ cèl·lules després de la cirurgia (una reducció del 99%). Normalment s'extreu una secció del tumor per al diagnòstic patològic, per tal d'eliminar els símptomes causats per la pressió de la massa tumoral contra el cervell, per eliminar part de la malaltia abans d'iniciar la teràpia secundària mitjançant radioteràpia i quimioteràpia i per prolongar la supervivència del pacient.
Sempre serà millor quan més gran sigui el grau d'extirpació del tumor. L'eliminació del tumor del 98%, o més, s'ha associat amb una esperança de supervivència significativament major i una millor qualitat de vida, enfront de la reducció de menys del 98% del tumor, que presenta un pitjor diagnòstic.[25] Les possibilitats que l'extirpació del tumor inicial sigui gairebé total pot ser molt més gran si la cirurgia està guiada per un tint fluorescent conegut com a àcid 5-aminolevulínic.[26] Les cèl·lules del glioblastoma s'infiltren àmpliament a través del cervell en el moment del diagnòstic invasiu, de manera que malgrat es practiqui una "resecció total" del tumor, la majoria dels pacients de GBM acaben desenvolupant amb el temps tumors recurrents tant prop de la zona del tumor original com en altres zones més distants, produint "lesions satèl·lit" dins del cervell. Altres tractaments, incloent-hi la radioteràpia, són utilitzats després de la cirurgia, en un esforç per tal d'endarrerir l'aparició de tumors recurrents.
Radioteràpia[modifica]
Després de la cirurgia, la radioteràpia és el tractament principal per a les persones amb glioblastoma. Un assaig clínic aleatori dut a terme en la dècada de 1970, va assignar a l'atzar 303 pacients amb GBM entre dos tipus de tractament diferents: la teràpia amb radiació i la sense radiació. Amb aquest estudi es va demostrar que els pacients que havien rebut radioteràpia van tenir una supervivència mitjana més del doble dels que no n'havien rebut.[27] Com a conseqüència de la investigació clínica posterior, s'ha arribat a la conclusió que el millor tractament per pacients amb GBM és la cirurgia seguida de radioteràpia. De mitjana, la radioteràpia, després de la cirurgia, pot reduir la mida del tumor en 107 cèl·lules. La radioteràpia total del cervell enfront aquella més precisa i selectiva (radioteràpia tridimensional conformal) no millora els resultats.[28] D'aquesta manera, una dosi total de radiació de 60-65 Gy és òptima per al tractament.[29]
La teràpia de captura del neutró de bor (Boron Neutron Capture Therapy) és una teràpia alternativa a l'anterior que ha estat provada per al tractament de persones amb GBM, però no és d'ús comú.
Quimioteràpia[modifica]
Com a conseqüència de la investigació clínica posterior, s'ha arribat a la conclusió que el millor tractament per pacients amb GBM és la cirurgia seguida de radioteràpia. En altres tipus de càncer, on la radioteràpia pot prolongar la supervivència o, fins i tot, curar els tumors, l'addició de quimioteràpia millora la supervivència del pacient en comparació al tractament, només, amb radioteràpia. Alguns exemples d'aquests càncers, són el càncer cervical i el càncer de gola, entre d'altres.
A causa d'això, en diversos assajos clínics, que es van dur a terme, s'esperava que la supervivència dels pacients amb GBM augmentés amb l'addició de quimioteràpia a la radioteràpia. Contràriament, es va observar que en la majoria d'aquests estudis no hi havia un benefici clar pels pacients en l'addició de la quimioteràpia a la radioteràpia. No obstant això, en un gran assaig clínic amb 575 pacients, assignats a l'atzar en dos grups (on els del primer van rebre un tractament amb radiació estàndard, i els del segon, a més de la radioteràpia, també va rebre quimioteràpia amb temozolomida), es va demostrar que el grup que va rebre la temozolomida va sobreviure una mitjana de 14,6 mesos, enfront dels 12,1 mesos pel grup que va rebre només radioteràpia.[30] Aquest tipus de tractament és ara l'estàndard per a la majoria dels casos de glioblastoma multiforme.[31][32] Temozolomide seems to work by sensitizing the tumor cells to radiation.[33]
Altes dosis de temozolomida en gliomes d'alt grau tenen baixa toxicitat, però els resultats són comparables a les dosis estàndard.[34]
The U.S. Food and Drug Administration va aprovar el bevacizumab per a tractar pacients amb glioblastoma en progressió després de la teràpia estàndard, sobre la base dels resultats de dos estudis que van demostrar que el bevacizumab redueix la mida del tumor en alguns pacients amb glioblastoma multiforme. En el primer estudi, en el 28% dels pacients amb glioblastoma es va observar una reducció del tumor, el 38% va sobreviure almenys un any, i el 43% va sobreviure com a mínim 6 mesos sense progressió de la malaltia.[35] A diferència del cas del càncer de còlon, en el càncer de pulmó i en altres càncers on el bevacizumab actua potenciant la quimioteràpia, els estudis ens mostren que en els pacients amb GBM, l'addició de quimioteràpia a bevacizumab no millora els resultats obtinguts en el cas de tractar només amb bevacizumab. El bevacizumab actua reduint l'edema cerebral i els símptomes conseqüents, i pot ser que el benefici d'aquesta droga sigui degut a la seva acció contra l'edema, en lloc de qualsevol acció contra el tumor en si. Alguns pacients amb edema cerebral en realitat no tenen cap tumor actiu restant, sinó que més aviat desenvolupen l'edema com a efecte tardà del tractament anterior amb radiació. Aquest tipus d'edema és difícil de distingir dels que s'originen a causa d'un tumor, i ambdós poden coexistir. Tots dos responen al bevacizumab.
Transferència de gens[modifica]
La transferència de gens és un enfocament prometedor per a la lluita contra el càncer, incloent el càncer de cervell.[36] A diferència dels tractaments convencionals actuals contra el càncer com la quimioteràpia i la radioteràpia, la transferència genètica té la capacitat de destruir selectivament les cèl·lules canceroses deixant indemnes les cèl·lules sanes. Durant les últimes dues dècades s'han aconseguit importants avenços en la tecnologia de la transferència genètica i aquest camp ha madurat fins al punt de disposar de viabilitat clínica i comercial. Els avenços inclouen un vector (vehicle de lliurament de gens) de construcció, l'eficiència del vector productor de cèl·lules i els processos d'expansió, també inclouen models preclínics de malalties que són objecte i orientació reglamentàries en matèria de disseny d'assaigs clínics. En un d'aquests enfocaments, els investigadors d'UCLA en el 2005, van reportar un benefici de supervivència a llarg termini en un model experimental de tumor cerebral en animals.[37] Posteriorment, en la preparació d'assaigs clínics en humans, aquesta tecnologia va ser desenvolupada per Tocagen Inc.,[38] i està actualment sota investigació clínica en fase I/II, per tal de dur a terme el tractament potencial de glioma recurrent d'alt grau, com el glioblastoma multiforme (GBM) i l'astrocitoma anaplàstic.[39]
Proteïnes terapèutiques[modifica]
Fins fa poc temps, les proteïnes terapèutiques rarament eren utilitzades en un subconjunt dels tractaments mèdics. Actualment, les proteïnes terapèutiques han augmentat exponencialment en nombre i en freqüència d'ús des de la introducció de la primera proteïna terapèutica recombinant (la insulina humana) en la dècada de 1980. D'aquesta manera, aquestes proteïnes ja tenen un paper important en gairebé tots els camps de la medicina, incloent en el càncer de cervell. Un estudi clínic aleatori, que es troba en fase II de desenvolupament clínic, amb el APG101 (proteïna terapèutica en el glioblastoma) es va iniciar a principis de 2010.[40] L'estudi compara l'eficàcia d'un tractament combinat amb radioteràpia i APG101 administrat per via intravenosa versus radioteràpia només, sense administració de APG101. APG101 és una proteïna resultant de la fusió de CD95 amb la regió Fc d'un anticòs utilitzada en el tractament de malalties malignes. APG101 representa una forma innovadora d'abordar el tractament del GBM, ja que té la funció d'inhibir el creixement invasiu de les cèl·lules del glioblastoma. Aquesta teràpia està basada en els resultats obtinguts en el Centre Alemany de Recerca del Càncer (DKFZ) en què en les cèl·lules del glioblastoma, la unió del lligand CD95 amb el seu receptor afí estimula el creixement invasiu de les cèl·lules tumorals. D'aquesta manera, la inhibició de la interacció amb APG101 disminueix la migració de les cèl·lules tumorals.[41] Fins ara, s'han realitzat assajos amb APG101 sobre 20 voluntaris sans i 32 pacients. La tolerància a aquest compost va ser bona i no es van observar efectes secundaris greus.[42]
Immunoteràpia[modifica]
La recaiguda en un glioblastoma està associada a la reaparició i la persistència de les cèl·lules mare tumorals.[43] En un assaig reduït, una vacuna consistent en hibridoma de cèl·lules B tumorals contra cèl·lules mare cancerígenes va causar una resposta immunitària específica contra el tumor i, en conseqüència, va intensificar la resposta del sistema immunitari cap a la malaltia.[44] Actualment s'estan realitzant assajos més extensos per avaluar millor aquesta forma de tractar la malaltia.
Camps elèctrics de corrent altern[modifica]

Un nou enfocament per al tractament de la malaltia és l'aplicació de camps elèctrics de corrent altern per interferir sobre la divisió de les cèl·lules canceroses. Al contrari de la cirurgia, la radioteràpia i la quimioteràpia, que s'utilitzen en el tractament de qualsevol tipus de càncer, l'aplicació del corrent altern només s'està investigant sobre el glioblastoma. Aquesta tècnica es basa en el fet que un camp elèctric amb una longitud d'ona determinada destrueix les cèl·lules que es troben en procés de divisió. Aquesta és una tècnica ideal per aplicar sobre els tumors cerebrals, ja que les cèl·lules cerebrals no es divideixen, però sí que ho fan les cèl·lules canceroses del cervell. Els pacients amb GBM tractats amb aquesta tècnica duen elèctrodes sobre el cuir cabellut units al sistema portàtil Novo-TTF. Recentment s'han publicat els resultats d'un assaig clínic extens en què els pacients amb una recaiguda del GBM van ser tractats amb el sistema Novo-TTF i mostren que aquest tractament és tan efectiu com la quimioteràpia pel que fa a la supervivència dels pacients.[45] Actualment s'està duent a terme un assaig clínic sobre nous diagnosticats de GBM que està estudiant si l'addició del sistema Novo-TTF sobre la radioteràpia estàndard i el tractament amb temozolomida millora la supervivència respecte a l'aplicació del tractament estàndard únicament.[46]
Teràpia metabòlica[modifica]
La dieta cetogènica s'ha utilitzat amb èxit en el tractament de glioblastomes en diversos estudis. Les cèl·lules canceroses, a causa de defectes en el metabolisme, són incapaces d'obtenir energia a partir dels greixos, de manera que depenen completament de glucosa i glutamina. Les neurones sanes poden utilitzar les cetones com a font d'energia molt eficient. Per tant, el fet de restringir els carbohidrats en la dieta perjudica considerablement les cèl·lules canceroses sense que les neurones sanes en resultin afectades. En la majoria dels estudis, les dietes cetogèniques o restringides en carbohidrats provoquen que la mida i el creixement del tumor es redueixin notablement.[47]
Recaiguda[modifica]
L'eliminació a llarg termini de la malaltia és possible, però el tumor normalment reapareix, sovint a uns 3 cm del lloc inicial, i un 10-20% dels casos poden desenvolupar noves lesions en regions més allunyades. L'aplicació de més cirurgia i tractament intens després de la recaiguda s'ha associat amb una certa millora.[48]
Pronòstic[modifica]
L'esperança de vida mitjana des del moment del diagnòstic sense cap mena de tractament és de 3 mesos, però amb tractament la supervivència sol ser d'entre 1 o 2 anys. L'augment de l'edat (per sobre dels 60 anys) comporta un pitjor pronòstic. La mort és provocada normalment per un edema cerebral o per l'increment de la pressió intracranial.[49] A Catalunya, té una taxa de supervivència a cinc anys per a homes al voltant del 9% i per a dones al voltant del 7%.[50]
Un bon resultat en el test de Karnofsky (KPS) i la metilació del gen MGMT s'associen amb una major supervivència.[49] Es pot realitzar un test d'ADN sobre els glioblastomes per determinar si el promotor del gen MGMT es troba metilat o no. Els pacients amb el promotor MGMT metilat solen presentar un major benefici a llarg termini que els que no el tenen metilat.[51] Aquesta característica de l'ADN és intrínseca per a cada pacient i actualment no es pot modificar externament.
Els beneficis a llarg termini també s'han associat amb els pacients que són tractats amb cirurgia, radioteràpia o quimioteràpia a base de temozolomida.[49] No obstant això, encara es desconeix per què alguns pacients amb glioblastoma sobreviuen més que d'altres. Una edat inferior als 50 anys, està relacionada amb una major supervivència en el glioblastoma multiforme, i també amb millors resultats en l'extirpació del tumor, la teràpia amb temozolomida i en els resultats del test de Karnofsky. Un estudi recent confirma que la menor edat està associada amb un pronòstic molt millor, amb una petita fracció de pacients menors de 40 anys que s'hagin curat i després de 10 anys, es creu que tindran un risc de defunció igual al de la població normal.[52]
L'UCLA Neuro-Oncology publica a temps real dades sobre la supervivència dels pacients amb aquest diagnòstic. Són l'única institució dels EUA que mostra com evolucionen els seus pacients. També mostren una llista d'agents utilitzats en quimioteràpia per tractar el GBM. Segons un estudi del 2003, el pronòstic del glioblastoma multiforme es pot dividir en tres subgrups segons el resultat del test de Karnofsky, l'edat del pacient i el tractament.
Referències[modifica]
- ↑ Gina Kolata and Lawrence K. Altman, M.D. «Kennedy Case Shows Progress and Obstacles in Cancer Fight». New York Times, 27-08-2009.
- ↑ Van Meir, E. G.; Hadjipanayis, C. G.; Norden, A. D.; Shu, H. K.; Wen, P. Y.; Olson, J. J. «Exciting New Advances in Neuro-Oncology: The Avenue to a Cure for Malignant Glioma». CA: A Cancer Journal for Clinicians, 60, 3, 2010, pàg. 166–93. DOI: 10.3322/caac.20069. PMC: 2888474. PMID: 20445000.
- ↑ Ohgaki, H; Kleihues, P «Population-based studies on incidence, survival rates, and genetic alterations in astrocytic and oligodendroglial gliomas». Journal of neuropathology and experimental neurology, 64, 6, 2005, pàg. 479–89. PMID: 15977639.
- ↑ Zheng, T; Cantor, KP; Zhang, Y; Chiu, BC; Lynch, CF «Risk of brain glioma not associated with cigarette smoking or use of other tobacco products in Iowa». Cancer epidemiology, biomarkers & prevention, 10, 4, 2001, pàg. 413–4. PMID: 11319186.
- ↑ Huncharek, Michael; Kupelnick, Bruce; Wheeler, Lamar «Dietary Cured Meat and the Risk of Adult Glioma: A Meta-Analysis of Nine Observational Studies». Journal of Environmental Pathology, Toxicology and Oncology, 22, 2, 2003, pàg. 129–37. DOI: 10.1615/JEnvPathToxOncol.v22.i2.60.
- ↑ Savitz, David A.; Checkoway, Harvey; Loomis, Dana P. «Magnetic Field Exposure and Neurodegenerative Disease Mortality among Electric Utility Workers». Epidemiology, 9, 4, 1998, pàg. 398–404. DOI: 10.1097/00001648-199807000-00009. PMID: 9647903.
- ↑ Inskip, Peter D.; Tarone, Robert E.; Hatch, Elizabeth E.; Wilcosky, Timothy C.; Shapiro, William R.; Selker, Robert G.; Fine, Howard A.; Black, Peter M.; Loeffler, Jay S. «Cellular-Telephone Use and Brain Tumors». New England Journal of Medicine, 344, 2, 2001, pàg. 79–86. DOI: 10.1056/NEJM200101113440201. PMID: 11150357.
- ↑ Kan P, Simonsen SE, Lyon JL, Kestle JR. «Cellular phone use and brain tumor: a meta-analysis». Journal of Neurooncology, 86, 1, 2008, pàg. 71–78. DOI: 10.1007/s11060-007-9432-1. PMID: 17619826.[Enllaç no actiu]
- ↑ Hardell L, Carlberg M, Hansson Mild K. «Epidemiological evidence for an association between use of wireless phones and tumor diseases». Pathophysiology, 16, 2–3, 2009, pàg. 113–22. DOI: 10.1016/j.pathophys.2009.01.003. PMID: 19268551.
- ↑ Baglietto, L; Giles, GG; English, DR; Karahalios, A; Hopper, JL; Severi, G «Alcohol consumption and risk of glioblastoma; evidence from the Melbourne Collaborative Cohort Study.». International Journal of Cancer, 128, 8, 2011, pàg. 1929–1934. DOI: 10.1002/ijc.25770. PMID: 21344375.
- ↑ Vilchez, R; Kozinetz, CA; Arrington, AS; Madden, CR; Butel, JS «Simian virus 40 in human cancers». The American Journal of Medicine, 114, 8, 2003, pàg. 675–84. DOI: 10.1016/S0002-9343(03)00087-1. PMID: 12798456.
- ↑ "Target acquired", The Economist, May 29th, 2008
- ↑ Cavenee, WK «High-grade gliomas with chromosome 1p loss». Journal of neurosurgery, 92, 6, 2000, pàg. 1080–1. PMID: 10839286.
- ↑ Glioblastoma multiforme at Mount Sinai
- ↑ «The cellular origin for malignant glioma and prospects for clinical advancements». Expert Review of Molecular Diagnostics, 12, 4, maig 2012, pàg. 383–94. DOI: 10.1586/erm.12.30. PMC: 3368274. PMID: 22616703.
- ↑ Hayden, Erika Check «Genomics boosts brain-cancer work». Nature, 463, 7279, 2010, pàg. 278. DOI: 10.1038/463278a. PMID: 20090720.
- ↑ Kuehn, B. M. «Genomics Illuminates a Deadly Brain Cancer». JAMA: the Journal of the American Medical Association, 303, 10, 2010, pàg. 925–7. DOI: 10.1001/jama.2010.236. PMID: 20215599.
- ↑ Ohgaki, Hiroko; Kleihues, Paul «Genetic alterations and signaling pathways in the evolution of gliomas». Cancer Science, 100, 12, 2009, pàg. 2235–41. DOI: 10.1111/j.1349-7006.2009.01308.x. PMID: 19737147.
- ↑ Murat, A.; Migliavacca, E.; Gorlia, T.; Lambiv, W. L.; Shay, T.; Hamou, M.-F.; De Tribolet, N.; Regli, L.; Wick, W. «Stem Cell-Related 'Self-Renewal' Signature and High Epidermal Growth Factor Receptor Expression Associated with Resistance to Concomitant Chemoradiotherapy in Glioblastoma». Journal of Clinical Oncology, 26, 18, 2008, pàg. 3015–24. DOI: 10.1200/JCO.2007.15.7164. PMID: 18565887.
- ↑ Smirniotopoulos, J. G.; Murphy, F. M.; Rushing, E. J.; Rees, J. H.; Schroeder, J. W. «From the Archives of the AFIP: Patterns of Contrast Enhancement in the Brain and Meninges». Radiographics, 27, 2, 2007, pàg. 525–51. DOI: 10.1148/rg.272065155. PMID: 17374867.
- ↑ Louis, David N.; Perry, Arie; Reifenberger, Guido; von Deimling, Andreas; Figarella-Branger, Dominique «The 2016 World Health Organization Classification of Tumors of the Central Nervous System: a summary» (en anglès). Acta Neuropathologica, 131, 6, 2016-06, pàg. 803–820. DOI: 10.1007/s00401-016-1545-1. ISSN: 0001-6322.
- ↑ Glioblastoma. ISBN 978-0-9944381-2-6. OCLC 1017991944.
- ↑ Lawson, H. Christopher; Sampath, Prakash; Bohan, Eileen; Park, Michael C.; Hussain, Namath; Olivi, Alessandro; Weingart, Jon; Kleinberg, Lawrence; Brem, Henry «Interstitial chemotherapy for malignant gliomas: the Johns Hopkins experience». Journal of Neuro-Oncology, 83, 1, 2006, pàg. 61–70. DOI: 10.1007/s11060-006-9303-1. PMID: 17171441.
- ↑ Stevens, Glen H. J. «Antiepileptic therapy in patients with central nervous system malignancies». Current Neurology and Neuroscience Reports, 6, 4, 2006, pàg. 311–318. DOI: 10.1007/s11910-006-0024-9. PMID: 16822352.
- ↑ Lacroix, Michel; Abi-Said, Dima; Fourney, Daryl R.; Gokaslan, Ziya L.; Shi, Weiming; Demonte, Franco; Lang, Frederick F.; McCutcheon, Ian E.; Hassenbusch, Samuel J. «A multivariate analysis of 416 patients with glioblastoma multiforme: prognosis, extent of resection, and survival». Journal of Neurosurgery, 95, 2, 2001, pàg. 190–8. DOI: 10.3171/jns.2001.95.2.0190. PMID: 11780887.
- ↑ Stummer, W; Pichlmeier, U; Meinel, T; Wiestler, O; Zanella, F; Reulen, H; Ala-Glioma Study, Group «Fluorescence-guided surgery with 5-aminolevulinic acid for resection of malignant glioma: a randomised controlled multicentre phase III trial». The Lancet Oncology, 7, 5, 2006, pàg. 392–401. DOI: 10.1016/S1470-2045(06)70665-9. PMID: 16648043.
- ↑ Walker, Michael D.; Alexander, Eben; Hunt, William E.; MacCarty, Collin S.; Mahaley, M. Stephen; Mealey, John; Norrell, Horace A.; Owens, Guy; Ransohoff, Joseph «Evaluation of BCNU and/or radiotherapy in the treatment of anaplastic gliomas». Journal of Neurosurgery, 49, 3, 1978, pàg. 333–43. DOI: 10.3171/jns.1978.49.3.0333. PMID: 355604.
- ↑ Showalter, Timothy N.; Andrel, Jocelyn; Andrews, David W.; Curran Jr., Walter J.; Daskalakis, Constantine; Werner-Wasik, Maria «Multifocal Glioblastoma Multiforme: Prognostic Factors and Patterns of Progression». International Journal of Radiation OncologyBiologyPhysics, 69, 3, 2007, pàg. 820–824. DOI: 10.1016/j.ijrobp.2007.03.045. PMID: 17499453.
- ↑ Fulton, DS; Urtasun, RC; Scott-Brown, I; Johnson, ES; Mielke, B; Curry, B; Huyser-Wierenga, D; Hanson, J; Feldstein, M «Increasing radiation dose intensity using hyperfractionation in patients with malignant glioma. Final report of a prospective phase I-II dose response study». Journal of neuro-oncology, 14, 1, 1992, pàg. 63–72. PMID: 1335044.
- ↑ Stupp, Roger; Mason, Warren P.; Van Den Bent, Martin J.; Weller, Michael; Fisher, Barbara; Taphoorn, Martin J.B.; Belanger, Karl; Brandes, Alba A.; Marosi, Christine «Radiotherapy plus Concomitant and Adjuvant Temozolomide for Glioblastoma». New England Journal of Medicine, 352, 10, 2005, pàg. 987–996. DOI: 10.1056/NEJMoa043330. PMID: 15758009.
- ↑ Mason, Warren P.; Mirimanoff, René O.; Stupp, Roger «Radiotherapy with Concurrent and Adjuvant Temozolomide: A New Standard of Care for Glioblastoma Multiforme». Progress in Neurotherapeutics and Neuropsychopharmacology, 1, 2006, pàg. 37–52. DOI: 10.1017/S1748232105000054.
- ↑ «Temozolomide Plus Radiation Helps Brain Cancer – National Cancer Institute». Arxivat de l'original el 2007-08-15. [Consulta: 15 setembre 2007].
- ↑ Chamberlain, Marc C.; Glantz, Michael J.; Chalmers, Lisa; Horn, Alixis; Sloan, Andrew E. «Early necrosis following concurrent Temodar and radiotherapy in patients with glioblastoma». Journal of Neuro-Oncology, 82, 1, 2006, pàg. 81–3. DOI: 10.1007/s11060-006-9241-y. PMID: 16944309.
- ↑ Dall'oglio, Stefano; D'amico, Anna; Pioli, Fabio; Gabbani, Milena; Pasini, Felice; Passarin, Maria Grazia; Talacchi, Andrea; Turazzi, Sergio; Maluta, Sergio «Dose-intensity temozolomide after concurrent chemoradiotherapy in operated high-grade gliomas». Journal of Neuro-Oncology, 90, 3, 2008, pàg. 315–9. DOI: 10.1007/s11060-008-9663-9. PMID: 18688571.
- ↑ FDA Approves Drug for Treatment of Aggressive Brain Cancer
- ↑ Fulci, Giulia; Chiocca, Antonio «The status of gene therapy for brain tumors». Expert Opinion on Biological Therapy, 7, 2, 2007, pàg. 197–208. DOI: 10.1517/14712598.7.2.197. PMC: 2819130. PMID: 17250458.
- ↑ Tai, Chien-Kuo; Jun Wang, Wei; Chen, Thomas C.; Kasahara, Noriyuki «Single-Shot, Multicycle Suicide Gene Therapy by Replication-Competent Retrovirus Vectors Achieves Long-Term Survival Benefit in Experimental Glioma». Molecular Therapy, 12, 5, 2005, pàg. 842–851. DOI: 10.1016/j.ymthe.2005.03.017. PMID: 16257382.
- ↑ http://www.Tocagen.com Arxivat 2020-06-01 a Wayback Machine.
- ↑ «A Study of a Replication Competent Retrovirus Administered to Subjects With Recurrent Glioblastoma (GBM)». ClinicalTrials.gov, gener 2011.
- ↑ «APG101 in Glioblastoma». ClinicalTrials.gov. [Consulta: 27 juny 2012].
- ↑ S. Kleber, I. Sancho-Martinez, B. Wiestler, A. Regnier-Vigouroux, C. Herold-Mende, A. Martin-Villalba «Yes and PI3K Bind CD95 to Signal Invasion of Glioblastoma». Cancer Cell, 13, 3, 11-03-2008, pàg. 235-248. DOI: 10.1016/j.ccr.2008.02.003.
- ↑ «APG101 Exceeds Expectations». Marketwatch. [Consulta: 15 agost 2012].[Enllaç no actiu]
- ↑ Ghebeh, H; Bakr, MM; Dermime, S «Cancer stem cell immunotherapy: the right bullet for the right target». Hematology/oncology and stem cell therapy, 1, 1, 2008, pàg. 1–2. PMID: 20063521.
- ↑ Moviglia, GA; Carrizo, AG; Varela, G; Gaeta, CA; Paes De Lima, A; Farina, P; Molina, H «Preliminary report on tumor stem cell/B cell hybridoma vaccine for recurrent glioblastoma multiforme». Hematology/oncology and stem cell therapy, 1, 1, 2008, pàg. 3–13. PMID: 20063522.
- ↑ A prospective, randomized, open-label, phase III clinical trial of NovoTTF-100A versus best standard of care chemotherapy in patients with recurrent glioblastoma. – Stupp et al. 28 (18): LBA2007 – ASCO Meeting Abstracts. Meeting.ascopubs.org (2010-06-20). Retrieved on 2010-10-19.
- ↑ http://www.cancer.gov/search/ViewClinicalTrials.aspx?cdrid=647437&version=HealthProfessional&protocolsearchid=8237659[Enllaç no actiu]
- ↑ http://www.nutritionandmetabolism.com/content/7/1/33
- ↑ Nieder, C; Adam, M; Molls, M; Grosu, A «Therapeutic options for recurrent high-grade glioma in adult patients: Recent advances». Critical Reviews in Oncology/Hematology, 60, 3, 2006, pàg. 181–93. DOI: 10.1016/j.critrevonc.2006.06.007. PMID: 16875833.
- ↑ 49,0 49,1 49,2 Krex, D.; Klink, B.; Hartmann, C.; Von Deimling, A.; Pietsch, T.; Simon, M.; Sabel, M.; Steinbach, J. P.; Heese, O. «Long-term survival with glioblastoma multiforme». Brain, 130, Pt 10, 2007, pàg. 2596–606. DOI: 10.1093/brain/awm204. PMID: 17785346.
- ↑ «Resultats dels Registres de Tumors Hospitalaris de l'Institut Català d'Oncologia en aliança amb l’Institut Català de la Salut 2013-2017». [Consulta: 30 agost 2020].
- ↑ Martinez, Ramon; Schackert, Gabriele; Yaya-Tur, Ricard; Rojas-Marcos, Iñigo; Herman, James G.; Esteller, Manel «Frequent hypermethylation of the DNA repair gene MGMT in long-term survivors of glioblastoma multiforme». Journal of Neuro-Oncology, 83, 1, 2006, pàg. 91–3. DOI: 10.1007/s11060-006-9292-0. PMID: 17164975.
- ↑ Smoll, Nicolas; Schaller, K; Gautschi OP «The Cure Fraction of Glioblastoma Multiforme». Neuroepidemiology, 39, 1, 2012.
| A Wikimedia Commons hi ha contingut multimèdia relatiu a: Glioblastoma multiforme |
