Tripsina
 | |||||||||
| Identificadors | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Número EC | 3.4.21.4 i 3.4.21.4 | ||||||||
| Número CAS | 9002-07-7
| ||||||||
| Bases de dades | |||||||||
| IntEnz | IntEnz view i IntEnz view | ||||||||
| BRENDA | BRENDA entry i BRENDA entry | ||||||||
| ExPASy | NiceZyme view i NiceZyme view | ||||||||
| KEGG | KEGG entry i KEGG entry | ||||||||
| MetaCyc | metabolic pathway i metabolic pathway | ||||||||
| PRIAM | profile i profile | ||||||||
| Estructures PDB | RCSB PDB PDBj PDBe PDBsum i RCSB PDB PDBj PDBe PDBsum | ||||||||
| Gene Ontology | AmiGO / EGO | ||||||||
| |||||||||
 | |
| Substància | família d'enzims |
|---|---|
| Nombre EC | 3.4.21.4 |
| Locus | Cr. 7 q32-qter |
| Identificadors | |
| Símbol | Tripsina 1 TRY1 |
| HUGO | 9475 |
| Entrez | 5644 |
| OMIM | 276000 |
| RefSeq | NM_002769 |
| P07477 | |
 | |
| Substància | família d'enzims |
|---|---|
| Locus | Cr. 7 q35 |
| Identificadors | |
| Símbol | PRSS2 |
| HUGO | 9483 |
| Entrez | 5645 |
| OMIM | 601564 |
| RefSeq | NM_002770 |
| P07478 | |
 | |
| Substància | família d'enzims |
|---|---|
| Nombre EC | 3.4.21.4 |
| Locus | Cr. 9 p13 |
| Identificadors | |
| Símbol | PRSS3 PRSS4 |
| HUGO | 9486 |
| Entrez | 5646 |
| RefSeq | NM_002771 |
| P35030 | |
La tripsina[2] és una proteasa de serina trobada al sistema digestiu de molts vertebrats. A aquests organismes hi assumeix la funció d'hidrolitzar les proteïnes.[3] La tripsina és produïda al pàncrees en forma del proenzim inactiu tripsinogen. La tripsina predominantment trenca les cadenes peptídiques per l'extrem carboxil dels aminoàcids lisina o arginina, excepte quan un d'aquests dos aminoàcids és seguit per una prolina. El procés és popularment conegut com la proteòlisi per tripsina o tripsinització, una proteïna està tripsinitzada quan ha estat digerida/tractada amb tripsina. Aquesta propietat de la tripsina per trencar proteïnes fa que aquesta s'utilitzi en nombrosos processos biotecnològics.
Funció i estructura[modifica]
La tripsina és secretada al duodè, on actua hidrolitzant pèptids, trencant els enllaços entre aminoàcids. Els pèptids tractats per tripsina han estat modificats anteriorment per la pepsina, un altre enzim. Això és necessari per a l'assimilació de les proteïnes dels aliments, ja que els pèptids són més petits que les proteïnes, però són encara massa grans per a ser absorbits a través de la paret de l'ili. La tripsina, com enzim que és, catalitza aquesta reacció.
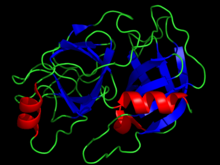
El mecanisme enzimàtic de la tripsina és similar al d'altres proteases de serina. Aquests enzims contenen una tríada catalítica que consisteix en histidina-57, aspartat-102 i serina-195.[4] Aquests formen un gradient de càrrega que fa tornar el centre actiu de la serina nucleofílic. Això s'aconsegueix mitjançant la modificació del medi electroestàtic de la serina. La reacció enzimàtica que catalitza la tripsina és termodinàmicament favorable però requereix una certa energia d'activació, ja que és "cinèticament desfavorable". A més, la tripsina conté un “forat oxianió”, format pels àtoms d'hidrogen de l'amida que fa de columna vertebral de la Gly-193 i Ser-195, que serveix per estabilitzar la càrrega negativa en desenvolupament sobre l'àtom d'oxigen del carbonil de l'amida. El residu d'aspartat (Asp 189) és responsable de captar i estabilitzar la lisina o arginina carregades positivament, i és per tant responsable de l'especificitat de l'enzim. Això significa que la major part de la tripsina trenca les proteïnes per l'extrem carboxil dels aminoàcids lisina i arginina, excepte quan un és seguit per la prolina.[5] La tripsina és considerada una endopeptidasa, és a dir, la divisió es produeix al mig de la cadena polipeptídica en lloc de als àcids amino terminal, als extrems de la cadena. La tripsina funciona a ple rendiment quan el pH és 8 (pH òptim) i una temperatura d'uns 37 °C (temperatura òptima de funcionament.[5]
La tripsina és produïda al pàncrees, en forma de zimogen inactiu, el tripsinogen. Quan el pàncrees és estimulat per la colecistocinina el tripsinogen és secretat a l'intestí prim. Un cop arriba a l'intestí prim, l'enzim enteropeptidasa l'activa transformant-lo en tripsina per trencament proteolític. La tripsina resultant activa altres tripsinògens que estiguin inactius, és el que s'anomena autocatàlisi. Com podem veure una petita quantitat d'enteropeptidasa és necessària per iniciar la reacció. Aquest mecanisme d'activació és comú per a la majoria de les proteases de serina i serveix per prevenir l'autodigestió del pàncrees. L'activitat de la tripsina no es veu afectada per l'inhibidor de la tosilo clorometilcetona fenilalanil, TPCK, que desactiva la quimotripsina. Això és important perquè, en algunes aplicacions, com l'espectrometria de masses, l'especificitat de l'escissió és important.
Relació de la tripsina amb algunes malalties[modifica]
Una conseqüència de la malaltia de la fibrosi cística o mucoviscidosis és una malaltia hereditària autosòmica recessiva que és provocada per una deficiència en el transport de la tripsina i altres enzims digestius del pàncrees. Això ens porta al trastorn anomenat ili meconial. Aquest trastorn consisteix en l'obstrucció intestinal de l'ili a causa de l'excés de meconi espès que en situacions normals es descompon per la tripsina i altres proteases per passar finalment a l'aparell excretor i ser expulsat.[6] Un altre problema pot sorgir a través de la deficiència d'alfa-1-antitripsina, en la qual el cos crea anticossos alfa-1-antitripsina, en contra de la tripsina. Això porta a una sèrie de complicacions d'òrgans en cascada, que afecten el fetge, els pulmons i la pell.
Emmagatzematge[modifica]
La tripsina s'ha d'emmagatzemar a temperatures molt baixes (entre -20 °C i -80 °C) per evitar l'autòlisi. També es pot prevenir mitjançant l'emmagatzematge de tripsina a pH 3 o mitjançant l'ús de la tripsina modificada per exemple, amb la metilació reductiva. Quan s'ajusta el pH torna de nou a l'activitat en un pH de 8.
Aplicacions[modifica]
- La tripsina es troba en gran quantitat al pàncrees i pot ser purificada amb força facilitat. Per això s'utilitza en diversos processos biotecnològics.
- La tripsina s'empra per rompre les proteïnes que permeten les unions entre cèl·lules. Això és causat per la capacitat que té la tripsina de trencar, com hem dit, els enllaços entre proteïnes. En el laboratori de cultiu de teixits, aquest procés s'utilitza en la collita de les cèl·lules cultivades a plaques de petri.
- És útil per dissociar les cèl·lules disseccionades (per exemple, abans de la fixació de cèl·lules i la seva classificació).
- Serveix per trencar la caseïna de la llet materna. Si la tripsina s'afegeix a una solució de llet en pols, el desglossament de la caseïna farà que la llet sigui transparent. La velocitat de reacció es pot mesurar mitjançant l'ús de la quantitat de temps que triga la llet a tornar-se transparent.
- La tripsina és una proteïna de la qual es fa ús en la investigació biològica, concretament als experiments proteòmics per digerir les proteïnes en pèptids per a l'anàlisi d'espectrometria de masses. La tripsina és especialment adequada per això, ja que té una especificitat molt ben definida, a causa del fet que només s'hidrolitzen els enllaços peptídics en els quals el grup carbonil és donat per un residu de Lys o bé Arg.
- També pot ser utilitzada per a dissoldre els coàguls de sang en la seva forma microbiana i en el tractament de la inflamació en la seva forma pancreàtica.
- S'utilitza en els aliments infantils preparats per tal de predigerir-los. Aquest enzim trenca les molècules proteiques, procés que ajuda al nadó a pair tot allò que el seu estómac no és capaç de digerir, com per exemple, les proteïnes de mida gran.
Referències[modifica]
- ↑ PDB 1UTN; Leiros HK, Brandsdal BO, Andersen OA, Os V, Leiros I, Helland R, Otlewski J, Willassen NP, Smalås AO «Trypsin specificity as elucidated by LIE calculations, X-ray structures, and association constant measurements». Protein Sci., 13, 4, April 2004, pàg. 1056–70. DOI: 10.1110/ps.03498604. PMC: 2280040. PMID: 15044735.
- ↑ (EC 3.4.21.4)
- ↑ Rawlings ND, Barrett AJ «Families of serine peptidases». Meth. Enzymol., 244, 1994, pàg. 19–61. PMID: 7845208.
- ↑ Polgár L «The catalytic triad of serine peptidases». Cell. Mol. Life Sci., 62, 19-20, October 2005, pàg. 2161–72. DOI: 10.1007/s00018-005-5160-x. PMID: 16003488.
- ↑ 5,0 5,1 «Sequencing Grade Modified Trypsin». www.promega.com, 01-04-2007. Arxivat de l'original el 2003-05-19. [Consulta: 8 febrer 2009].
- ↑ Noone PG, Zhou Z, Silverman LM, Jowell PS, Knowles MR, Cohn JA «Cystic fibrosis gene mutations and pancreatitis risk: relation to epithelial ion transport and trypsin inhibitor gene mutations». Gastroenterology, 121, 6, December 2001, pàg. 1310–9. PMID: 11729110.
Enllaços externs[modifica]
| A Wikimedia Commons hi ha contingut multimèdia relatiu a: Tripsina |
- Trypsin Inhibitors Arxivat 2008-04-23 a Wayback Machine. and Trypsin Assay Method at Sigma-Aldrich
- «Tripsina» (en anglès). Medical Subject Headings.
