Organoide: diferència entre les revisions
Robot catalanitza noms i paràmetres de plantilles |
#1Lib1Ref |
||
| Línia 1: | Línia 1: | ||
[[Fitxer:Intestinal_organoid.PNG|thumb|'''Organoid''' Intestinal crescut de cèl·lules mare Lgr5+.]] |
[[Fitxer:Intestinal_organoid.PNG|thumb|'''Organoid''' Intestinal crescut de cèl·lules mare Lgr5+.]] |
||
Un '''organoid''', informalment també conegut com a '''miniòrgan'''{{ |
Un '''organoid''', informalment també conegut com a '''miniòrgan''',<ref>{{Ref-publicació|cognom=Miravalls|nom=Julio|article=Organoides, la 'fábrica' de tejido humano|publicació=EL MUNDO|llengua=castellà|url=http://www.elmundo.es/economia/2017/07/24/5975be36468aeb37548b4629.html|data=03-08-2017|pàgines=|citació=El proceso para generar un mini-órgano requiere unos 10 días y el resultado es un tejido de unos milímetros.}}</ref> és un [[Òrgan (anatomia)|òrgan]] [[tridimensional]] ''mínim'' crescut [[in vitro]]. La tècnica per créixer organoids ràpidament des de principis del 2010, i poc després ja va ser considerat un dels avenços científics més significatius del moment.<ref>{{Cite web|last=Kerry Grens|title=2013’s Big Advances in Science|url=http://www.the-scientist.com/?articles.view/articleNo/38747/title/2013-s-Big-Advances-in-Science/|publisher=''[[The Scientist]]''|accessdate=26 December 2013|date=December 24, 2013}}</ref> |
||
== Història == |
== Història == |
||
Revisió del 15:12, 31 gen 2018
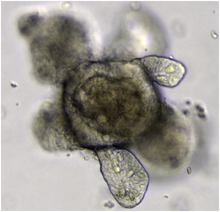
Un organoid, informalment també conegut com a miniòrgan,[1] és un òrgan tridimensional mínim crescut in vitro. La tècnica per créixer organoids ràpidament des de principis del 2010, i poc després ja va ser considerat un dels avenços científics més significatius del moment.[2]
Història
El 2008 Yoshiki Sasai i el seu equip a l'institut RIKEN van demostrar que les cèl·lules mare poden agrupar-se en boles de cèl·lules neuronals que poden organitzar-se en capes diferenciades.[3] El 2009 el Laboratori de Hans Clevers a l'Institut Hubrecht i el Centre Mèdic Universitari d'Utrecht, als Països Baixos, van demostrar que només a partir de cèl·lules mare LGR5 podien generar estructures velloses sense caldre una base mesenquimal.[4]
El 2013, Madeline Lancaster a l'Acadèmia austríaca de Ciències va establir un protocol per al cultiu d'organoids cerebrals derivats de cèl·lules mare per tal d'imitar l'organització cel·lular del cervell humà en desenvolupament.[5] El 2014, Artem Shkumatov et al. A la Universitat d'Illinois a Urbana-Champaign va demostrar que podien crear-se organoids cardiovasculars a partir de cèl·lules d'ES modulant la rigidesa del substrat al qual s'adherien. La rigidesa fisiològica promovia la tridimensionalitat dels EBs i la diferenciació cardiomiogènica.[6]
Takebe et al. va demostrar un mètode generalitzat per a miniorgans formats a partir de teixits diversos combinant progenitors específics de teixits derivades de cèl·lules mare pluripotents o mostres de teixit pertinent amb cèl·lules mare endotelials i mesenquimals (MSC). Es va suggerir que els teixits menys madurs, o els miniòrgans, generats a partir del principi de condensació autoorganitzada podria ser l'aproximació més eficaç cap a la reconstitució de funcions d'òrgan madur després d'un trasplantament, més que no condensats generats de cèl·lules d'una etapa més avançada[7]
Tipus d'organoids
- Organod cererbal
- Organoid tiroïdeu[8]
- Organoid intestinal
- Organoid testicular
- Organoid hepàtic[9]
- Organoid pancreàtic[10]
- Organoid gàstric[11]
- Organoid epitelial[4][12]
- Organoid pulmonar[13]
- Organoid renal[14][15][16]
- Embrionari (Gastruloids)[17][18]
Organoids com a models de malaltia
Els organoids proporcionen una oportunitat per a crear models cel·lulars de malalties humana, els quals poden ser estudiats en el laboratori per a millor la comprensió de les causes de la malaltia i identificar tractaments possibles. Com a exemple, l'edició del genoma amb el sistema CRISPR va aplicar-se a cèl·lules mare pluripotents per tal d'introduir mutacions específiques en gens implicats en dues malalties renals: la poliquistosi renal i la glomerulosclerosis segmental focal.[19] Aquestes cèl·lules mare pluripotents modificades amb CRISPR van ser cultivades com un miniòrgan renal, que va arribar a exhibir els fenotips associats a la malaltia. Paral·lelament, aquests fenotips no es presentaven en aquells organoids que sense mutacions CRISPR.[19] Aquests experiments demostren l'ús d'organoids com a models més complexos de malalties en el laboratori, anant un pas més enllà dels teixits cultivats en un placa de petri.
Bibliografia
- Willyard, Cassandra «The boom in mini stomachs, brains, breasts, kidneys and more». Nature, vol. 523, 2015, pàg. 520–522. DOI: 10.1038/523520a.
- Kelly Rae Chi (2015). Orchestrating Organoids. A guide to crafting tissues in a dish that reprise in vivo organs. The Scientist.
- Takebe, T., Enomura, M., Yoshizawa, E., Kimura, M., Koike, H., Ueno, Y., ... & Taniguchi, H. (2015). Vascularized and Complex Organ Buds from Diverse Tissues via Mesenchymal Cell-Driven Condensation. Cell stem cell, 16(5), 556-565. DOI:10.1016/j.stem.2015.03.004
- Turner DA, Baillie-Johnson P, Martinez Arias, A (2016). "Organoids and the genetically encoded self-assembly of embryonic stem cells". Bioassays 38 (2): 181-91. doi: 10.1002/bies.201500111
Referències
- ↑ Miravalls, Julio «Organoides, la 'fábrica' de tejido humano» (en castellà). EL MUNDO, 03-08-2017. «El proceso para generar un mini-órgano requiere unos 10 días y el resultado es un tejido de unos milímetros.»
- ↑ Kerry Grens. «2013’s Big Advances in Science». The Scientist, December 24, 2013. [Consulta: 26 December 2013].
- ↑ Ed Yong. «Lab-Grown Model Brains». The Scientist, August 28, 2013. [Consulta: 26 December 2013].
- ↑ 4,0 4,1 Sato, Toshiro; Vries, Robert G.; Snippert, Hugo J.; Van De Wetering, Marc; Barker, Nick; Stange, Daniel E.; Van Es, Johan H.; Abo, Arie; Kujala, Pekka «Single Lgr5 stem cells build cryptvillus structures in vitro without a mesenchymal niche». Nature, vol. 459, 7244, 2009, pàg. 262–5. Bibcode: 2009Natur.459..262S. DOI: 10.1038/nature07935. PMID: 19329995.
- ↑ Chambers, Stuart M.; Tchieu, Jason; Studer, Lorenz «Build-a-Brain». Cell Stem Cell, vol. 13, 4, October 2013, pàg. 377–8. DOI: 10.1016/j.stem.2013.09.010. PMID: 24094317.
- ↑ ; Baek, K; Kong, H «Matrix Rigidity-Modulated Cardiovascular Organoid Formation from Embryoid Bodies». PLoS ONE, vol. 9, 4, 2014, pàg. e94764. Bibcode: 2014PLoSO...994764S. DOI: 10.1371/journal.pone.0094764. PMC: 3986240. PMID: 24732893.
- ↑ Takebe, T.; Enomura, M.; Yoshizawa, E.; Kimura, M.; Koike, H.; Ueno, Y.; Taniguchi, H. «Vascularized and Complex Organ Buds from Diverse Tissues via Mesenchymal Cell-Driven Condensation». Cell stem cell, vol. 16, 5, 2015, pàg. 556–565. DOI: 10.1016/j.stem.2015.03.004.
- ↑ Martin, Andreas; Barbesino, Giuseppe; Davies, Terry F. «T-Cell Receptors and Autoimmune Thyroid Disease—Signposts for T-Cell-Antigen Driven Diseases». International Reviews of Immunology, vol. 18, 1–2, 1999, pàg. 111–40. DOI: 10.3109/08830189909043021. PMID: 10614741.
- ↑ ; Gehart, H; Van Boxtel, R; Hamer, K; Blokzijl, F; Verstegen, M. M.; Ellis, E; Van Wenum, M; Fuchs, S. A. «Long-Term Culture of Genome-Stable Bipotent Stem Cells from Adult Human Liver». Cell, vol. 160, 1–2, 2015, pàg. 299–312. DOI: 10.1016/j.cell.2014.11.050. PMC: 4313365. PMID: 25533785.
- ↑ ; Bonfanti, P; Boj, S. F.; Sato, T; Loomans, C. J.; Van De Wetering, M; Sojoodi, M; Li, V. S.; Schuijers, J «Unlimited in vitro expansion of adult bi-potent pancreas progenitors through the Lgr5/R-spondin axis». The EMBO Journal, vol. 32, 20, 2013, pàg. 2708–2721. DOI: 10.1038/emboj.2013.204. PMC: 3801438. PMID: 24045232.
- ↑ ; Koo, B. K.; Huch, M; Sibbel, G; Basak, O; Lyubimova, A; Kujala, P; Bartfeld, S; Koster, J «Differentiated Troy+ chief cells act as 'reserve' stem cells to generate all lineages of the stomach epithelium». Cell, vol. 155, 2, 2013, pàg. 357–368. DOI: 10.1016/j.cell.2013.09.008. PMC: 4094146. PMID: 24120136.
- ↑ Barker, Nick; Van Es, Johan H.; Kuipers, Jeroen; Kujala, Pekka; Van Den Born, Maaike; Cozijnsen, Miranda; Haegebarth, Andrea; Korving, Jeroen; Begthel, Harry «Identification of stem cells in small intestine and colon by marker gene Lgr5». Nature, vol. 449, 7165, 2007, pàg. 1003–7. Bibcode: 2007Natur.449.1003B. DOI: 10.1038/nature06196. PMID: 17934449.
- ↑ Lee, Joo-Hyeon; Bhang, Dong Ha; Beede, Alexander; Huang, Tian Lian; Stripp, Barry R.; Bloch, Kenneth D.; Wagers, Amy J.; Tseng, Yu-Hua; Ryeom, Sandra «Lung Stem Cell Differentiation in Mice Directed by Endothelial Cells via a BMP4-NFATc1-Thrombospondin-1 Axis». Cell, vol. 156, 3, pàg. 440–455. DOI: 10.1016/j.cell.2013.12.039. ISSN: 0092-8674. PMC: 3951122. PMID: 24485453.
- ↑ Takasato, Minoru; Er, Pei X.; Chiu, Han S.; Maier, Barbara; Baillie, Gregory J.; Ferguson, Charles; Parton, Robert G.; Wolvetang, Ernst J.; Roost, Matthias S. «Kidney organoids from human iPS cells contain multiple lineages and model human nephrogenesis». Nature, vol. 526, 7574, pàg. 564–568. DOI: 10.1038/nature15695.
- ↑ Freedman, BS; Brooks, CR; Lam, AQ; Fu, H; Morizane, R; Agrawal, V; Saad, AF; Li, MK; Hughes, MR «Modelling kidney disease with CRISPR-mutant kidney organoids derived from human pluripotent epiblast spheroids.». Nature communications, vol. 6, 23-10-2015, pàg. 8715. DOI: 10.1038/ncomms9715. PMID: 26493500.
- ↑ Morizane, Ryuji; Lam, Albert; Freedman, Benjamin; Kishi, Seiji; Valerius, Todd; Bonventre, Joseph «Nephron organoids derived from human pluripotent stem cells model kidney development and injury.». Nature Biotechnology, vol. 33, 11, pàg. 1193–1200. DOI: 10.1038/nbt.3392.
- ↑ van den Brink, Susanne C.; Baillie-Johnson, Peter; Balayo, Tina; Hadjantonakis, Anna-Katerina; Nowotschin, Sonja; Turner, David A.; Martinez Arias, Alfonso «Symmetry breaking, germ layer specification and axial organisation in aggregates of mouse embryonic stem cells». Development (Cambridge, England), vol. 141, 22, 01-11-2014, pàg. 4231–4242. DOI: 10.1242/dev.113001. ISSN: 1477-9129. PMC: 4302915. PMID: 25371360.
- ↑ Turner, David A.; Baillie-Johnson, Peter; Martinez Arias, Alfonso «Organoids and the genetically encoded self-assembly of embryonic stem cells». BioEssays: News and Reviews in Molecular, Cellular and Developmental Biology, vol. 38, 2, 01-02-2016, pàg. 181–191. DOI: 10.1002/bies.201500111. ISSN: 1521-1878. PMID: 26666846.
- ↑ 19,0 19,1 Freedman, BS; Brooks, CR; Lam, AQ; Fu, H; Morizane, R; Agrawal, V; Saad, AF; Li, MK; Hughes, MR «Modelling kidney disease with CRISPR-mutant kidney organoids derived from human pluripotent epiblast spheroids.». Nature communications, vol. 6, 23-10-2015, pàg. 8715. PMID: 26493500.
