Solut: diferència entre les revisions
m Robot treu enllaç igual al text enllaçat |
coa ----> cosa |
||
| Línia 2: | Línia 2: | ||
Un '''solut''', en una [[dissolució]], és el compost en menor proporció respecte el [[solvent]].<ref>{{Harvsp|Silvestroni|p.229}}</ref> En el llenguatge comú, el solut també es coneix com "la substància que es dissol",<ref>Canales, Margarita ''Fisicoquímica'' Volumen I: Teoría.</ref> per la qual cosa es pot trobar en un [[estat d'agregació de la matèria|estat d'agregació]] diferent al de l'inici del procés de dissolució i experimentar una [[transició de fase]]. |
Un '''solut''', en una [[dissolució]], és el compost en menor proporció respecte el [[solvent]].<ref>{{Harvsp|Silvestroni|p.229}}</ref> En el llenguatge comú, el solut també es coneix com "la substància que es dissol",<ref>Canales, Margarita ''Fisicoquímica'' Volumen I: Teoría.</ref> per la qual cosa es pot trobar en un [[estat d'agregació de la matèria|estat d'agregació]] diferent al de l'inici del procés de dissolució i experimentar una [[transició de fase]]. |
||
El més comú és que el solut sigui un [[sòlid]] en un dissolvent [[líquid]], |
El més comú és que el solut sigui un [[sòlid]] en un dissolvent [[líquid]], cosa que origina una solució líquida. Una de las característiques més significatives d'una dissolució acostuma a ser la seva concentració de solut, és a dir, la mitjana de la quantitat de solut continguda en ella. |
||
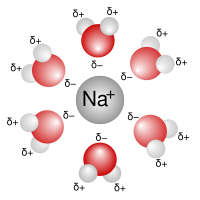
[[Fitxer:Na+H2O.svg|thumb|200px|[[Solvatació]] d'un [[Ió (àtom) |ió]] de [[sodi]] en aigua.]] |
[[Fitxer:Na+H2O.svg|thumb|200px|[[Solvatació]] d'un [[Ió (àtom) |ió]] de [[sodi]] en aigua.]] |
||
Revisió del 21:55, 22 feb 2016

Un solut, en una dissolució, és el compost en menor proporció respecte el solvent.[1] En el llenguatge comú, el solut també es coneix com "la substància que es dissol",[2] per la qual cosa es pot trobar en un estat d'agregació diferent al de l'inici del procés de dissolució i experimentar una transició de fase.
El més comú és que el solut sigui un sòlid en un dissolvent líquid, cosa que origina una solució líquida. Una de las característiques més significatives d'una dissolució acostuma a ser la seva concentració de solut, és a dir, la mitjana de la quantitat de solut continguda en ella.
Una altra característica significativa seria la facilitat per a dissoldre's o la solubilitat que pugui presentar en el dissolvent. La solubilitat d'un compost químic depèn en gran mesura de la seva estructura molecular. En general, els compostos iònics i moleculars polars són solubles en dissolvents polars com l'aigua o l'etanol; i els compostos moleculars apolars en dissolvents apolars com l'hexà, l'èter o el tetraclorur de carboni.
Referències
- ↑ Silvestroni p.229
- ↑ Canales, Margarita Fisicoquímica Volumen I: Teoría.
Bibliografia
- Fondamenti di chimica (en italià). Bologna : Milano: Zanichelli ; CEA, 1996. ISBN 88-408-0998-8.
- Elettrochimica (en italià). Elsevier, 1976, p. 454. ISBN 88-214-0500-1.
