Química organometàl·lica

La química organometàl·lica és una branca de la química que estudia els composts organometàl·lics, composts que contenen un o més àtoms de carboni enllaçats directament a un àtom d'un metall mitjançant enllaç covalent.
Els organometàl·lics es diferencien del complexos de coordinació perquè aquests tenen càrrega elèctrica, presenten un nombre variable d'electrons d i són solubles en aigua. Els composts organometàl·lics, per contra, solen ser neutres, tenen un nombre fix d'electrons d i són solubles en dissolvents orgànics. Els organometàl·lics es classifiques segon el metall amb el prefix organo-, per exemple composts d'organocrom. S'inclouen també, a més dels metalls tradicionals, alguns metal·loides (bor, silici, arsènici i seleni). Els composts d'un metall amb carbonils, com ara el tetracarbonil de níquel [Ni(CO)₄] són considerats organometàl·lics malgrat el monòxid de carboni CO sigui un compost inorgànic; però no són considerats organometàl·lics els compostos d'un metall amb cianur, com [Fe(CN)₆]4–. Dos organometàl·lics que es troben a la natura són el coenzim de vitamina B₁₂, que conté un enllaç cobalt-carboni (Co―C) i el dimetilmercuri, H₃C―Hg―CH₃, que es produeix per bacteris per eliminar el mercuri metàl·lic tòxic. No obstant això, els compostos organometàl·lics són generalment inusuals en els processos biològics. L'ús majoritari del organometàl·lics és com a catalitzadors i com a reactius en química orgànica.
Història[modifica]
1760-1899[modifica]
La química organometàl·lica té el seu origen el 1760 a París. En una farmàcia militar, el químic i farmacèutic Louis Claude Cadet de Gassicourt (1731-1799) obtingué un líquid vermellós per reacció d'acetat de potassi amb triòxid de diarseni. Aquest líquid fou anomenat «licor fumant de Cadet» i conté els composts cacodil i òxid de cacodil, els primers compostos organometàl·lics que es varen sintetitzar. La reacció és:
El 1827 el químic danès William Christopher Zeise (1789-1847) sintetitzà el primer complex π, l'anomenada sal de Zeise.[1]

A mitjans de la dècada de 1850, el químic anglès Edward Frankland (1825-1889) sintetitzà diversos complexos metàl·lics alquil sensibles a l'aire: ZnEt₂ (1849), HgEt₂ (1852), SnEt₄ i BMe₃ (1860). La primera síntesi fou:
Els alquilmercuris i els alquilzinc es poden emprar per sintetitzar molts altres organometàl·lics. Per exemple, el químic alemany Charles Friedel (1832-1899) i l'estatunidenc James Mason Crafts (1839-1917) prepararen diversos organoclorosilans RnSiCl4–n per reaccions de SiCl₄ amb ZnR₂ (1863). Poc després, el químic francès Paul Schützenberger (1829-1897) sintetitzà els primers derivats metàl·lics-carbonílics [Pt(CO)₂Cl₂] i [Pt(CO)Cl₂]₂ (1868-1870). Vint anys després, se sintetitzaren els primers composts binaris metall-carbonil: [Ni(CO)₄] per l'alemany Ludwig Mond el 1890 i [Fe(CO)₅] de Mond i del francès Marcellin Berthelot (1827-1907) el 1891.
A partir de 1893 i durant un període de vint anys, el químic suís Alfred Werner (1866–1919) desenvolupà les idees modernes de química inorgànica en la seva proposta segons que l'ió Co3+ està envoltat per sis lligands en un complex octaèdric [CoL₆]3+. Aquestes idees eren contràries a les proposades pels químics destacats d'aquell temps, com el del químic danès Sophus Mads Jørgensen (1837-1914), segons qui els lligands haurien d'estar alineats en una cadena amb el metall al final.[1]

1900-1949[modifica]
Al tombant del segle XX quan es produí una contribució important per part del químic francès Philippe Barbier (1848-1922) i especialment del seu estudiant Victor Grignard (1871-1935). Grignard obtingué el 1900 per la reacció de magnesi amb halogenurs orgànics RX, mitjançant addició oxidativa, els ara anomenats reactius de Grignard RMgX (X=Cl, Br, I), que permeten alquilar derivats carbonílics.[2]
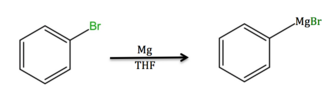
Aquest descobriment tengué un enorme impacte, no només en la química orgànica, sinó també en resultà ser de considerable importància en la química organometàl·lica dels metalls de transició. Per exemple, el 1919, el químic alemany Franz Hein (1892-1976) sintetitzà el que creia que era un polifenilcromoderivat [(Cr(σ-Ph)n]: No obstant això, uns 36 anys més tard, es revelà que el compost posseeix una estructura tipus sandvitx.[1]
La primera meitat del segle XX fou especialment destacable per l'aparició de la catàlisi. La distinció entre catàlisi homogènia i heterogènia fou delimitada pel químic francès Paul Sabatier (1854-1941) que havia sigut alumne de Berthelot. El treball de Sabatier i Jean-Baptiste Senderens (1856-1937) sobre la hidrogenació heterogènia de les olefines a hidrocarburs saturats amb níquel finalment van conduir a un Premi Nobel compartit el 1912 entre Sabatier i Grignard. Molts descobriments seminals, però, es feren a Alemanya durant aquesta primera meitat del segle xx. El 1922, Fischer i Hans Tropsch (1889-1935) informaren de la reacció catalitzada heterogènia entre CO i H₂ (gas de síntesi) per donar mescles d'alcans lineals i alquens amb pocs composts oxigenats com a subproductes (procés Fischer-Tropsch, desenvolupat industrialment el 1925). El 1938, l'alemany Otto Roelen (1897-1993) descobrí la catàlisi per [Co₂(CO)₈] de la hidroformilació d'olefines per CO i H₂ (procés oxo). Des de 1939 fins a finals de la dècada de 1940, l'alemany Walter Reppe (1892-1969) treballà en la catàlisi de transformació d'alquins (tetramerització a ciclooctatetraè, 1948). Curiosament, només hi va haver alguns avenços en el descobriment de nous complexos durant aquest període. A més del iodotrimetilplatí, [PtMe₃I], sintetitzat per l'anglès William Jackson Pope (1870-1939) a principis del segle xx, la llista inclou [Fe(η4-butadiè)(CO)₃] fet per Reilhen el 1930 i el treball de l'alemany Walter Hieber (1895-1976) sobre carbonils metàl·lics a partir de 1928 (per exemple, síntesi de [Fe(H)₂(CO)₄], 1931).[1]

1950-actualitat[modifica]
El 1952, el químic teòric alemany Ernst Otto Fischer (1918-2007) i el químic britànic Geoffrey Wilkinson (1921-1996) descobriren independentment l'estructura sandvitx del ferrocè, sintetitzat l'any anterior pel químic alemany Peter L. Pauson (1925-2013) i l'estatunidenc Thomas J. Kealy (1927-2012).[3]



Des de la dècada de 1950, la química organometàl·lica s'ha convertit en un camp molt actiu, marcat pel descobriment de nous compostos organometàl·lics juntament amb la seva detallada caracterització estructural i química i la seva aplicació com a intermediaris sintètics i catalitzadors en processos industrials. El 1963 l'alemany Karl Ziegler (1898-1973) sintetitzà i l'italià Giulio Natta (1903-1979) aplicà un catalitzador organometàl·lic d'alumini [(Al(C₂H₅)₂Cl)] per a l'obtenció de polímers. Per aquest descobriment reberen el Premi Nobel de Química el 1963.[4] Els descobriments paral·lels de Fischer i Wilkinson possibilitaren la posterior síntesi d'altres compostos amb estructures sandvitx, i el 1973 foren guardonats conjuntament amb el Premi Nobel de Química per les seves contribucions a l'estudi dels compostos sandvitx.[5] Fischer y l'estatunidenc Richard Royce Schrock (1945) el 1973 sintetitzaren els primers organometàl·lics de carbè i carbí [(CO)₄Cr=CR₂] i [(CO)₄CrCR]. El 2001 reberen el Premi Nobel de Química l'estatunidenc William S. Knowles (1917-2012), el japonès Ryōji Noyori (1938) i l'estatunidenc Karl Barry Sharpless (1941) pels catalitzadors de reaccions d'hidrogenació i oxidació quirals.[6] El 2005 el francès Yves Chauvin (1930-2015), i els estatunidencs Robert Howard Grubbs (1942) i Richard Royce Schrock pel desenvolupament en química orgànica del mètode de la metàtesi gràcies a la síntesi d'una àmplia gamma de catalitzadors.[7] El 2010 foren guardonats amb el Premi Nobel de Química l'estatunidenc Richard Fred Heck (1931-2015), i els japonesos Ei-ichi Negishi (1935-2021) i Akira Suzuki (1930) pel desenvolupament de catalitzadors de pal·ladi per a reaccions d'acoblament útils en química orgànica.[8]
Els composts organometàl·lics[modifica]
Característiques[modifica]

Els compostos organometàl·lics es classifiquen en funció del metall com a compostos de metalls de grup principal de la taula periòdica o compostos de metalls de transició. Els metalls del grup principal dels compostos organometàl·lics es consideren típicament els del bloc s (grups 1 i 2) i els elements més pesants del bloc p (grups 13-15). Els metalls de transició inclouen els elements en els blocs d i f (grups 3-12).[9]

Les propietats físiques i químiques dels compostos organometàl·lics varien molt. La majoria són sòlids, especialment aquells els grups d'hidrocarburs dels quals tenen forma d'anell o aromàtics, però alguns són líquids i altres són gasos. La seva estabilitat amb la temperatura i oxidació varia molt. Alguns són molt estables, però una sèrie de compostos d'elements electropositius com el liti, el sodi i l'alumini són inflamables espontàniament. Molts compostos organometàl·lics són altament tòxics, especialment aquells que són volàtils.[9]
Les propietats dels compostos organometàl·lics depenen en gran manera del tipus d'enllaços carboni-metall implicats.
- Alguns són enllaços covalents ordinaris, en els quals es comparteixen parells d'electrons entre els carbonis i el metall, com el cas del dimetilmercuri.
- Altres són enllaços covalents multicèntrics, en els quals l'enllaç implica més de dos àtoms. Per exemple el ferrocè.
- Un tercer tipus són els enllaços iònics, en els quals el parell d'electrons d'unió és donat per un sol àtom.

En els enllaços donant-acceptor, l'àtom metàl·lic està connectat a hidrocarburs amb múltiples enllaços entre els àtoms de carboni. Quan els àtoms metàl·lics formen enllaços covalents amb àtoms de carboni, els electrons solen compartir-se desigualment. Com a resultat, l'enllaç es polaritza iun extrem és més negatiu que l'altre. L'extensió de la polarització depèn de la força amb què l'àtom metàl·lic uneix els electrons. Els compostos organometàl·lics oscil·len en la potència polar des del metilassi, en què l'enllaç és gairebé com certs enllaços iònics, per conduir, la qual cosa enllaça amb el carboni amb molt poca polarització.[9]
Usos[modifica]

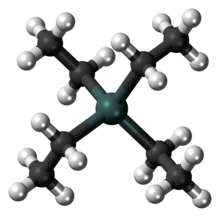
Els compostos organometàl·lics constitueixen un grup molt gran de substàncies que han tingut un paper important en el desenvolupament de la química. S'utilitzen en gran manera com a catalitzadors (substàncies que augmenten la taxa de reaccions sense consumir-se) i com a intermedis al laboratori i a la indústria. A causa de la polaritat dels enllaços, molts compostos organometàl·lics tenen reactivitats que els han fet importants en la síntesi química. Els halurs d'organomagnesi (reactius de Grignard), per exemple, s'utilitzen àmpliament en síntesi de química orgànica, així com en compostos organoliti i organobor. Els compostos d'alquilalumini també s'utilitzen en la síntesi orgànica, com el trietilalumini.[9]
Els organometàl·lics de titani, són catalitzadors importants en la polimerització d'hidrocarburs insaturats, com l'etilè i el propilè. El mecanisme d'acció dels catalitzadors d'alquiltitanialumini probablement implica la interacció entre els àtoms de titani i els dobles enllaços dels hidrocarburs.[9]
Els compostos organometàl·lics que contenen plom, estany i mercuri són importants des del punt de vista comercial. Un gran nombre de compostos d'organoestany, per exemple, s'utilitzen com a productes farmacèutics, pesticides, estabilitzadors per al clorur de polivinil i retardants de flama.[9]
El metilmercuri ha causat greus problemes de contaminació a conseqüència de la seva toxicitat. Aquest fet ha portat a controls estrictes sobre la descàrrega de mercuri des de plantes químiques a rius, llacs i oceans. També el tetraetilplom emprat per millorar la benzina, i ara prohibit per aquest ús, donant lloc a les conegudes benzines sense plom.[9]

El monòxid de carboni reacciona fàcilment amb molts àtoms de transició-metall per formar carbonils metàl·lics, ells mateixos una classe d'organometàl·lics. Els carbonils metàl·lics s'utilitzen com a catalitzadors en moltes reaccions en la indústria petroquímica. Un dels primers a ser descobert fou el tetracarbonil de níquel, un compost de níquel volàtil que es convertí en la base d'un procés de purificació del níquel.[9]

Referències[modifica]
- ↑ 1,0 1,1 1,2 1,3 History of Organometallic Chemistry (en anglès). Berlin, Heidelberg: Springer Berlin Heidelberg, 2007, p. 5–20. DOI 10.1007/978-3-540-46129-6_2. ISBN 978-3-540-46128-9.
- ↑ Seyferth, Dietmar «The Grignard Reagents». Organometallics, 28, 6, 23-03-2009, pàg. 1598–1605. DOI: 10.1021/om900088z. ISSN: 0276-7333.
- ↑ Kauffman, George B. «The discovery of ferrocene, the first sandwich compound» (en anglès). Journal of Chemical Education, 60, 3, 1983-03, pàg. 185. DOI: 10.1021/ed060p185. ISSN: 0021-9584.
- ↑ «The Nobel Prize in Chemistry 1963» (en anglès americà). [Consulta: 4 juliol 2021].
- ↑ «The Nobel Prize in Chemistry 1973» (en anglès americà). [Consulta: 4 juliol 2021].
- ↑ «The Nobel Prize in Chemistry 2001» (en anglès americà). [Consulta: 4 juliol 2021].
- ↑ «The Nobel Prize in Chemistry 2005» (en anglès americà). [Consulta: 4 juliol 2021].
- ↑ «The Nobel Prize in Chemistry 2010» (en anglès americà). [Consulta: 4 juliol 2021].
- ↑ 9,0 9,1 9,2 9,3 9,4 9,5 9,6 9,7 Shriver, D.F.. «Organometallic compound». A: Encyclopedia Britannica, 15 novembre 2018.



