Usuari:Enrospv/Tacrolimús
 | |
 | |
| Dades clíniques | |
|---|---|
| Noms comercials | Tacrolimus STADA (Espanya) Prograf, Advagraf, Protopic, altres (Internacional) |
| AHFS/Drugs.com | Monografia |
| MedlinePlus | a601117 |
| Dades de llicència | EMEA:enllaç, US Daily Med:enllaç |
| Risc per l'embaràs | |
| Via | Tòpica, oral, intravenosa (IV) |
| Codi ATC | D11AH01 L04 |
| Dades químiques i físiques | |
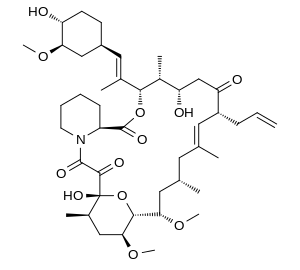
| Fórmula | C44H69NO12 |
| Massa molecular | 804.018 |
| Model 3D (Jmol) | Imatge interactiva |
O=C3C(=O)N1CCCC[C@H]1C(=O)O[C@H](C(=C/[C@@H]2CC[C@@H](O)[C@H](OC)C2)/C)[C@H](C)[C@@H](O)CC(=O)[C@@H](/C=C(/C[C@@H](C[C@H](OC)[C@H]4O[C@]3(O)[C@H](C)C[C@@H]4OC)C)C)C\C=C | |
InChI=1S/C44H69NO12/c1-10-13-31-19-25(2)18-26(3)20-37(54-8)40-38(55-9)22-28(5)44(52,57-40)41(49)42(50)45-17-12-11-14-32(45)43(51)56-39(29(6)34(47)24-35(31)48)27(4)21-30-15-16-33(46)36(23-30)53-7/h10,19,21,26,28-34,36-40,46-47,52H,1,11-18,20,22-24H2,2-9H3/b25-19+,27-21+/t26-,28+,29+,30-,31+,32-,33+,34-,36+,37-,38-,39+,40+,44+/m0/s1 Key:QJJXYPPXXYFBGM-LFZNUXCKSA-N | |
| Estat legal | |
| R. dispensació |
|
| Dades farmacocinètiques | |
| Biodisponibilitat | 24% (5–67%), menor després de menjars greixosos |
| Unió proteica | ≥98.8% |
| Metabolisme | Hepàtic CYP3A4, CYP3A5 |
| Vida mitjana | 11.3 h per a pacients de transplant (rang de 3.5–40.6 h) |
| Excreció | Majoritàriament fecal |
| Identificadors | |
(−)-(3S,4R,5S,8R,9E,12S,14S,15R,16S,18R,26aS)-8-allyl-5,6,8,11,12,13,14,15,16,17,18,19,24,25,26,26a-hexadecahydro-5,19-dihydroxy-3-{(E)-2-[(1R,3R,4R)-4-hydroxy-3-methylcyclohexyl]-1-methylvinyl}-14,16-dimethoxy-4,10,12,18-tetramethyl-15,19-epoxy-3H-pyrido[2,1-c][1,4]oxaazacyclotricosane-1,7,20,21(4H,23H)-tetrone
| |
| Sinònims | FK-506, fujimycin |
| Número CAS | 104987-11-3 |
| PubChem (CID) | 445643 |
| DrugBank | DB00864 |
| ChemSpider | 393220 |
| UNII | Y5L2157C4J |
| KEGG | D00107 C01375 |
| ChEBI | CHEBI:61049 |
| ChEMBL | CHEMBL269732 |
| PDB ligand ID | FK5 (PDBe, RCSB PDB) |
El tacrolimús (o tacrolimus), venut sota les marques Protopic, Prograf i altres internacionalment; i Tacrolimus STADA a l'estat espanyol, és un fàrmac immunosupressor. S'utilitza després d'un trasplantament al·loempeltat per a reduir el risc de rebuig d'òrgan, i també com a medicació tòpica en el tractament de malalties mediades per limfòcits T com èczemes i psoriasi. També es fa servir per a la uveïtis refractària severa després de trasplants de medul·la òssia, exacerbacions de la malaltia de canvis mínims, malaltia de Kimura, la condició de la pell coneguda com a vitiligo, i la síndrome de l'ull sec en gats i gossos.[2][3]
El tacrolimús inhibeix la calcineurina, involucrada en la producció d'interleucina-2, una molècula que provoca el desenvolupament i la proliferació de limfòcits T, part de la resposta immunitària apresa del cos (o adaptada)
Químicament, és una lactona macròlida[4] descoberta en 1987, de la fermentació d'un brou de terra japonesa que contenia el bacteri Streptomyces tsukubaensis.
Usos mèdics[modifica]
Trasplantaments[modifica]
Té propietats immunosupressores semblants a la ciclosporina, però és molt més potent. La immunosupressió amb tacrolimús s'associà en un estudi amb una taxa significativament baixa de refracció aguda comparada amb el tractament basat en ciclosporina (30.7% vs 46.4%).[5] Els resultats clínics són millors amb tacrolimús que amb ciclosporina durant el primer any de trasplant de fetge.[6][7] No obstant això, els resultats a llarg termini no van millorar al mateix nivell. El tacrolimús normalment es prescriu com a part de un còctel post-transplant que inclou esteroids, micofenolat i inhibidors dels receptors IL-2 com el basiliximab. Les dosis es controlen segons els nivells de sang.
Colitis ulcerosa[modifica]
Recentment, el tacrolimús s'ha fet servir per a eliminar la inflamació associada a la colitis ulcerosa, una forma de síndrome del colon irritable. Encara que s'utilitza gairebé únicament en estudis científics, el tacrolimús ha mostrat una eficàcia significativa en la supressió dels brots de la malaltia.[8][9]
Pell[modifica]

Com a ungüent, el tacrolimús es fa servir per a tractar l'èczema, en particular la dermatitis atòpica. Suprimeix la inflamació de forma similar als esteroides, i és igual d'efectiu com un esteroide de potència mitjana. Una gran benefici del tacrolimús és que no causa l'aprimament de la pell (atròfia), ni cap dels altres efectes secundaris relacionats.[10]
S'aplica en lesions actives fins que es curen, però també es pot fer servir contínuament en dosis baixes (cada dos setmanes), i aplicat a la pell més fina de la cara i les parpelles. S'han dut estudis clínics fins a un any de duració. Recentment també s'ha fet servir per a tractar el vitiligo segmental en xiquets, especialment en àrees de la cara.[11]
Lupus nefritis[modifica]
El tacrolimús ha mostrat una reducció del risc en infecció seriosa i també augmentar la remissió renal en lupus nefritis.[12][13]
Contraindicacions i precaucions[modifica]
Les contraindicacions i precaucions inclouen:[14]
- Lactància
- Malaltia hepàtica
- Immunosupressió
- Infants
- Infecció
- Malalties neoplàsiques, com:
- Oligúria
- Embaràs
- Prolongació de l'interval QT
- Exposició a la llum solar (raigs UV)
- Suc d'aranger[15]
Ús tòpic[modifica]
- Apòsit oclusiu
- Lesions malignes conegudes o sospitoses
- Síndrome de Netherton o malalties similars de la pell
- Algunes infeccions de la pell[10]
Efectes secundaris[modifica]
Per via oral o intravenosa[modifica]
Els efectes secundaris poden ser severs i inclouen infecció, dany cardíac, hipertensió, visió borrosa, problemes de ronyó i fetge (nefrotoxicitat),[16] hiperkalèmia, hipomagnesèmia, hiperglucèmia, diabetis mellitus, coïssor, dany als pulmons (com el sirolimús),[17] i altres problemes neuropsiquiàtrics com a pèrdua d'apetit, insomni, síndrome d'encefalopatia posterior reversible, confusió, feblesa, depressió, malsons vívids, rampes, neuropatia, atacs epilèptics, tremolors, i catatonia.[18]
A més a més, pot agreujar potencialment la severitat d'infeccions bacterians o fungals així com infeccions virals per l'herpes zòster o polyomavirus.[14]
Carcinogènesi i mutagènesi[modifica]
En persones que reben immunosupressors per a reduir el rebuig de l'empelt del trasplant, hi ha un risc de malignitat (càncer) reconegut com a possible complicació.[14] Els càncers més comuns són limfomes no hodgkinians[19] i càncers de pell. Aquest risc sembla estar relacionat amb la intensitat i la duració del tractament.
Ús tòpic[modifica]
Els efectes adversos més comuns associats a l'ús de tacrolimús tòpic, especialment en una àrea ampla, inclouen una sensació de cremor o coïssor en les aplicacions inicials, amb una sensibilitat pujada en l'àrea afectada. Més poc comuns són símptomes gripals, mal de cap, esternuts, i cremor als ulls.[20]
Riscs de càncer[modifica]
El tacrolimús i un medicament relacionat per als èczemes (pimecrolimus) són sospitosos de tindre un risc carcnigènic, encara que encara existeix controvèrsia en la matèria. La FDA va emetre una alerta en març de 2005 per al medicament, basant-se en models animals i un xicotet grup de pacients. Fins que més estudis humans ens donen resultats més conclusius, la FDA recomana que els usuaris estiguen avisats del riscs potencials. No obstant això, la pràctica actual en els dermatòlegs del Regne Unit no ho considera un problema significant i s'està recomanant progressivament més l'ús d'aquests medicaments.[21]
Interaccions[modifica]
Així com la ciclosporina, té un rang molt ample d'interaccions. El tacrolimús es metabolitza principalment pel sistema d'enzims citocrom P450 del fetge, i hi ha moltes substàncies que interactuen amb aquest sistema i indueixen o inhibeixen l'activitat metabòlica del sistema.[14]
Les interaccions inclouen el suc d'aranger que augmenta les concentracions en plasma de tacrolimús. Com que les infeccions són una causa major de morbiditat i mortalitat en el pacient post-trasplant les interaccions més normalment reportades, inclouen les que ocorren amb medicament antimicròbics. Antibiòtics macròlids incloent eritromicina i claritromicina, així com diversos medicaments dels meus nous d'antifungals, especialment dels azols (fluconazol, voriconazol) augmenten el nivell de tacrolimús competint per enzims citocroms.[14]
Farmacologia[modifica]
Mecanisme d'acció[modifica]
El tacrolimús és un inhibidor de la calcineurina macròlid. En limfòcits T, l'activació dels receptors normalment puja el calci intracel·lular, que actua via la calmodulina per a activar la calcineurina. La calcineurina desfosforileix el factor de transcripció del factor nuclear de limfòcits T activats (NF-AT), que mou al nucli dels limfòcits T i augmenta l'activitat de la codificació dels gens per a la IL-2 i citocines relacionades. El tacrolimús prevené la desfosforilització del NF-AT.[22]
De forma més detallada, el tacrolimús redueix l'activitat de la ciclofilina A lligant-se a la immunofilina FKBP12 (proteïna de lligam de la FK506), creant un nou complex. Aquest complex FKBP12-FK506 interactua amb i inhibeix la calcineurina, inhibint tant el senyal de transducció dels limfòcits T i la transcripció de la IL-2.[23] Tot i que aquesta activitat és semblant a la de la ciclosporina, la incidència de rebuig agut es redueix quan s'usa el tacrolimús i no la ciclosporina.[5] Encara que la immunosupressió a curt termini per a la supervivència del pacient i l'empelt és similar entre els dos medicaments, el tacrolimús té un perfil de lípids més favorable, i açò`pot tindre implicacions importants a llarg termini segons la influència pronòstica de la supervivència del trasplant.[24]
Farmacodinàmica[modifica]
El tacrolimús oral s'absorbeix lentament en el tracte gastrointestinal, amb una biodisponibilitat de un 20 a 25% (amb variacions d'un 5 a 67%) i aconsegueix la concentració màxima en plasma sanguini (Cmax) d'una a tres hores. Prenent el medicament junt amb menjars, especialment rics en greixos, enlenteix l'absorció i redueix la biodisponibilitat. En la sang, el tacrolimús es lliga principalment als eritròcits, els quals només un 5% es troben en el plasma sanguini, dels quals més d'un 98,8% es lliguen a les proteïnes sanguínies.[14][25]
La substància es metabolitza en el fetge, principalment a través de la CYP3A, i en el mur intestinal. Tots els metabòlits trobats en la circulació són inactius. La semivida varia àmpliament i pareix ser més alta en persones sanes (43 hores de mitjana) que en pacients amb trasplants de fetge (12 hores) o de ronyó (16 hores), per diferències en la depuració. El tacrolimús s'elimina de forma predominant per les deposicions en forma dels seus metabòlits.[14][25]
Quan s'aplica localment a un èczema, el tacrolimús té una biodisponibilitat mínima o nul·la.[14]
Farmacogenètica[modifica]
L'enzim predominant responsable per al metabolisme del tacrolimús és CYP3A5. Variacions genètiques en CYP3A5 resulten en canvis en l'activitat de la proteïna i poden afectar a les concentracions de tacrolimús en el cos. Particularment, individus que són homozigòtics per a l'al·lel G en el polimorfisme de nucleòtids simples (SNP) rs776746 (també conegut com a CYP3A5 *3/*3) tenen una proteïna CYP3A5 no funcional. La freqüència de l'al·lel G varia arreu del món, del 4% en algunes poblacions africanes al 80-90% en la població blanca.[26] A través d'un gran nombre d'estudis, individus homozigòtics per a l'al·lel G han mostrat tindre majors concentracions de tacrolimús i requereixen dosis inferiors del medicament, comparat amb els indivus que no ho són. És important aconseguir la concentració òptima de tacrolimús: si els nivells són massa baixos, hi ha un risc de rebuig de trasplant, si els nivells són massa alts, hi ha un risc de toxicitat pel medicament. Hi ha proves que suggereixen que donar dosis als pacients segons el genotip rs776746 pot resultar en l'aconseguiment més ràpid i freqüent de nivells de tacrolimús òptims. No obstant això, falten evidències consistents si les dosis basades en el genotip rs776746 resulten en millors resultats clínics (com un descens en el risc de rebuig de trasplant o toxicitat pel medicament).[27][28][29][30]
Alguns estudis també mostren que polimorfismes genètics en gens diferents al CYP3A5, com el NR1I2[31][32] (codificador del PXR), també influeix la farmacodinàmica del tacrolimús.
Història[modifica]
El tacrolimús es va descobrir en 1987;[33] va se run dels primers immunosupressors macròlids descoberts, precedit pel descobriment de la rapamicina (sirolimus) en Rapa Nui (Illa de Pasqua) l'any 1975.[34] És produït per un bacteri trobat en terra, Streptomyces tsukubaensis.[35] El nom tacrolimús és derivat de "Tsukuba macrolide immunosupressant" (Immunosupressor macròlid de Tsukuba, en anglés)[36]
El tacrolimús es va aprovar per la FDA americana en 1994,[37][38] per a l'ús en trasplant de fetge; les indicacions es van estendre per a incloure ronyó, cor, intestí prim, pàncrees, pulmó, tràquea, pell, còrnia, medul·la òssia i extremitats. Versions genèriques del tacrolimús es va aprovar en els EUA l'any 2017.[39]
El tacrolimús es va aprovar per a ús medicinal en la Unió Europea en 2002, per al tractament de la dermatitis atòpica moderada o severa.[40] En 2007, les indicacions s'expandiren per a incloure la profilaxi de rebuig de trasplant en els rebedors adults de ronyó o fetge i el tractament de rebuig resistent al tractament amb altres immunosupressors en adults.[41] En 2009, les indicacions es van estendre per a incloure la profilaxi de rebuig de trasplant en adults i xiquets per a ronyó, fetge, pulmó o cor i el tractament de rebuig resistent al tractament amb altres agents immunosupressors en adults i xiquets.[42]
Formes disponibles[modifica]
La versió comercial del medicament és propietat de Astellas Pharma, i es ven amb la marca Prograf, amb una administració de dos al dia. Altres fabricants tenen autorització per a produir marques alternatives de la formulació per a dos dosis diàries.[43]
La dosi única al dia autoritzada inclou Advagraf (Astellas Pharma) i Envarsus (comercialitzat com Envarsus XR per Veloxis Pharmaceuticals i comercialitzada en Europa per Chiesi).[43] Aquestes formulacions volen reduir la variació farmacodinàmica en els nivells en sang i facilitar el seguiment de les dosis.
La formulació tòpica es comercialitza per LEO Pharma sota el nom Protopic.[43]
Biosíntesi[modifica]
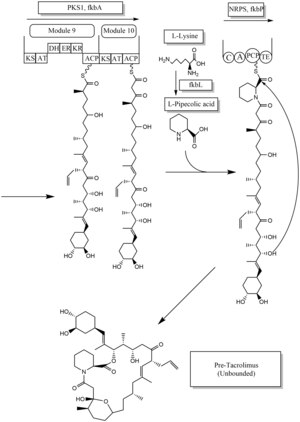
La biosíntesi del tacrolimús és síntesis híbrida de policètid sintases de tipus 1]] (PKS 1) i sintases de pèptid no ribosòmmic (NRPS). Investigacions mostren que aquesta síntesi híbrida consisteix de deu mòduls de sintetases policètides i un mòdul de sintetasa de pèptid no ribosòmic. Els enzims sintètics per al tacrolimús es troben en 19 clústers de gens anomenats fkb. Aquests genes són fkbQ, fkbN, fkbM, fkbD, fkbA, fkbP, fkbO, fkbB, fkbC, fkbL, fkbK, fkbJ, fkbI, fkbH, fkbG, allD, allR, allK i allA.[44]
Hi ha diverses formes possibles de la biosíntesi del tacrolimús. Les unitats fonamentals per la biosíntesi són aquestes: una mol·lècula d'àcid 4,5-dihydroxycyclohex-1-enecarboxylic (DHCHC) com a unitat inicial, quatre molècules de malonyl-CoA, cinc molècules de methylmalonyl-CoA, una molècula d'allylmalonyl-CoA com a unitats d'allargament. Tot i això, dos molècules de malonyl-CoA són capaços de substituir dos molècules de methoxymalonyl CoA. Una vegada que dos mol·lècules de malonyl-CoA són substituïdes, els pasos d'unió post-sintetasa no són necessaris quan dos mol·lècules de methoxymalonyl CoA són substituïdes. La biosíntesi del methoxymalonyl CoA a proteïnes portadores de Acyl és precedida de cinc enzims (fkbG, fkbH, fkbI, fkbJ, and fkbK). L'allylmalonyl-CoA també és capaç de ser substituït pel propionylmalonyl-CoA.[44]
La unitat inicial, el DHCHC de l'àcid corísmic es forma per l'enzim fkbO i és carregat en el domini de la ligasa-CoA (CoL). Després, procedeix a reducció depenent de la NADPH (ER). Tres enzimes, fkbA, B i C forcen processos de la cèl·lula de càrrega al mòdul 10, l'últim pas de PKS 1. L'enzim fkbB és responsable de la síntesi d'allylmalonyl-CoA o possiblement de propionylmalonyl-CoA en C21, que és un pas inusual del PKS 1 general. Com s'ha dit, si dos molècules de methoxymalonyl CoA se substitueixen per dos molècules malonyl-CoA, es trobaran en el mòdul 7 i 8 (C13 i C15), i l'enzim fkbA forçarà aquest procés. Després de l'últim pas (mòdul 10) de PKS 1, una molècula de L-àcid pipecòlic format per L-lisina i catalitzat per l'enzim fkbL se sintetitza en la molècula del mòdul 10. El procés de síntesi del L-àcid pipecòlic és NRPS-forçat per l'enzim fkbP. Després de sintetitzar les subunitats completes, la molècula és ciclitzada. Després de la ciclització, la pre-molècula de tacrolimús passa pel lligat post-sintetasa com l'oxidació i S-Adenosil metionina. Particularment, l'enzim fkbM és responsable de la metilació de l'alcohol atacant l'alcohol de l'iniciador DHCHC (Número de carbó 31 mostrat en marró), i l'enzim fkbD és responsable del C9 (mostrat en verd). Després d'aquests passos de lligam, la molècula de tacrolimús esdevé biològicament activa.[44][45][46]
Vegeu també[modifica]
- Tohru Kino
- Stuart Schreiber
- Thomas Starzl
- FK1012, un derivat.
- Ciclosporina
Referències[modifica]
- ↑ 1,0 1,1 «Tacrolimus Use During Pregnancy». Drugs.com, 03-10-2019. [Consulta: 29 abril 2020].
- ↑ «Effect of topical 0.02% tacrolimus aqueous suspension on tear production in dogs with keratoconjunctivitis sicca». Veterinary Ophthalmology, vol. 8, 4, 2005, pàg. 225–32. DOI: 10.1111/j.1463-5224.2005.00390.x. PMID: 16008701.
- ↑ «Tacrolimus for Dogs and Cats».
- ↑ «Tacrolimus ointment in the management of atopic dermatitis». Clin Cosmet Investig Dermatol, vol. 2, January 2009, pàg. 1–7. DOI: 10.2147/ccid.s3378. PMC: 3047924. PMID: 21436963.
- ↑ 5,0 5,1 McCauley, Jerry. «Long-Term Graft Survival In Kidney Transplant Recipients». Slide Set Series on Analyses of Immunosuppressive Therapies. Medscape, 19-05-2004. [Consulta: 6 juny 2006].
- ↑ «Cyclosporin versus tacrolimus for liver transplanted patients». The Cochrane Database of Systematic Reviews, vol. 4, 4, October 2006, pàg. CD005161. DOI: 10.1002/14651858.CD005161.pub2. PMID: 17054241.
- ↑ «Tacrolimus versus microemulsified ciclosporin in liver transplantation: the TMC randomised controlled trial». Lancet, vol. 360, 9340, October 2002, pàg. 1119–25. DOI: 10.1016/S0140-6736(02)11196-2. PMID: 12387959.
- ↑ «Tacrolimus is safe and effective in patients with severe steroid-refractory or steroid-dependent inflammatory bowel disease--a long-term follow-up». The American Journal of Gastroenterology, vol. 101, 5, May 2006, pàg. 1048–56. PMID: 16573777.
- ↑ «Tacrolimus (FK506) for induction of remission in refractory ulcerative colitis». The Cochrane Database of Systematic Reviews, vol. 16, 3, July 2008, pàg. CD007216. DOI: 10.1002/14651858.CD007216. PMID: 18646177.
- ↑ 10,0 10,1 Haberfeld, H. Austria-Codex (en german). Vienna: Österreichischer Apothekerverlag, 2015.
- ↑ «Tacrolimus ointment promotes repigmentation of vitiligo in children: a review of 57 cases». Journal of the American Academy of Dermatology, vol. 51, 5, November 2004, pàg. 760–6. DOI: 10.1016/j.jaad.2004.05.036. PMID: 15523355.
- ↑ «Risk of serious infections with immunosuppressive drugs and glucocorticoids for lupus nephritis: a systematic review and network meta-analysis». BMC Medicine, vol. 14, 1, September 2016, pàg. 137. DOI: 10.1186/s12916-016-0673-8. PMC: 5022202. PMID: 27623861.
- ↑ Singh, Jasvinder A.; Hossain, Alomgir; Kotb, Ahmed; Wells, George A. «Comparative effectiveness of immunosuppressive drugs and corticosteroids for lupus nephritis: a systematic review and network meta-analysis» (en anglès). Systematic Reviews, vol. 5, 1, 2016, pàg. 155. DOI: 10.1186/s13643-016-0328-z. ISSN: 2046-4053. PMC: 5020478. PMID: 27619512.
- ↑ 14,0 14,1 14,2 14,3 14,4 14,5 14,6 14,7 Haberfeld, H. Austria-Codex (en german). Vienna: Österreichischer Apothekerverlag, 2015.
- ↑ «Delayed effect of grapefruit juice on pharmacokinetics and pharmacodynamics of tacrolimus in a living-donor liver transplant recipient». Drug Metabolism and Pharmacokinetics, vol. 21, 2, April 2006, pàg. 122–5. DOI: 10.2133/dmpk.21.122. PMID: 16702731.
- ↑ «Calcineurin inhibitor nephrotoxicity». Clinical Journal of the American Society of Nephrology, vol. 4, 2, February 2009, pàg. 481–508. DOI: 10.2215/CJN.04800908. PMID: 19218475.
- ↑ «Tacrolimus-induced lung injury in a rheumatoid arthritis patient with interstitial pneumonitis». Modern Rheumatology, vol. 18, 2, 2008, pàg. 208–11. DOI: 10.1007/s10165-008-0034-3. PMID: 18306979.
- ↑ «Catatonic mutism after liver transplant rapidly reversed with lorazepam». General Hospital Psychiatry, vol. 29, 3, 2007, pàg. 280–1. DOI: 10.1016/j.genhosppsych.2007.01.004. PMID: 17484951.
- ↑ «Key Statistics for Non-Hodgkin Lymphoma» (en anglès). www.cancer.org. [Consulta: 19 febrer 2020].
- ↑ «Efficacy and safety of tacrolimus ointment treatment for up to 4 years in patients with atopic dermatitis». Journal of the American Academy of Dermatology, vol. 53, 2 Suppl 2, August 2005, pàg. S186–94. DOI: 10.1016/j.jaad.2005.04.062. PMID: 16021174.
- ↑ «Advice to dermatologists re topical tacrolimus». Therapy Guidelines Committee. British Association of Dermatologists, December 2002. Arxivat de l'original el 2013-12-13.
- ↑ William F. Ganong. Review of medical physiology. 22nd. Lange medical books, 2005-03-08, p. 530. ISBN 978-0-07-144040-0.
- ↑ «Calcineurin is a common target of cyclophilin-cyclosporin A and FKBP-FK506 complexes». Cell, vol. 66, 4, August 1991, pàg. 807–15. DOI: 10.1016/0092-8674(91)90124-H. PMID: 1715244.
- ↑ «Tacrolimus (FK506) versus cyclosporine microemulsion (neoral) as maintenance immunosuppression therapy in kidney transplant recipients». Transplantation Proceedings, vol. 37, 7, September 2005, pàg. 3025–8. DOI: 10.1016/j.transproceed.2005.08.040. PMID: 16213293.
- ↑ 25,0 25,1 Arzneistoff-Profile (en german). 9. 18. Eschborn, Germany: Govi Pharmazeutischer Verlag, 2003. ISBN 978-3-7741-9846-3.
- ↑ Bains, Ripudaman Kaur. «Molecular diversity and population structure at the CYP3A5 gene in Africa». University College London. [Consulta: 13 juny 2016].
- ↑ «Clinical pharmacokinetics and pharmacodynamics of tacrolimus in solid organ transplantation». Clinical Pharmacokinetics, vol. 43, 10, 2004, pàg. 623–53. DOI: 10.2165/00003088-200443100-00001. PMID: 15244495.
- ↑ «Effect of CYP3A and ABCB1 single nucleotide polymorphisms on the pharmacokinetics and pharmacodynamics of calcineurin inhibitors: Part I». Clinical Pharmacokinetics, vol. 49, 3, March 2010, pàg. 141–75. DOI: 10.2165/11317350-000000000-00000. PMID: 20170205.
- ↑ «Effect of CYP3A and ABCB1 single nucleotide polymorphisms on the pharmacokinetics and pharmacodynamics of calcineurin inhibitors: Part II». Clinical Pharmacokinetics, vol. 49, 4, April 2010, pàg. 207–21. DOI: 10.2165/11317550-000000000-00000. PMID: 20214406.
- ↑ «PharmGKB summary: cyclosporine and tacrolimus pathways». Pharmacogenetics and Genomics, vol. 23, 10, October 2013, pàg. 563–85. DOI: 10.1097/fpc.0b013e328364db84. PMC: 4119065. PMID: 23922006.
- ↑ «Tacrolimus population pharmacokinetic-pharmacogenetic analysis and Bayesian estimation in renal transplant recipients». Clinical Pharmacokinetics, vol. 48, 12, 01-01-2009, pàg. 805–16. DOI: 10.2165/11318080-000000000-00000. PMID: 19902988.
- ↑ «A pharmacogenomic study on the pharmacokinetics of tacrolimus in healthy subjects using the DMETTM Plus platform». The Pharmacogenomics Journal, vol. 17, 1, January 2017, pàg. 105–106. DOI: 10.1038/tpj.2016.85. PMID: 27958377.
- ↑ «FR-900520 and FR-900523, novel immunosuppressants isolated from a Streptomyces. I. Taxonomy of the producing strain». The Journal of Antibiotics, vol. 41, 11, November 1988, pàg. 1586–91. DOI: 10.7164/antibiotics.41.1586. PMID: 3198493.
- ↑ «FK-506, a novel immunosuppressant isolated from a Streptomyces. I. Fermentation, isolation, and physico-chemical and biological characteristics». The Journal of Antibiotics, vol. 40, 9, September 1987, pàg. 1249–55. DOI: 10.7164/antibiotics.40.1249. PMID: 2445721.
- ↑ «Sourcing a chemical succession for cyclosporin from parasites and human pathogens». Drug Discovery Today, vol. 10, 10, May 2005, pàg. 688–91. DOI: 10.1016/S1359-6446(05)03395-7. PMID: 15896681. Supports source organism, but not team information
- ↑ Ponner, B, Cvach, B (Fujisawa Pharmaceutical Co.): Protopic Update 2005
- ↑ «Prograf: FDA-Approved Drugs». U.S. Food and Drug Administration (FDA). [Consulta: 29 abril 2020].
- ↑ «Prograf: FDA-Approved Drugs». U.S. Food and Drug Administration (FDA). [Consulta: 29 abril 2020].
- ↑ «Tacrolimus: FDA-Approved Drugs». U.S. Food and Drug Administration (FDA). [Consulta: 29 abril 2020].
- ↑ «Protopic EPAR». European Medicines Agency (EMA). [Consulta: 29 abril 2020].
 Aquest article incorpora text d'aquesta font, la qual és de domini públic.
Aquest article incorpora text d'aquesta font, la qual és de domini públic.
- ↑ «Advagraf EPAR». European Medicines Agency (EMA). [Consulta: 29 abril 2020].
 Aquest article incorpora text d'aquesta font, la qual és de domini públic.
Aquest article incorpora text d'aquesta font, la qual és de domini públic.
- ↑ «Modigraf EPAR». European Medicines Agency (EMA). [Consulta: 29 abril 2020].
- ↑ 43,0 43,1 43,2 Joint Formulary Committee. «British National Formulary (online)». London: BMJ Group and Pharmaceutical Press. [Consulta: 24 setembre 2015].
- ↑ 44,0 44,1 44,2 «omic Approaches». Antibiotics, vol. 7, 2, May 2018, pàg. 39. DOI: 10.3390/antibiotics7020039. PMC: 6022917. PMID: 29724001.
- ↑ «FK506 maturation involves a cytochrome p450 protein-catalyzed four-electron C-9 oxidation in parallel with a C-31 O-methylation». Journal of Bacteriology, vol. 195, 9, May 2013, pàg. 1931–9. DOI: 10.1128/JB.00033-13. PMC: 3624582. PMID: 23435975.
- ↑ «Enhanced FK506 production in Streptomyces clavuligerus CKD1119 by engineering the supply of methylmalonyl-CoA precursor». Journal of Industrial Microbiology & Biotechnology, vol. 36, 12, December 2009, pàg. 1473–82. DOI: 10.1007/s10295-009-0635-7. PMID: 19756799.
Lectura addicional[modifica]
- «Comparative efficacy of 20 graft-versus-host disease prophylaxis therapies for patients after hematopoietic stem-cell transplantation: A multiple-treatments network meta-analysis». Crit. Rev. Oncol. Hematol., vol. 150, March 2020, pàg. 102944. DOI: 10.1016/j.critrevonc.2020.102944. PMID: 32247246.
Enllaços externs[modifica]
- «Tacrolimus». Drug Information Portal. U.S. National Library of Medicine.
- «Tacrolimus Injection». MedlinePlus.
- «Tacrolimus Topical». MedlinePlus.