Estearat de magnesi
| Substància química | tipus d'entitat química |
|---|---|
| Massa molecular | 590,512 Da |
| Rol | metabòlit primari i excipient |
| Estructura química | |
| Fórmula química | C₃₆H₇₀MgO₄ |
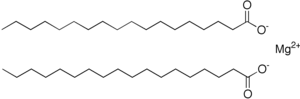 | |
| SMILES canònic | |
| Identificador InChI | Model 3D |
| NFPA 704: Standard System for the Identification of the Hazards of Materials for Emergency Response () | |
L'Estearat de magnesi és el compost químic amb la fórmula Mg(C
18H
35O
2)
2. És un sabó, format per sal que conté dos equivalents d'estearat (l’anió de l’àcid esteàric) i un catió de magnesi (Mg2 +). L'estearat de magnesi és una pols blanca i insoluble en aigua. Les seves aplicacions aprofiten la seva suavitat, insolubilitat en molts dissolvents i baixa toxicitat. S'utilitza com a agent desprenent i com a component o lubricant en la producció de productes farmacèutics i cosmètics.[1]
Producció
[modifica]L'estearat de magnesi es produeix per reacció de l'estearat de sodi amb sals de magnesi o mitjançant el tractament de l’òxid de magnesi amb àcid esteàric.[1] Alguns suplements nutricionals especifiquen que l'estearat de sodi utilitzat en la fabricació de l'estearat de magnesi es produeix a partir d'àcid esteàric d'origen vegetal.[2]
Usos
[modifica]L'estearat de magnesi s’utilitza sovint com a antiadherent[3] en la fabricació de comprimits, càpsules i pols mèdiques.[4] En aquest sentit, la substància també és útil perquè té propietats lubricants, evitant que els ingredients s’adhereixin als equips de fabricació durant la compressió de pols químics en pastilles sòlides; l'estearat de magnesi és el lubricant més utilitzat per a les pastilles.[5] No obstant això, pot causar una menor humectabilitat i una desintegració més lenta de les pastilles i una dissolució més lenta i fins i tot solubilitat del medicament.
L'estearat de magnesi també es pot utilitzar de manera eficient en processos de recobriment en sec.[6][7][8]
En la creació de caramels premsats, l'estearat de magnesi actua com a agent desprenent i s'utilitza per unir el sucre a caramels durs com els "mints".[9]
L'estearat de magnesi és un ingredient comú en les fórmules per a nadons.[10]
Curiositat
[modifica]L'estearat de magnesi és un component important dels cèrcols de brutícia que s'enganxen a la paret de la banyera. Quan són produïts per aigua i sabó, l'estearat de magnesi i l'estearat de calci formen un sòlid blanc insoluble en aigua i es coneixen col·lectivament com a escuma de sabó. En el cas dels cèrcols en aparells sanitaris, la sal esteàrica ha absorbit restes orgàniques provinents de la pell. La duresa de l'aigua en facilita la precipitació.[11]
Seguretat
[modifica]L'estearat de magnesi es considera generalment segur per al consum humà a nivells inferiors a 2.500 mg / kg al dia[12] i es classifica als Estats Units com a generalment reconegut com a segur (GRAS). El 1979, el subcomitè de la FDA sobre substàncies GRAS (SCOGS) va informar: "No hi ha proves a la informació disponible sobre ... estearat de magnesi ... que demostri, o suggereixi motius raonables per sospitar un perill per al públic quan és usat en nivells actuals i de la manera que es practica ara, o que es podria esperar raonablement en el futur."[13]
Referències
[modifica]- ↑ 1,0 1,1 Angelo Nora, Alfred Szczepanek, Gunther Koenen, "Metallic Soaps" in Ullmann's Encyclopedia of Industrial Chemistry 2005 Wiley-VCH, Weinheim. doi:10.1002/14356007.a16_361
- ↑ «Quick search results of the DSLD». National Institutes of Health. Arxivat de l'original el 29 d’octubre 2018.
- ↑ Ritter, Steve «What's That Stuff? Excipients: Inactive ingredients in medicines serve multiple functions in drug delivery». Chemical & Engineering News, 86, 1, 2008, pàg. 25. DOI: 10.1021/cen-v086n001.p025.
- ↑ Sworbrick, James; Boylan, James C. Encyclopedia of pharmaceutical technology, 1990, p. 2274. ISBN 9780824728243.
- ↑ Weiner, Myra L.; Kotkoskie, Lois A. Excipient Toxicity and Safety, 1999, p. 10. ISBN 9780824782108.
- ↑ Ouabbas Y, Dodds J., Galet L., Chamayou A., Baron M. «Particle-particle coating in a cyclomix impact mixer». Powder Technol., 189, 2, 2009, pàg. 245–252. DOI: 10.1016/j.powtec.2008.04.031.
- ↑ Thomas G., Ouabbas Y., Grosseau P., Baron M., Chamayou A., Galet L. «Modeling the main interaction forces between powder particles. Application to silica gel-magnesium stearate mixtures». Applied Surface Science, 255, 17, 2009, pàg. 7500–7507. Bibcode: 2009ApSS..255.7500T. DOI: 10.1016/j.apsusc.2009.03.099.
- ↑ Sato A., Serris E., Grosseau P., Thomas G., Galet L., Chamayou A., Baron M. «Experiment and simulation of dry particle coating». Chem. Eng. Science, 86, 2013, pàg. 164–172. DOI: 10.1016/j.ces.2012.07.037.
- ↑ https://www.ctahr.hawaii.edu/oc/freepubs/pdf/FST-9.pdf
- ↑ Erich Lück and Gert-Wolfhard von Rymon Lipinski. «Foods, 3. Food Additives». A: Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH, 2002. DOI 10.1002/14356007.a11_561. ISBN 978-3527306732.
- ↑ Solos, Heather. «Cleaning The Bathtub» (en anglès). Home EC-101, 30-11-2009. [Consulta: 28 gener 2021].
- ↑ Søndergaarda, D.; Meyera, O.; Würtzena, G. «Magnesium stearate given peroprally to rats. A short term study». Toxicology, 17, 1, 1980, pàg. 51–55. DOI: 10.1016/0300-483X(80)90026-8. PMID: 7434368.
- ↑ FDA's SCOGS Database; Report No. 60; ID Code: 557-04-0; Year: 1979
