Viquipèdia:Llibre d'estil/Composts químics
La nomenclatura química canvia cada cert temps per adaptar-la als nous coneixements i aquests canvis, introduïts per la Unió Internacional de Química Pura i Aplicada, IUPAC, s'han de tenir en compte alhora de titular els articles i anomenar substàncies químiques dintre d'un article, evitant emprar noms que han esdevingut incorrectes amb el pas dels anys, i que transmeten als lectors una manca d'actualització dels continguts. És el cas dels noms anhídrid carbònic, clorur sòdic, sulfat ferrós o triòxid de diclor que ara no són acceptats i s'anomenen, respectivament, diòxid de carboni, clorur de sodi, sulfat de ferro(II) o diclorur de trioxigen.
Composts inorgànics[modifica]
En quan als compostos inorgànics la IUPAC, a les recomanacions més modernes de l'any 2005, ofereix vàries maneres d'anomenar-los que, malgrat sigui correcte emprar-les, en una mateixa obra cal no mesclar-les per evitar confusions. D’acord amb aquestes normes de nomenclatura sistemàtica les substàncies inorgàniques poden ser anomenades mitjançant tres sistemes:
- Nomenclatura de composició o estequiomètrica. La proporció de cada element es pot expressar de tres formes diferents:
- Mitjançant prefixos multiplicadors
- Mitjançant nombres d'oxidació (sistema de Stock)
- Mitjançant nombres de càrrega (sistema d'Ewens-Bassett)
- Nomenclatura de substitució
- Nomenclatura d’addició
La IUPAC està elaborant actualment un document on hi haurà un conjunt de regles per triar entre les diferents possibilitats en situacions en què és important decidir sobre un nom únic, serà el nom IUPAC preferit o PIN. Està dissenyant-se per ser utilitzat en situacions legals i reglamentàries. Fins que no es publiqui aquest document a la Viquipèdia es recomana emprar la nomenclatura de composició mitjançant prefixos multiplicadors i nombres d'oxidació, segons els tipus de substàncies, i la nomenclatura tradicional quan també sigui acceptada per la IUPAC. Queden desaconsellades la nomenclatura de substitució i la d'addició, així com la de composició mitjançant nombres de càrrega, excepte aquesta pel cas dels ions. Tanmateix es aconsellable indicar a la infotaula els altres noms acceptats per la IUPAC.
En base a aquestes consideracions, també emprades a la Viquipèdia en anglès, es recullen a continuació una sèrie de recomanacions pels editors de la Viquipèdia per tal d'assolir els objectius citats.
Nomenclatura dels elements[modifica]
Els elements químics s'anomenen, de manera general, amb el nom de l’element químic corresponent. En el cas dels no metalls que formen substàncies moleculars el seu nom es basa en el nombre d’àtoms que tengui la molècula i s’indica amb el corresponent prefix multiplicador. El prefix mono- s’utilitza només per als casos en els que l’element no es troba a la naturalesa en estat monoatòmic. Exemples:
| Fórmula | Nom IUPAC recomanat a la Viquipèdia | Nom IUPAC no recomanat a la Viquipèdia | Nom no acceptat per la IUPAC |
|---|---|---|---|
| H₂ | dihidrogen | hidrogen | |
| N | mononitrogen | ||
| N₂ | dinitrogen | nitrogen | |
| O₂ | oxigen | dioxigen | |
| O3 | ozó | trioxigen | |
| P4 | tetrafòsfor | fòsfor blanc | |
| S8 | octasofre | ||
| Ag | argent; plata | ||
| As | arseni; arsènic | ||
| W | tungstè; wolframi |
Nomenclatura dels ions simples[modifica]
Els cations monoatòmics s’anomenen amb el nombre de càrrega entre parèntesi. Per als homonuclears, formats per més d’un àtom del mateix element, s’afegeix el corresponent prefix multiplicador (di-, tri-, tetra-, penta-, hexa-,...). No es deixa cap espai entre el nom de l’element i el nombre de càrrega.
Pel que fa als anions s’anomenen afegint el sufix –ur. Per als homonuclears, formats per més d’un àtom del mateix element, s’afegeix el corresponent prefix multiplicador (di-, tri-, tetra-, penta-, hexa-,...). A continuació es pot posar el nombre de càrrega entre parèntesi si pot donar lloc a ambigüitat. En el cas de l’oxigen no s’utilitza el sufix –ur i s’anomena com òxid.
|
|
Nomenclatura dels composts binaris[modifica]
Composts metall-no metall[modifica]

En el composts binaris entre un metall i un no metall es recomana emprar la nomenclatura de composició, sistema de Stock. La IUPAC ha establit un ordre d'elements per a facilitar la nomenclatura de la següent manera:
- A cada columna de la taula periòdica l'element més electronegatiu és el situat més amunt i l'electronegativitat disminueix en baixar dins la columna.
- L'element que segueix al situat a la part més baixa d'una columna és el situat a damunt de la columna immediatament a l'esquerra.
- L'element més electronegatiu és el fluor. L'hidrogen se situa entre el poloni i el nitrogen. Els gasos nobles (grup 18) se situen a l'esquerra del grup dels alcalins (grup 1).
Aquest ordre també afecta l'ordre dels símbols a les fórmules. Així ClO o I₂O5 són incorrectes i s'han d'escriure: OCl i O5I₂.
Per anomenar un compost se segueixen les següents regles:
- L'element més electronegatiu s'ha d'escriure primer amb el nom de l'anió (fluorur, clorur, hidrur, òxid, dibismutur…).
- A continuació s'ha d'escriure la preposició de.
- Finalment s'ha d'escriure el nom de l'element més electropositiu amb el seu nombre d'oxidació en números romans dintre d'un parèntesi i sense que quedi cap espai entre el nom i el parèntesi, malgrat contradigui l'ús habitual dels parèntesis en català. En el cas de que un element només tengui un estat d'oxidació no s'ha d'escriure.
| Fórmula | Nom IUPAC recomanat a la Viquipèdia | Nom IUPAC no recomanat a la Viquipèdia | Nom no acceptat per la IUPAC |
|---|---|---|---|
| KF | fluorur de potassi | fluorur potàssic | |
| HgCl₂ | clorur de mercuri(II) | diclorur de mercuri; clorur de mercuri(2+) | clorur mercúric; clorur de mercuri (II) |
| CuH | hidrur de coure(I) | hidrur de coure; hidrur de coure(1+) | hidrur cuprós; hidrur de coure (I) |
| Fe₂O3 | òxid de ferro(III) | triòxid de ferro; òxid de ferro(3+) | òxid fèrric; òxid de ferro (III) |
| BaO₂ | peròxid de bari | diòxid de bari; diòxid(2-) de bari | peròxid bàric |
| AgBr | bromur d'argent(I) | bromur de plata; bromur d'argent(1+) | bromur d'argent (I) |
| NaOH | hidròxid de sodi | hidròxid sòdic | |
| Pb(OH)4 | hidròxid de plom(IV) | tetrahidròxid de plom; hidròxid de plom(4+) | hidròxid plúmbic; hidròxid de plom (IV) |
Composts no metall-no metall[modifica]
En els composts binaris entre dos no metalls es recomana l'ús de la nomenclatura de composició mitjançant prefixos multiplicadors. El nom es forma seguint les regles:
- L'element més electronegatiu s'anomena primer indicant el nombre d'àtoms a la fórmula mitjançant un prefix multiplicador (di-, tri-, tetra-, penta-, hexa-,...) i amb la terminació d'anió (fluorur, clorur, òxid, hidròxid…)
- A continuació es posa la preposició de.
- Finalment s'anomena l'element més electropositiu indicant el nombre d'àtoms a la fórmula mitjançant un prefix multiplicador (di-, tri-, tetra-, penta-, hexa-,...).
| Fórmula | Nom IUPAC recomanat a la Viquipèdia | Nom IUPAC no recomanat a la Viquipèdia | Nom no acceptat per la IUPAC |
|---|---|---|---|
| H₂S | sulfur d'hidrogen | sulfà | àcid sulfhídric |
| P₂O3 | triòxid de difòsfor | òxid de fòsfor(III) | òxid de fòsfor (III) |
| O5I₂ | diiodur de pentaoxigen | pentaòxid de diiode | |
| N₂O | òxid de dinitrogen | òxid de nitrogen(I) | òxid nitrós; òxid de nitrogen (I) |
| PH3 | trihidrur de fòsfor | fosfà; hidrur de fòsfor(III) | fosfina; hidrur de fòsfor (III) |
| SF6 | hexafluorur de sofre | fluorur de sofre(VI) |
Nomenclatura dels oxoàcids[modifica]
La nomenclatura tradicional no canvia per a la nomenclatura dels oxoàcids. Per tant la utilització de prefixos (hipo-, per-, meta-, di-) i sufixos (-ós i -ic) per indicar els nombres d’oxidació i l’estequiometria entre els òxids i les molècules d’aigua es mantén. No obstant això:
- Es deixen d’utilitzar el prefix orto- per als àcids dels grups 13 i 15 de la taula periòdica (B, Si, P, As i Sb), per innecessari,
- i el prefix piro-, que s’ha de substituir pel prefix di- per indicar la combinació de l’òxid amb dues molècules d’aigua.
| Fórmula | Nom IUPAC recomanat a la Viquipèdia | Nom IUPAC no recomanat a la Viquipèdia | Nom no acceptat per la IUPAC |
|---|---|---|---|
| H3PO4 | àcid fosfòric | trihidroxidoxidfosfor; trihidrogen(tetraoxidfosfat) | àcid ortofosfòric |
| H4P₂O7 | àcid difosfòric | tetrahidroxidtrioxiddifosfor; tetrahidrogen(heptaoxiddifosfat) | àcid pirofosfòric |
| HPO3 | àcid metafosfòric | hidroxiddioxidfosfor; hidrogen(trioxidfosfat) | |
| HNO₂ | àcid nitrós | hidroxidoxidnitrogen; hidrogen(dioxidnitrat) | |
| HNO3 | àcid nítric | hidroxiddioxidnitrogen; hidrogen(trioxidnitrat) |
Nomenclatura dels anions heteropoliatòmics[modifica]
Els anions derivats dels oxoàcids es recomana que s'anomenin seguint el sistema tradicional, acceptat per la IUPAC. Se substitueixen els sufixos de la nomenclatura tradicional -ós i -ic de l'àcid del que deriven per - it i -at respectivament.
| Fórmula | Nom IUPAC recomanat a la Viquipèdia | Nom IUPAC no recomanat a la Viquipèdia | Nom no acceptat per la IUPAC |
|---|---|---|---|
| OCl- | hipoclorit | oxidclorat(1-) | |
| SO32- | sulfit | trioxidsulfat(2-) | |
| ClO4- | perclorat | tetraoxidclorat(1-) | |
| HCO3- | hidrogencarbonat | hidrogen(trioxidcarbonat)(1-) | |
| Cr₂O72- | dicromat | heptaoxiddicromat(2-) |
Nomenclatura de les oxosals[modifica]
Per anomenar una oxosal s'empre el nom de l'anió, continuació s'afegeix la preposició de, i es completa amb el nom del metall indicant entre parèntesi amb nombres romans el seu nombre d’oxidació. No s'ha de deixar cap espai entre el nom i el parèntesi, malgrat contradigui l'ús habitual dels parèntesis en català. Si el metall només té un estat d’oxidació, aquest no s’indica.
| Fórmula | Nom IUPAC recomanat a la Viquipèdia | Nom IUPAC no recomanat a la Viquipèdia | Nom no acceptat per la IUPAC |
|---|---|---|---|
| PbSO3 | sulfit de plom(II) | trioxidsulfat de plom; trioxidsulfat(2-) de plom(2+) | sulfit plumbós; sulfit de plom (II) |
| Na₂CO3 | carbonat de sodi | trioxidcarbonat de disodi; triòxidcarbonat(2-) de sodi | carbonat sòdic |
| Cu(NO₂)₂ | nitrit de coure(II) | bis(dioxidnitrat) de coure; dioxidnitrat(1-) de coure(2+) | nitrit cúpric; nitrit de coure (II) |
| Fe₂(SO4)3 | sulfat de ferro(III) | tris(tetraoxidsulfat) de diferro; tetraoxidsulfat(2-) de ferro(3+) | sulfat fèrric; sulfat de ferro (III) |
| NaHCO3 | hidrogencarbonat de sodi | hidrogen(trioxidcarbonat) de sodi | bicarbonat sòdic; bicarbonat de sodi |
Nomenclatura dels composts de coordinació[modifica]
Els noms dels lligants aniònics, tant els inorgànics com els orgànics, reben la terminació -o. Així els noms dels anions acabats en -ur, -it o -at es converteixen en -uro, -ito, -ato, respectivament. Així els anions hidrur, sulfit i nitrat quan actuen com a lligants reben el nom d'hidruro, sulfito i nitrato. Si el complex és aniònic s'afegeix la terminació -at al nom de l'àtom central.
| Fórmula | Nom IUPAC recomanat a la Viquipèdia | Nom IUPAC no recomanat a la Viquipèdia | Nom no acceptat per la IUPAC |
|---|---|---|---|
| K4[Fe(CN)6] | hexacianoferrat(II) de potassi | hexacianoferrat(4-) de potassi; hexacianoferrat de tetrapotassi | |
| [CrBr(H₂O)5](NO3)₂ | nitrat de pentaaquabromcrom(III) | nitrat de pentaaquabromcrom(2+) | |
| Na3[AlF6] | hexafluoroaluminat(III) de sodi | hexafluoroaluminat(3-) de sodi | |
| K[Co(CO)4] | tetracarbonilcobaltat(-I) de potassi | tetracarbonilcobaltat(1-) de potassi | |
| [Pt(NH3)4][PtCl6] | hexacloroplatinat(IV) de tetraaminaplatí(II) | hexacloroplatinat(2-) de tetraaminaplata(2+) |
Nomenclatura dels composts d'addició[modifica]
Els composts d'addició, o adductes, són formats per la combinació de dues o més substàncies estables amb una proporció estequiomètrica fixa, però amb una estructura sovint incerta. Hi trobam els solvats, clatrats i els composts d'intercalació. S'anomenen mitjançant els noms dels seus components separats per un guió ultrallarg (—), i indicant la proporció de cada espècie després del nom per números aràbics, entre parèntesis, separats per barres inclinades. El parèntesi ha d'anar separat del nom per un espai. Els noms dels components s'escriuen segons el número creixent, si n'hi ha el mateix nombre s'ordenen alfabèticament segons els primers símbols. Com a única excepció, si contenen aigua, se cita sempre en últim lloc.
| Fórmula | Nom IUPAC recomanat a la Viquipèdia | Nom IUPAC no recomanat a la Viquipèdia | Nom no acceptat per la IUPAC |
|---|---|---|---|
| CaCl₂·8NH3 | clorur de calci—amoníac (1/8) | ||
| Kr·46H₂O | criptó—aigua (1/46) | ||
| Na₂CO3·10H₂O | carbonat de sodi—aigua (1/10) | carbonat de sodi decahidrat | |
| 3CdSO4·8H₂O | sulfat de cadmi—aigua (3/8) |
Nomenclatura dels composts orgànics[modifica]
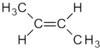
La nomenclatura dels composts orgànics és molt complexa i aquí només es presenten unes recomanacions en quan als composts orgànics més simples. Les darreres recomanacions de la IUPAC són del 2013 i modifiquen les recomanacions anteriors del 1993 i de 1979. En la darrera publicació la IUPAC ja presenta el nom IUPAC preferit o PIN, amb l'objectiu de que cada compost tingui un únic nom a efectes legals, comercials, sanitaris, etc. Les recomanacions del 1993 modificaven unes anteriors del 1979 essent el canvi més important que els localitzadors del grup principal o dels dobles i triples enllaços s'han de situar just davant el corresponent sufix i no davant del nom com es feia abans. A continuació hi ha exemples de composts senzills:
Per a composts més complexos el nom sistemàtic de la IUPAC resulta molt llarg i complicat, la qual cosa fa recomanable no emprar-lo a la Viquipèdia com a nom de l'article ni dintre d'ell. En aquests casos es recomana emprar el nom comú, tant al títol com en el text i especificar el nom sistemàtic de la IUPAC, el PIN, al principi de la introducció de l'article i a la infotaula. Es pot crear un article amb el títol igual que el PIN que tengui una redirecció cap a l'article anomenat amb el nom comú.
Bibliografia[modifica]
- Casassas i Simó, E.; Sales i Cabré, J. Nomenclatura de química inorgànica: recomanacions de 1990. 1a. Barcelona: Institut d'Estudis Catalans, 1997. ISBN 9788472833609.
- Connelly, N.G.; Damhus, T. Nomenclature of Inorganic Chemistry: IUPAC recommendations 2005 (en anglès). 1a. Cambridge, UK: Royal Society of Chemistry, 2005. ISBN 9780854044382.
- Connelly, N.G.; Damhus, T. Nomenclatura de Química Inorgànica. Recomendaciones de 2005 (en castellà). 1a. Saragossa: Prensas Universitarias de Zaragoza, 2007.
- Favre, H.A.; Powell, W.H. Nomenclature of Organic Chemistry: IUPAC Recommendations and Preferred Names 2013 (en anglès). 1a. Cambridge, UK: Royal Society of Chemistry, 2013. ISBN 9780854041824.
- Sales i Cabré, J.; Vilarrasa i Llorens, J. Introducció a la nomenclatura química. Inorgànica i orgànica. 5a. Barcelona: Reverte, 2006. ISBN 9788429175516.