Inserció migratòria
Reacció química organometàl·lica on el lligand aniònic i el lligand neutre d'un complex metàl·lic, ambdós lligands en posició cis, es combinen entre si per generar un únic lligand aniònic. És una inserció 1,1 d'un lligand neutre.
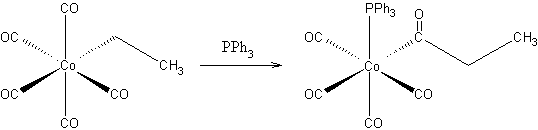
Al produir-se la reacció queda lliure un orbital del metall (es genera una vacant de coordinació) que ràpidament queda ocupat per qualsevol lligand neutre a 2 electrons que tinguem en dissolució per tal de mantenir el seu estat d'oxidació invariable. El centre metàl·lic és un metall de transició generalment deficient en electrons.[1]
Propietats[modifica]
- No tenim un canvi formal de l'estat d'oxidació (a excepció dels alquilidens)
- Els dos lligands implicats (aniònic i neutre) han de trobar-se en posició cis
- Cal tenir lligands neutres per poder ocupar la vacant de coordinació generada i així evitar reaccions secundàries com poden ser la β-eliminació
- Generalment aquesta reacció és més afavorida per centres metàl·lics deficients en electrons.
Classificació de lligands[modifica]
En aquesta reacció tenim 2 tipus de lligands implicats els aniònics i els neutres. Alguns dels més comuns són:
- Lligands neutres: CO (carbonil), NH₃ (amoniac), PR₃ (fosfines), CNR, alquens, alquins, carbens, etc. En el cas dels lligands CO aquests s'insereixen en enllaços metall-alquil o metall-aril, però molt difícilment en enllaços metall-H o altres enllaços metall-acil, metall-halur, etc.
- Lligands aniònics: H- (hidrur), alquils R- com el CH3- (metil), Ph- (aril), CN-, RS-, RO-, η¹-al·lil, η¹-acetat, O2- (oxo), etc.
Mecanisme[modifica]

El primer pas és la migració del grup metil cap a un dels lligands neutres en posició cis, en aquest punt ens queda lliure una vacant de coordinació de dos electrons (complex de 16electrons) i que ràpidament torna a ser ocupada pels dos electrons del lligand neutre que tinguem en dissolució, ja sigui un grup CO o qualsevol altre dels citats abans per acabar donant el producte. El producte torna a complir la regla dels 18 electrons.
La segona etapa és la determinant de la velocitat de la reacció (k₂) i és en aquest punt on cal tenir especial cura que hi hagi lligands neutres presents en dissolució per tal d'evitar reaccions secundàries.
Una forma molt intuïtiva per entendre el mecanisme és fer un marcatge isotòpic. Per exemple, si el que fem és marcar el lligand entrant per exemple un grup carbonil amb el carboni marcat 13CO, el producte obtingut tindrà un sol lligand marcat i aquest es trobarà en posició cis respecte al nou lligand format (en aquest exemple seria el grup acetil).
És una reacció d'equilibri susceptible de tornar enrere si apliquem temperatura o a vegades també podem patir la β-eliminació si tenim protons en β.
Enllaços externs[modifica]
- Migratory Insertion Arxivat 2004-09-13 a Wayback Machine.
- The Organometallic HyperTextBook: Insertion Reactions
Referències[modifica]
- ↑ H.Crabtree, Robert. «Insertion and elimination». A: The organometallic chemistry of the transition metals. Primera edició. Wiley-Interscience, 1988, p. 142-159.
