Reacció SN1
La reacció SN1 o substitució nucleòfila unimolecular és un tipus de substitució nucleòfila que consta de dos passos, entre els quals es passa per un intermedi carbocatiònic.
Mecanisme[modifica]
La reacció consta de dues etapes: en la primera, es trenca l'enllaç entre el grup sortint i el substrat, formant-se així un intermedi carbocatiònic que té una hibridació sp² (geometria plana). En la segona etapa, el nucleòfil ataca l'intermedi.
Exemple[modifica]
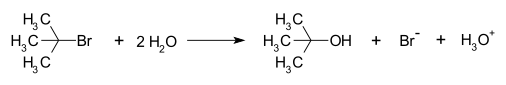
Un exemple de reacció que té lloc a través d'un mecanisme SN1 és la hidròlisi del bromur de terc-butil amb aigua per formar t-butanol.
Aquesta reacció SN1 té lloc en tres etapes:
- Formació del carbocatió terc-butil per la separació del grup sortint (un anió bromur) de l'àtom de carboni: aquesta etapa és lenta i reversible.[1]
- Atac nucleofílic: el carbocatió reaccióna amb el nucleòfil. Si el nucleòfil és una molècula neutra (per exemple, el dissolvent) es necessita una tercera etapa per completar la reacció. Quan el dissolvent és aigua l'intermedi és un ió oxoni. Aquesta etapa de la reacció és ràpida.
- Desprotonació: eliminació d'un àtom d'hidrogen del nucleòfil protonat amb aigua actuant com a base, formant l'alcohol i un ió oxoni. Aquesta etapa és ràpida.
Cinètica de la reacció[modifica]
La reacció SN1 segueix una cinètica de primer ordre, ja que en l'etapa lenta, la de ruptura de l'enllaç entre substrat i grup sortint, només hi intervé l'espècie R-X.
Factors que afecten a la velocitat de reacció[modifica]
- Substrat. La velocitat dependrà de la capacitat d'estabilitzar l'intermedi de reacció. Els substrats terciaris reaccionen ràpid, ja que els respectius carbocations són més estables.
- Nucleòfil. La naturalesa del nucleòfil no afecta apreciablement a la velocitat, ja que aquest enra a l'etapa ràpida.
- Dissolvent. Els dissolvents polars solvaten el catió intermedi, estabilitzant-lo i rebaixant així l'energia d'activació.
- Grup sortint. La capacitat d'estabilitzar el grup sortint afecta enormement a la velocitat de reacció, ja que l'etapa limitant és precisament la sortida d'aquest.
Referències[modifica]
- ↑ Peters, K. S. «Nature of Dynamic Processes Associated with the SN1 Reaction Mechanism». Chem. Rev., 107, 3, 2007, pàg. 859–873. DOI: 10.1021/cr068021k. PMID: 17319730.




![{\displaystyle v=k\cdot [R-X]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/2ca8984b8466c92364f3000ff92673b13cf17ed2)