Aldehid
| Substància química | classe estructural d'entitats químiques |
|---|---|
| Estructura química | |
 | |
| SMILES canònic | |
Un aldehid és un compost orgànic que conté un grup carbonil terminal, o sigui que el grup carbonil està enllaçat a un àtom d'hidrogen i a un altre àtom de carboni. La fórmula general que representa els compostos que presenten aquest grup funcional és R-CHO.
El grup aldehid és electròfil a causa de la deficiència electrònica de l'àtom de carboni.
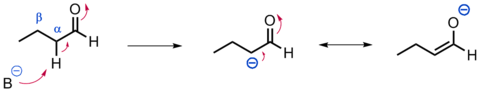
Com en els altres grups funcionals que presenten un grup carbonil, els àtoms d'hidrogen situats en posició α són relativament àcids (en els aldehids pKa ~17) a causa de l'estabilització per ressonància de la base conjugada.
Nomenclatura[modifica]

Segons les normes de la IUPAC,[1][2] aquests compostos s'anomenen substituint la terminació -à de l'alcà corresponent per la terminació -al. A banda d'això, pels següents compostos també es permet la utilització de la nomenclatura trivial:
- HCHO es pot anomenar formaldehid
- CH₃CHO es pot anomenar acetaldehid
- C₆H₅CHO es pot anomenar benzaldehid
En el cas que la molècula presenti un altre grup funcional prioritari (un grup àcid carboxílic), s'utilitza el prefix oxo- per designar el grup aldehid.
Química[modifica]
Síntesi[modifica]
Els aldehids es poden preparar per diferents mètodes:
- Oxidació d'alcohols primaris. Aquest mètode es basa en la reacció d'un alcohol primari amb agents oxidants suaus, com per exemple PCC,[3] PDC,[4] IBX,[5] el periodinà de Dess-Martin (DMP)[6] o l'oxidació de Swern.[7] Agents oxidants més forts com el dicromat o permanganat potàssic portarien a l'oxidació directa fins a àcid carboxílic.
- Ozonòlisi d'alquens.[8] La reacció d'un alquè amb ozó porta a la formació d'un ozònid, un intermedi altament reactiu que reacciona amb espècies reductores per donar un grup aldehid.[9][10]
- Reducció d'èsters. La reducció d'aquests compostos amb agents reductors com el DIBAL-H o el LDBBA són capaços d'aturar-se en l'estadi d'aldehid.[11][12]
- Reducció de clorurs d'àcid utilitzant la reacció de Rosenmund.[13]
- Homologació de cetones amb metoximetilentrifenilfosfina, utilitzant una modificació de la reacció de Wittig.[14]
- Reaccions de formilació. Aquestes reaccions, com la Vilsmeier-Haack,[15] s'utilitzen per introduir grups aldehid.
- Reacció de Nef. La hidròlisi de nitroalcans primaris porta a la formació d'aldehids.[16]
Tautomeria ceto-enol[modifica]

La tautomeria ceto-enol es refereix a l'equilibri que existeix entre la forma ceto i enol en els aldehids i les cetones.[17] Aquest equilibri està catalitzat per àcids i bases, i generalment es troba desplaçat cap a la forma carbonílica, ja que aquesta és més estable.
Reaccions d'oxidació i reducció[modifica]

- Els aldehids es poden reduir a alcohols primaris, utilitzant agents reductors com el borhidrur de sodi (NaBH₄) o l'hidrur d'alumini i liti (LiAlH₄).
- Els aldehids es poden oxidar a àcids carboxílics emprant agents oxidants com el permanganat potàssic (KMnO₄) o el dicromat potàssic (K₂Cr₂O₇).
- Al sotmetre un aldehid que no presenta àtoms d'hidrogen en posició α (per exemple el benzaldehid) a un medi fortament bàsic, es dona la reacció de Cannizzaro,[18] en la que l'aldehid desproporciona per donar l'alcohol i l'àcid carboxílic corresponent.
Reaccions d'addició nucleofílica[modifica]
En les reaccions d'addició nucleofílica, un nucleòfil s'addiciona a l'àtom de carboni del grup carbonil per donar un compost en el que aquest àtom de carboni té geometria tetraèdrica. Juntament amb la protonació de l'àtom d'oxigen del grup carbonil (que es pot donar abans o després de l'addició del nucleòfil), aquesta reacció dona un producte en el que l'àtom de carboni del grup carbonil està enllaçat al nucleòfil, a un àtom d'hidrogen i a un grup hidroxil.

En molts casos, l'addició del nucleòfil provoca la pèrdua d'una molècula d'aigua. En aquests casos aquesta reacció s'anomena d'addició-eliminació o reacció de condensació.
Alguns exemples de reaccions d'addició nucleofílica són els següents:
- En les reaccions d'acetalització un alcohol s'addiciona al grup carbonil sota catàlisi àcida o bàsica per formar un hemiacetal. Sota catàlisi àcida, l'hemiacetal pot reaccionar amb una segona molècula d'alcohol per formar l'acetal. Els hemiacetals cíclics, com els de la glucosa solen ser estables. Els acetals són estables, però reverteixen a la forma carbonílica al tractar-los amb àcid.
- Els aldehids poden reaccionar amb aigua per formar hidrats, compostos de l'estil R-C(H)(OH)(OH). Tot i això, aquests compostos només són estables amb la presència de grups fortament electroatraients, com en l'hidrat de cloral. El mecanisme de formació d'aquests compostos és el mateix que en el cas dels acetals.
- L'addició d'amines primàries i secundàries al grup aldehid porta a l'obtenció dels corresponents hemiaminals (R-C(H)(OH)(NR₂)), intermedis que poden eliminar una molècula d'aigua per acabar obtenint imines o ions imini en el cas de les amines secundàries.
- La reacció d'un aldehid amb HCN permet obtenir cianhidrines, compostos de fórmula general R-C(H)(OH)(CN).
- En la reacció de Grignard, un reactiu de Grignard (també anomenat magnesià) s'addiciona al grup aldehid per donar l'alcohol corresponent substituït amb el grup provinent del reactiu de Grignard.
- En les reaccions aldòliques el enolats de cetones, èsters, amides i àcids carboxílics s'addicionen a aldehids per formar compostos β-hidroxicarbonílics (aldols). La deshidratació posterior sota catàlisi àcida o bàsica porta a la formació de compostos α,β-insaturats. La combinació d'aquests dos passos (addició i deshidratació) es coneix com a condensació aldòlica.
- La hidroxilamina (NH₂OH) es pot addicionar al grup carbonil. L'eliminació d'aigua resulta en la formació de l'oxima.
Exemples d'aldehids[modifica]
Vegeu també[modifica]
Referències[modifica]
- ↑ IUPAC. Nomenclature of Organic Chemistry ("Blue Book")
- ↑ «Short summary of IUPAC nomenclature of organic compounds». Arxivat de l'original el 2009-02-26. [Consulta: 18 febrer 2009].
- ↑ Pyridinium chlorochromate (PCC)
- ↑ Pyridinium dichromate (PDC)
- ↑ IBX, 2-Iodoxybenzoic acid
- ↑ Dess-Martin periodinane, IBX, Triacetoxyperiodinane
- ↑ Swern Oxidation
- ↑ Ozonolysis
- ↑ Criegee, R. Angew. Chem. Int. Ed. Engl. 1975, 745-752.doi:10.1002/anie.197507451
- ↑ Geletneky, C.; Berger, S. Eur. J. Org. Chem. 1998, 1625-1627.
- ↑ Zakharkin, L. I.; Khorlina, I. M. Tet. Lett. 1962, 619-620.doi:10.1016/S0040-4039(00)70918-X
- ↑ Kim, M. S.; Choi, Y. M.; An, D. K. Tet. Lett. 2007, 5061-5064.doi:10.1016/j.tetlet.2007.05.091
- ↑ Rosenmund Reduction
- ↑ Levine, S. G. J. Am. Chem. Soc. 1958, 6150-6151.doi:110.1021/ja01555a068
- ↑ Vilsmeier-Haack Reaction
- ↑ Pinnick, H. W. Organic Reactions 1990.doi:10.1002/0471264180.or038.03
- ↑ IUPAC Gold Book - Tautomerism doi:10.1351/goldbook.T06252
- ↑ Cannizzaro Reaction
Bibliografia[modifica]
- Clayden, J.; Greeves, N.; Warren, S.; Wothers, P., Organic chemistry, Oxford University Press, 2001.
Enllaços externs[modifica]
| A Wikimedia Commons hi ha contingut multimèdia relatiu a: Aldehid |
- Organic Chemistry Animations ChemTube3d (anglès)
- Aldehyde. Encyclopedia Britannica (anglès)
- Organic-chemistry.org (anglès)
- IUPAC. Compendium of Chemical Terminology, 2nd ed. (the "Gold Book").doi:10.1351/goldbook.A00208
