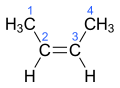Alquè
| Substància química | classe estructural d'entitats químiques |
|---|

Els alquens, també anomenats olefines, són hidrocarburs alifàtics que tenen algun doble enllaç entre els àtoms de carboni i per això són anomenats insaturats. La fórmula genèrica dels alquens és i l'alquè més simple és l'etè, . El més important a escala industrial és l'etè, punt de partida per a l'obtenció d'altres composts químics importants.
Etimologia[modifica]
Molts dels primers composts orgànics que es caracteritzaren provenien de greixos i, per tant, foren anomenats «alifàtics», del grec ἄλειφαρ, -ατος áleiphar, -atos 'ungüent' i ‒́ic. L'observació que els alcans eren insolubles en aigua i poc reactius originà el nom «parafines», del llatí Paraffin, i aquest del llatí parum affīnis 'poc afí'. Per contra, els alquens reaccionent fàcilment amb, per exemple, halògens, per formar compostos greixosos i, per tant, se'ls anomenà «olefines», una contracció del francès gaz oléfiant, nom antic de l'etè, que prové del llatí oleum, 'oli' i de -fiant del sufix -fier, 'en relació a'. En adonar-se que els grups alquil podien conservar-se en les reaccions sense canvis, de la mateixa manera que ho fan els ions dels metalls alcalins, i que reaccionaven amb els halògens, s'establí que les classes de composts orgànics amb aquestes propietats es derivarien del mot «alquil», i d'aquí els noms alcà, alquè i alquí. El mot «alquil» deriva de l'àrab clàssic al-kuhl, que originàriament s'emprava per anomenar pols fina de minerals d'antimoni emprada en cosmètica i que passà a anomenar substàncies molt fines, molt pures o destil·lades, com l'alcohol (etanol).[1]
El 1866 els sufixos patronímics femenins grecs -ηνη -ene, -ινη -ine, i -ονη -one (Ismene, Mersin, Hermione, Persèfone…) estaven en ús dispers com a sufixos d'hidrocarburs que significaven «filla de», així que el químic alemany August Wilhelm von Hofmann (1818-1892), un antic estudiant de Justus von Liebig (1803-1873), suggerí sistematitzar la nomenclatura utilitzant tota la seqüència de vocals a, e, i, o, u per crear sufixos per als hidrocarburs , , , i , respectivament. Només els tres primers sufixos (en català: -à, -è, -í), romangueren per anomenar els hidrocarburs amb enllaços simples, dobles i triples, respectivament.[2]
Geometria molecular[modifica]

El doble enllaç covalent que present en els alquens confereix la major part de les propietats dels alquens. Aquest doble enllaç C=C consta d'un enllaç σ i un enllaç π. Els dos àtoms de carboni tenen una hibridació sp², hibridació resultant de la barreja d'un orbital molecular 2s i dos orbitals 2p, la qual cosa conduïx a la formació de tres orbitals híbrids sp², de geometria trigonal plana. Aquests orbitals sp² poden combinar-se per a formar un enllaç σ, entre ambdós carbonis en la direcció que uneix els nuclis dels carbonis. Per altra banda l'enllaç π resulta de la superposició dels orbitals atòmics p que no han hibridat. En aquest tipus d'enllaç, els electrons estan deslocalitzats al voltant dels carbonis, per damunt i per sota del plànol molecular. Energèticament, s'observa que la superposició dels orbitals sp² és molt més efectiva que la dels orbitals p i per tant la component σ és bastant més energètica que la π. El fet que el doble enllaç sigui rígid (en contraposició a l'enllaç simple, format per un sol enllaç σ, que pot girar lliurement al llarg del seu eix) es deu a la presència dels orbitals π, així, si volem que existeixi una rotació, és necessari trencar els enllaços π i tornar a formar-los. L'energia necessària per a trencar aquests enllaços no és massa elevada, de l'ordre dels 65 kcal·mol–1, la qual cosa correspon a temperatures d'entre 400 i 500 °C. Això significa que per sota d'aquestes temperatures els dobles enllaços romanen rígids i, per tant, la molècula té una configuració estable, però per damunt l'enllaç π pot trencar-se i tornar-se a formar i apareix una rotació lliure.
Polaritat[modifica]
Depenent de l'estructura, pot aparèixer un moment dipolar feble. L'enllaç alquil-alquenil està polaritzat en la direcció de l'àtom amb orbital sp², ja que la component s d'un orbital sp² és major que en un sp3 (això podria interpretar-se com la proporció de s a p en la molècula, sent 1:2 en sp² i 1:3 en sp3, encara que aquesta idea és simplement intuïtiva). Això és degut al fet que els electrons situats en orbitals híbrids amb major component s estan més lligats al nucli que els p, per tant l'orbital sp² és lleugerament captador d'electrons i apareix una polarització neta cap a ell. Una vegada que tenim polaritat en l'enllaç neta, la geometria de la molècula ha de permetre que aparegui un moment dipolar net en la molècula.
Isomeria cis-trans[modifica]
El fet que no sigui possible la rotació al voltant de l'enllaç doble, fa que si els dos àtoms d'un mateix carbonis són diferents, i això passa a ambdós carbonis del doble enllaç, existeixen isòmers anomenats cis i trans. El cis és l'isòmer que té els substituents al mateix costat, i l'isòmer trans els que els té oposats.
Nomenclatura[modifica]

Segons les normes de la Unió Internacional de Química Pura i Aplicada (IUPAC), els alquens s'anomenen indicant el nombre de carbonis de la cadena lineal més llarga amb els prefixos et-, prop-, but-, pent-... per a 2, 3, 4, 5... carbonis respectivament, i el sufix -è. Si la cadena forma un anell s'ha de posar davant el prefix ciclo-. Exemples són: etè, propè, ciclohexè.[3]
La posició del doble enllaç s'ha d'indicar, excepte si no hi més d'una posició possible, mitjançant un localitzador numèric que s'ha de situar just davant del sufix, separant-lo del prefix i del sufix amb guions. El localitzador ha de ser el més baix dels dos carbonis afectats. La numeració ha de començar per l'extrem més pròxim al doble enllaç. Per exemple: but-1-è o but-2-è.[3]

Quan hi ha més d'un doble enllaç, s'anomenen indicant la posició de cadascun d'ells i especificant amb els sufixos -adiè, -atriè, -atetraè, etc. davant del sufix -è el nombre de dobles enllaços presents. Exemples: buta-1,3-diè o hexa-1,3,5-triè.[3]
Quan els alquens presenten ramificacions, la cadena principal és aquella que conté més dobles enllaços. En segon terme, segueixen vigents les normes dels hidrocarburs ramificats. La numeració es fa començant per l'extrem més pròxim a un doble enllaç. Exemples: 6-etilnona-1,4-diè o 3-metil-4-propilhexa-1,4-diè.[3]
Propietats físiques[modifica]
La presència del doble enllaç modifica lleugerament les propietats físiques dels alquens enfront dels alcans. D'aquestes, la temperatura d'ebullició és la qual menys es modifica. A temperatura ambient els primers membres de la sèrie, l'etè, el propè i els butens, són gasos a temperatura ambient; els catorze següents són líquids; i els de més carbonis són sòlids.[4]
La presència del doble enllaç es nota més en aspectes com la polaritat i l'acidesa. Espectroscòpicament, els enllaços dobles aïllats són transparents a la radiació visible i a la ultraviolada pròxima, mentre que els conjugats i els cumulats absorbeixen longituds d'ona superiors a 214 i 180 nm, respectivament. Els alquens donen una absorció característica a la zona de 1 640–1 690 cm–1 de l'infraroig.[5]
Propietats químiques[modifica]
Acidesa[modifica]
El carboni alquenil té major acidesa enfront dels alcans, degut també a la polaritat de l'enllaç. Així, l'età (un alcà) té un pKa de 50 (o un Ka de 10–50) enfront del pKa = 44 de l'etè. Aquest fet s'explica fàcilment considerant que, al desprendre's un protó de la molècula, queda una càrrega negativa romanent que en el cas de l'etè es deslocalitza més fàcilment en l'enllaç π i σ que en l'enllaç σ simple que existeix en un alcà. De totes maneres, la seva acidesa és molt menor que la dels alcohols o els àcids carboxílics.[6]
Reaccions químiques[modifica]

Hidratació[modifica]
La reacció d'hidratació és una reacció d'addició d'aigua al doble enllaç catalitzada per un àcid, àcid sulfúric, , o àcid fosfòric, . Si l'alquè és propè s'obté propan-2-ol d'acord amb la regla de Markóvnikov (un hidrogen de l'aigua s'addiciona al carboni amb més hidrògens i el grup hidroxil, , a l'altre carboni del doble enllaç). La reacció requereix temperatures d'uns 250 °C i un pH elevat. S'empra industrialment.[6]

Oximercuració[modifica]
La reacció d'hidratació requereix condicions d'altes temperatures difícils d'aconseguir en els laboratoris. L'addició d'un grup hidroxil, , es pot dur a terme mitjançant la reacció d'oximercuració en condicions més suaus. Primer es duu a terme una reacció amb etanoat de mercuri(II) dissolt en tetrahidrofurà aquós, formant-se un complex organometàl·lic de mercuri. Seguidament es fa reaccionar amb borohidrur de sodi, , i a partir de propè s'obté propan-2-ol.

Hidroboració[modifica]
La hidroboració és una reacció on s'addiciona un trihidrur de bor o borà, al propè i s'obté un organoborà. El producte obtingut és anti-Markóvnikov. Seguidament es pot oxidar aquest compost mitjançant peròxid d'hidrogen en medi bàsic i, si l'alquè és propè, s'obté el propan-1-ol.[6]

Dihidroxilació[modifica]
La reacció d'hidroxilació consisteix en l'addició de dos grups hidroxil, , un a cada carboni del doble enllaç. S'empra com a reactiu peròxid d'hidrogen, , i requereix emprar com a catalitzador òxid d'osmi(VIII), , car i tòxic. Es forma un producte intermediari, un osmat que es pot tractar amb hidrogensulfit de sodi, , i si l'alquè és propè dona el propan-1,2-diol.[6]

Halogenació[modifica]
L'halogenació consisteix en l'addició electròfila d'una molècula d'un halogen (, , o ) al doble enllaç, formant-se un derivat dihalogenat, amb un àtom d'halogen addicionat a cadascun dels carbonis que formen el doble enllaç. En el cas del propè si l'halogen és el brom es forma 1,2-dibromopropà.[6]

Addició d'halurs d'hidrogen[modifica]
L'addició d'un halur d'hidrogen (, , o ) dona lloc a un haloalcà. En el cas del propè es formen dos productes, si s'addiciona bromur d'hidrogen s'obté un 90 % de 2-bromopropà i un 10 % d'1-bromopropà, seguint la regla de Markóvnikov.[6]
En cas que la reacció tengui lloc en presència de peròxids orgànics, s'obté majoritàriament el producte anti-Markóvnikov.[6]
Addició d'àcids hipohalurosos[modifica]
L'àcid hipoclorós i l'àcid hipobromós poden addicionar-se al doble enllaç formant halohidrines, això és un compost amb un halogen enllaçat a un carboni i un grup hidroxil, , al carboni veí.[6]
Reacció de Diels-Alder[modifica]

La reacció de Diels-Alder és una cicloaddició d'un alquè, o un compost més complexe que contengui un doble enllaç, amb un diè conjugat. S'obté un cicloalquè de sis costats, un ciclohexè. És un dels mètodes més importants per a l'obtenció d'alquens cíclics de sis costats.[7]

Hidrogenació[modifica]
Un alquè pot reduir-se a un alcà mitjançant hidrogenació fent passar un corrent d'hidrogen sobre un catalitzador. El platí i el pal·ladi són els catalitzadors més comuns per a la hidrogenació dels alquens; el pal·ladi s'utilitza en general en forma de pols molt fi “suportat” en un material inert com el carbó vegetal (Pd/C) per maximitzar l'àrea superficial. El platí s'utilitza habitualment com òxid de platí(IV), , un catalitzador anomenat catalitzador d'Adams.[6]

Epoxidació[modifica]
Els alquens s'oxiden per donar epòxids en el tractament amb un peroxoàcid, , com l'àcid meta-cloroperoxobenzoic. Un epòxid, també anomenat oxirà, és un èter cíclic amb un àtom d'oxigen en un anell de tres membres.[6] En el cas del propè es forma òxid de propè o 1,2-epoxipropà, un compost de gran importància industrial.
Oxidació[modifica]
L'oxidació pot tenir lloc emprant ozó, , o permanganat de potassi, . L'ozó, preparat passant un flux d'oxigen a través d'una descàrrega elèctrica d'alt voltatge, s'addiciona ràpidament al propè a baixes temperatures per donar un intermediari cíclic anomenat molozònid. Aquest es transposa espontàniament per formar un ozònid que es tracta immediatament amb un agent reductor com el zinc metàl·lic en àcid acètic per convertir-lo en metanal i etanal, dos aldehids.[6]
Mitjançant la reacció amb permanganat de potassi en medi àcid o neutre s'obté també la ruptura del doble enllaç i la formació, en aquest cas, d'àcid etanoic i diòxid de carboni.[6]
Preparació[modifica]
Per a la preparació d'alquens determinats hom empra principalment les reaccions de deshidratació d'alcohols amb alúmina, deshidrohalogenació d'halurs d'alquil amb potassa alcohòlica, piròlisi d'hidròxids d'amoni quaternari, reacció de Wittig i hidrogenació parcial d'alquins.

Deshidratació d'alcohols[modifica]
Les reaccions de deshidratació catalitzades per àcids (àcid sulfúric, àcid fosfòric, òxid d'alumini...) són reaccions d'eliminació d'aigua d'un alcohol formant-se un doble enllaç entre el carboni que conté el grup hidroxil i un carboni veí que tengui un hidrogen. Habitualment es realitzen en tetrahidrofurà com a dissolvent. Es forma l'alquè més estable, seguint la regla de Zaitzev (enllaços dobles entre els carbonis amb el màxim de substituents).

Deshidrohalogenació[modifica]
L'eliminació d'un halur d'hidrogen condueix a la formació d'un alquè. L'hidrogen que s'elimina és el que està situat al carboni veí del que té enllaçat l'halogen. Aquest carboni s'anomena carboni β, per la qual cosa aquesta reacció també és coneguda com eliminació β. Per a dur a terme la reacció hom ha d'emprar bases fortes, com ara l'hidròxid de potassi dissolt en etanol o alcòxids de sodi[8]

Eliminació de Hofmann[modifica]
L'eliminació de Hofmann (també coneguda com a metilació exhaustiva o la «degradació de Hofmann») és el procés en el qual una amina reacciona per crear una amina terciària i un alquè per tractament amb iodur de metil en excés, seguit per tractament amb òxid d'argent(I), aigua, i calor.[8]

Eliminació de Cope[modifica]
L'eliminació de Cope és la reacció que es produeix quan s'escalfen òxids d'amines terciàries al voltant dels 150 °C. Es produeix un alquè i s'elimina una hidroxilamina. L'òxid es genera en una primera etapa per tractament de l'amina terciària amb peròxid d'hidrogen . A continuació el producte obtingut s'escalfa i s'obté l'alquè.[8]

Piròlisi d'èsters[modifica]
Si s'escalfen a una temperatura entre 200 °C i 500 °C els èsters que tenguin al manco un hidrogen unit al segons carboni del radical enllaçat a l'oxigen, s'obté un alquè i un àcid carboxílic.[8]

Reacció de Wittig[modifica]
La reacció de Wittig és una reacció química en la qual un aldehid o cetona reacciona amb un ilur de fòsfor (també anomenat fosforà) obtenint-se un alquè i òxid de trifenilfosfina com a subproducte.[9]
Vegeu també[modifica]
Referències[modifica]
- ↑ Senning, Alexander. The etymology of chemical names : tradition and convenience vs. rationality in chemical nomenclature, 2019. ISBN 3-11-061124-4.
- ↑ «Alkane Nomenclature». [Consulta: 6 abril 2021].
- ↑ 3,0 3,1 3,2 3,3 Unió Internacional de Química Pura i Aplicada. Comissió de Nomenclatura de Química Orgànica. Guia de la IUPAC per a la nomenclatura de compostos orgànics : recomanacions del 1993 (incloent-hi les revisions, tant publicades com no publicades fins ara, de l'edició del 1979 de la Nomenclature of organic chemistry), febrer del 2017. ISBN 978-84-9965-333-4.
- ↑ Bhasin, S. K.. Pharmaceutical Organic Chemistry.. New Delhi: Elsevier Health Sciences APAC, 2012. ISBN 978-81-312-3267-5.
- ↑ «olefina | enciclopèdia.cat». [Consulta: 5 abril 2021].
- ↑ 6,00 6,01 6,02 6,03 6,04 6,05 6,06 6,07 6,08 6,09 6,10 6,11 McMurry, John. Química orgánica. 8a ed. México: Cengage Learning, 2012. ISBN 607-481-789-8.
- ↑ Allinger, N.L.; i col. Química orgánica. 2. ed. Barcelona: Editorial Reverté, 1984. ISBN 84-291-7015-4.
- ↑ 8,0 8,1 8,2 8,3 Solomons, T. W. Graham. Química orgánica. 1. ed. Mexico: Limusa, 1979. ISBN 968-18-0982-3.
- ↑ Per un article de revisió sobre aquesta reacció vegeu: Maryanoff, B. E.; Reitz, A. B. Chem. Rev. 1989, 863-927. doi:10.1016/10.1021/cr00094a007
| A Wikimedia Commons hi ha contingut multimèdia relatiu a: Alquè |