Líquid iònic
Un líquid iònic (LI) és un fluid constituït exclusivament per ions, considerant-se així les sals amb una temperatura de fusió per sota del punt d'ebullició de l'aigua (100 °C al nivell del mar, ja que vària d'acord amb la pressió atmosfèrica) i que sovint són hidrolíticament estables. Aquestes substàncies són de vegades anomenades electròlits líquids, fusions iònics, fluids iònics, sals foses, sals líquides, o vasos iònics. [1][2][3]
La composició química general d'aquests materials és sorprenentment consistent, fins i tot encara que la composició específica i les propietats físiques i químiques varien tremendament. La majoria té una estructura composta per un catió orgànic i un anió inorgànic poliatòmic. A causa que hi ha molts i molt coneguts cations i anions, el nombre potencial de LI és enorme, de l'ordre de milions de combinacions possibles. Descobrir un nou tipus de líquid iònic és relativament fàcil, però determinar aplicacions dels líquids iònics requereix una inversió molt més substancial en la determinació de les seves propietats físiques i químiques.
Els primers LI inicialment van ser desenvolupats per ser usats com electròlit, encara que a causa de les seves propietats: una volatilitat pràcticament nul·la, amb una pressió de vapor gairebé zero, ja que estan composts completament d'ions; inflamabilitat menyspreable; un ampli rang de líquids, és a dir, una alta estabilitat tèrmica i un baix punt de fusió; i una miscibilitat controlada amb els compostos orgànics; aquest tipus de materials ha anat guanyant importància i un particular interès com un nou tipus no convencional de dissolvent (dissolvent verd), especialment per la seva nul·la volatilitat, que permet no considerar a aquestes substàncies com compostos orgànics volàtils (COV).
Estructura[modifica]
Un líquid iònic està format per ions molt asimètrics i voluminosos, per la qual cosa presenta forces atractives més febles que les sals iòniques convencionals.
En general, posseeixen una estructura composta per un catió orgànic, que conté un heteroàtom (N o P), associat a un anió mineral o orgànic d'elevada grandària, entre els cations més comuns es destaquen: [bmin]+(1-butil-3-metil-imidazoli), [hmim]+ (1-hexil-3-metil-imidazoli), [omim]+(1-octil-3-metil-imidazoli), [beim]+ (1-butil-3-etil-imidazoli), [emim]+ (1-etil-3-metil-imidazoli), etc.
 |
Entre els anions més usuals es troben: PF₆-(Hexafluorofosfat), BF₄-(Tetrafluoroborat), CF₃-COO-(Trifluoroacetat), CF₃-SOTA₃-(Trifluorosulfonat o Triflato), SbF₆-(Hexafluor Antimoniat), etc.
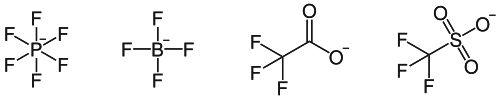 |
El tetrafluoroborat d'1-butil-3-metilimidazoli, el clorur d'1-butil-3-metilimidazoli i l'hexafluorofosfat 1-butil-3-metilimidazoli són alguns exemples de líquids iònics.
Propietats[modifica]
Entre les propietats més interessants dels líquids iònics es poden destacar:
- Baix punt de fusió (són líquids a temperatura ambient).
- Pressió de vapor molt baixa (no són volàtils).
- Alta estabilitat tèrmica que en molts casos supera els 300 °C, per sobre d'aquesta temperatura solen descompondre's.
- Alt calor específic.
- Alt poder dissolvent de diferents matèries orgàniques, inorgàniques i polimèriques, polars i no polars.
- Elevada estabilitat química.
- Posseeixen acidesa tipus Brønsted o Lewis i superacidesa.
- Elevada conductivitat iònica.
- Bones propietats electroquímiques.
- Elevada viscositat entre 10-500 cP.
- Elevada densitat.
- pH variable trobant-se LI àcids, neutres o bàsics.
- No inflamables.[4] Breu exposició (5 a 7 segons) amb una torxa de flama pot encendre alguns líquids iònics. La combustió completa és possible per a alguns líquids iònics.[5] No corrosius.
- Potents catalitzadors.
- Fàcilment reciclables.
- Incolors en estat pur.
Aplicacions industrials (exemples)[modifica]
Els líquids iònics (LI) poden considerar-se com a nous dissolvents a causa de les seves propietats: baixa inflamabilitat, baixa o nul·la volatilitat, estabilitat tèrmica i alta conductivitat iònica. Per aquesta raó, les seves principals aplicacions serien substituint als dissolvents orgànics convencionals en reaccions bifàsiques i en processos de separació
- Separació líquid - líquid
- Separació sòlid - líquid
- Separació d'ions metàl·lics
A més, es poden utilitzar en altres aplicacions com en l'extracció amb fluids supercrítics o en el desenvolupament de nous processos tecnològics i industrials.
Procés BASIL[modifica]
BASIL (Biphasic Acid Scavenging utilising Ionic Liquids) és un procés industrial desenvolupat per BASF per a la formació d'alcoxifenilfosfines mitjançant la següent reacció química:
En aquesta reacció es forma un líquid iònic immiscible que se separa de la barreja i pot tornar a utilitzar-se en el següent cicle del procés. Est és un dels més importants exemples de l'ús de líquids iònics a nivell industrial, en el qual es produeixen tones de producte, amb rendiments del 98%. Va rebre el premi ECN d'innovació l'any 2004.
Altres processos desenvolupats per BASF:
- Cloració d'alcohols reemplaçant el fosgen com a agent de cloració per àcid clorhídric (HCl). Aquest actua com a nucleòfil donant lloc a quatre compostos diferents, mentre que dissolt en un líquid iònic s'obté el producte clorat pur.
- Trencament de barreges azeotròpiques, que els líquids iònics poden actuar com a auxiliars millorant la separació, per exemple en barreges aigua-etanol i aigua-tetrahidrofurà.
Procés Difasol[modifica]
Es basa en la dimerització d'alquens, generalment propè i butè, a hexè i octè. És un procés molt important desenvolupat per Institut Français du Pétrole (IFP), utilitzant un líquid iònic com a dissolvent i un catalitzador de niquel. La reacció es duu a terme mitjançant un sistema bifàsic on els productes es queden en una segona fase i se separen fàcilment. El catalitzador queda dissolt en la fase líquid iònic.
Additius per a pintures[modifica]
Degussa, utilitza líquids iònics com a additius en la fabricació de noves pintures, amb l'objectiu de millorar l'acabat, l'aparença i les propietats d'assecat. Això permet la reducció de l'ús de substàncies orgàniques volàtils.
Una altra aplicació, en la qual Degussa investiga, és en l'ús de LI en bateries de liti com a electròlits.
Síntesi de fàrmacs[modifica]
Central Glass Company sintetitza intermedis farmacèutics mitjançant la reacció d'acoblament de Sonogashira. Utilitzen un líquid iònic com a mitjà de reacció substituint als dissolvents tradicionals com toluè o tetrahidrofurà.
Un altre procés és la desmetilació d'arileter per a la generació de fenols que es presenta a continuació:
Aquesta reacció ha estat desenvolupada per Eli Lilly, companyia farmacèutica, i portada a escala de planta pilot per produir aquests intermedis farmacèutics
Recuperació[modifica]
Des del punt de vista mediambiental així com econòmic, la recuperació de líquids iònics (LI) mitjançant la tecnologia de membrana (nanofiltració) és del tot interessant per tenir aquests compostos alt valor afegit en la indústria la qual els utilitzi, ser més beneficiós per al medi ambient i ser l'opció més còmoda, ja que és un equip que podem adquirir al mercat (però no un de tecnologia d'adsorció). Amb aquesta opció es recupera el líquid iònic i no es generen residus de carbó actiu. La nanofiltració, a més, presenta alts nivells de retenció sent el seu consum d'energia no gaire alt. Respecte a proves experimentals d'adsorció del LI sobre carbó actiu, s'ha vist que aquesta, es tracta d'una altra tècnica interessant de recuperació dels LI.
Toxicitat[modifica]
Els LI tenen diverses propietats per ser seleccionats com a candidats a dissolvents verds, perquè en utilitzar-los presenten beneficis per a l'ambient entre ells es destaca la disminució d'emissions atmosfèriques en eliminar perdudes de dissolvent per evaporació, i la reducció de residus a causa que aquests poden ser reutilitzats. Igualment, en eliminar l'etapa d'evaporació del dissolvent es redueix el consum energètic. També és possible el disseny de LI no tòxics i biodegradables mitjançant l'adequada selecció del catió i l'anió.
Encara que els LI eviten la contaminació atmosfèrica que originen els dissolvents tradicionals, la seva relativa solubilitat en fase aquosa pot causar problemes de contaminació de l'aigua i per tant problemes als éssers vius, no obstant això, per a un ús segur dels LI es fa necessari conèixer la seva toxicitat i biodegradabilitat.
Encara que les dades que es tenen no han estat determinats per a molts LI, la volatilitat pràcticament nul·la d'aquests redueix les potencials vies d'exposició, sent el contacte directe amb la pell i la ingestió pràcticament les úniques vies possibles. És adequat ressaltar que s'han realitzat diferents assajos i estudis per determinar la toxicitat i la biodegradabilitat dels LI, on es mostra que alguns d'aquests poden ser tòxics així com bastant inofensius i biodegradables, no obstant això, la majoria dels LI que s'han investigat són irritants i tenen una toxicitat comparable als dissolvents orgànics convencionals.
Toxicitat in vitro[modifica]
Aquests assajos han demostrat activitat inhibidora de l'acetilcolinesterasa; aquesta inhibició depèn de la longitud de la cadena alquílica del catió i poc de l'anió, la major activitat inhibidora es dona amb cadenes alquíliques llargues.
Els assajos in vitro solament donen indicacions del perill potencial, però no impliquen que hagi d'haver-hi un efecte sobre un organisme complet, per a això ha de comptar-se amb dades de transport (sobretot a través de membranes biològiques) i de bioacumulació.
Segons el coeficient de repartiment octanol/aigua (Kow) la solubilitat en octanol dels LI augmenta amb la longitud de la cadena alquílica del catió.
Toxicitat en microorganismes[modifica]
La toxicitat davant de microorganismes és molt notable en alguns casos i depèn de la longitud de la cadena alquílica (el que es relaciona amb el coeficient de repartiment). Els LI amb cations amb cadena alquílica llarga provoquen la pèrdua del flagel dels microorganismes que el posseeixen i igualment generen un efecte inhibitori en el creixement dels mateixos. L'efecte tòxic de LI vària molt amb el microorganisme utilitzat.
Toxicitat en cèl·lules[modifica]
En cèl·lules de l'epiteli la citotoxicitat dels LI que s'han assajat han mostrat que aquesta augmenta amb el temps d'exposició. En cèl·lules de carcinoma de còlon com HT-29 i CaCo-2, la citotoxicitat augmenta amb la longitud de la cadena alquílica del catió del LI, però també depèn de l'anió (per exemple l'anió hexafluorofosfat augmenta la toxicitat); encara que la influència de l'anió no és clara, sembla molt menor a la del catió.
En general, la citotoxicitat augmenta amb la longitud de la cadena alquílica del catió, arribant fins i tot a ser superior que la presentada pels dissolvents orgànics convencionals com: acetonitril, acetona, benzè, toluè, fluorobencè, metanol, àcid acètic, diclorometà i xilè.
Toxicitat en organismes[modifica]
Organismes com caragols d'aigua dolça, rates, peixos (peix zebra), exposats a alguns LI basats en cations imidazoli i pirimidina han presentat alteracions estructurals i bioquímiques, en general els LI han afectat el seu moviment, causant perdudes d'equilibri i una marcada tendència a romandre immòbils, a més han generat la disminució en el seu creixement en comparació amb els organismes testimoni. Igualment per a aquest cas la toxicitat augmenta també amb la longitud de la cadena alquílica del catió.
Un estudi realitzat utilitzant morritort (Lepidium sativum) determina que els LI a força de cations imidazoli generen una lleugera toxicitat a aquesta planta comestible, a causa d'una disminució en el seu creixement en ser comparat amb altres substàncies com el fenol i sulfat de zinc.
Referències[modifica]
- ↑ Thomas Welton «Room-Temperature Ionic Liquids». Chem. Rev., 99, 1999, pàg. 2071–2084. DOI: 10.1021/cr980032t. PMID: 11849019.
- ↑ F. Endres; S. Zein El Abedin «Air and water stable ionic liquids in physical chemistry». Phys. Chem. Chem. Phys., 8, 18, 2006, pàg. 2101–16. Bibcode: 2006PCCP....8.2101E. DOI: 10.1039/b600519p. PMID: 16751868.
- ↑ Freemantle, Michael. An Introduction to Ionic Liquids. Royal Society of Chemistry, 2009. ISBN 978-1-84755-161-0.
- ↑ Marcin Smiglak; W. Mathew Reichert; John D. Holbrey; John S. Wilkes; Luyi Sun; 7 «Combustible ionic liquids by design: is laboratory safety another ionic liquid myth?». Chemical Communications, 2006, 24, 2006, pàg. 2554–2556. DOI: 10.1039/b602086k. PMID: 16779475.
- ↑ ; Thomas Keicher; Volker Weiser; Horst Krause; Stefan Schlechtriem«Synthesis, Characterization and Combustion of Triazolium Based Salts» (pdf) p. 1–23, 10-07-2010. [Consulta: 2 març 2016].
Estudis relacionats[modifica]
- Evans-White, Lamberti, G., A,. Environ Toxicol Chem. 2009, 28:2, 418-426.
- Matzke, M., Stolte, S., Thiele, K., Juffernholz, T., Arning, J., Ranke, J., Urs Welz-Biermann, Bernd Jastorff., Green Chem., 2007, 9, 1198–1207.
- Plechkova, N.V., Seddon,K.R., Chem. Soc. Rev., 2008, 37, 123-150.
- Seki, S., Kobayashi, Y., Ohno, Y., Usami, A., Mita, Y., Watanabe, M., Terada, N., Chem. Comm., 2006, 544-545.
- Studzinka, S., Buszewski, B. Anal. Bioanal. Chem., 2009, 393:983-990.
- Torrecilla, J. S., García, J., Rojo, E., Rodríguez, F., J.Hazard Mater., 2008, doi:10.1016/j.jhazmat.2008.08.022
- Wasserscheid, P., Welton, T,. (2008). Ionic Liquids in Synthesis. Wiley-VCH. ISBN 978-3-527-31239-9. (anglès)
- Zhao, D., Liao, Y., Zhang, Z., Review. Clean 2007, 35 (1), 42 – 48.
- Fernández, J.F., Atalaya Solís, P., Virtual Pro 2013, 137, 13.
Enllaços externs[modifica]
- Procés Basil
- Difasol
- Toxicitat de LI
- Ionic liquids Merck Arxivat 2012-03-05 a Wayback Machine.


