Grafit
 Grafit de Letovice, República Txeca | |
| Fórmula química | C |
| Epònim | writing (en) |
| Classificació | |
| Categoria | Mineral |
| Nickel-Strunz 10a ed. | 01.CB.05a |
| Nickel-Strunz 9a ed. | 1.CB.05a |
| Nickel-Strunz 8a ed. | I/B.02 |
| Dana | 1.3.6.2 |
| Heys | 1.25 |
| Propietats | |
| Sistema cristal·lí | sistema hexagonal |
| Hàbit cristal·lí | tabular, de sis cares foliada, les masses granulars compactades |
| Grup espacial | grup espacial 194 |
| Massa molar | 12 Da |
| Color | negre acer, gris |
| Exfoliació | Perfecta |
| Fractura | escamosa; desigual quan no es fa en el sentit de l'exfoliació |
| Duresa | 1 a 2 |
| Lluïssor | Metàl·lica terrosa |
| Color de la ratlla | Negre acer - gris |
| Densitat | 2,09 a 2,23 g/cm³ |
| Més informació | |
| Estatus IMA | mineral heretat (G) |
| Símbol | Gr |
| Referències | [1] |
El grafit és un mineral de la classe dels elementals, i en la seua composició concreta intervé un element semimetàl·lic. Està format quasi exclusivament per àtoms de carboni, i es tracta de fet d'una de les formes al·lotròpiques en què es pot presentar el carboni elemental, juntament amb el diamant, el ful·lerè i altres, com el grafè. El grafit és la forma més estable del carboni en condicions estàndard (o a pressions i temperatures baixes), motiu pel qual se l'utilitza en termoquímica per a definir l'estat estàndard respecte del qual es mesura la calor de formació dels compostos del carboni. També és polimorf de la chaoïta i la lonsdaleïta. Rep el seu nom per Abraham Gottlob Werner l'any 1789, i el terme grafit deriva del grec γραφειν (graphein) que significa escriure. Es pot considerar el grafit com el carbó de màxim contingut en carboni, trobant-se per damunt de l'antracita, de manera que se'l pot anomenar meta-antracita, encara que normalment no se l'empra com a combustible degut al fet que és molt difícil encendre'l. També és possible entendre el grafit com una successió de capes de grafè superposades.
Característiques[modifica]
El grafit és de color negre amb lluentor metàl·lica, refractari i s'exfolia amb facilitat. En la direcció perpendicular a les capes presenta una conductivitat de l'electricitat baixa i que augmenta amb la temperatura, comportant-se doncs com un semiconductor. Al llarg de les capes la conductivitat és major i augmenta proporcionalment a la temperatura, comportant-se com un conductor semimetàl·lic. A diferència del diamant, encara que els dos estan formats per carboni, el grafit és molt tou i el diamant és el mineral més dur segons l'escala de Mohs.
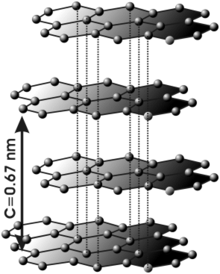
En el grafit els àtoms de carboni presenten hibridació sp2, això significa que forma tres enllaços covalents en el mateix pla a un angle de 120° (estructura hexagonal) i que un orbital Π perpendicular a aquest pla quedi lliure (aquests orbitals deslocalitzats són fonamentals per definir el comportament elèctric del grafit). L'enllaç covalent entre els àtoms d'una capa és extremadament fort, en canvi les unions entre les diferents capes es realitzen per forces de Van der Waals i les interaccions entre els orbitals Π, i són molt més febles. L'estructura laminar del grafit fa que sigui un material marcadament anisòtrop.
El grafit té funcions de ratllar altres minerals per a mesurar la seva duresa, ja que no és gaire fràgil. De manera artificial, el grafit es pot convertir en diamant augmentant la temperatura i la pressió, i utilitzant un catalitzador per augmentar la velocitat de la reacció.
El grafit és polimorf del diamant, la chaoïta i la lonsdaleïta. Té dos politips, el grafit-2H, que també cristal·litza en el sistema hexagonal, i el grafit-3R, que ho fa en el trigonal.[2][3] A més es coneixen dues varietats: la cliftonita, un grafit octaèdric pseudomòrfic després de kamacita, trobat en uns pocs meteorits de ferro, i el grafit urànic, un grafit que com el seu nom indica conté urani.
Formació[modifica]
El grafit es troba en roques metamòrfiques com a resultat de la reducció de compostos de carboni sedimentàris durant el metamorfisme. També es troba en roques ígnies i en els meteorits.[4] Els minerals associats amb el grafit inclouen quars, calcita, diferents miques i turmalina. En meteorits s'ha trobat amb troilita i minerals silicats. Els cristalls de grafit petits en ferro meteorític es coneixen com a cliftonita. El principal productor mundial de grafit és la Xina, seguit de l'Índia i el Brasil.
Usos[modifica]

- Barrejat amb una pasta serveix per fabricar llapis.
- Es pot trobar en maons, rajoles, gresols, etc.
- És un bon lubricant sòlid, ja que llisca fàcilment degut a la superposició de capes (de grafé) que constitueix la seua estructura reticular.
- S'utilitza en la fabricació de diverses peces en enginyeria, com pistons, juntes, volanderes, rodaments, etc.
- És conductor de l'electricitat i es fa servir per fabricar elèctrodes.
- També té altres aplicacions elèctriques, com per exemple les petits peces de carbó que en molts motors elèctrics possibiliten el contacte entre les fases elèctriques i el col·lector.
- És usat també per crear discos de grafit semblants als de discos vinil.
- Es troba també a molts tipus de reactors nuclears, en els quals s'empra de vegades grafit sintètic, ultrapur, com a matriu moderadora del flux neutrònic (fa anar més lents els neutrons). S'ha d'anar amb compte que el grafit usat als reactors no contingui materials absorbents de neutrons tals com el bor, amplament usat com a elèctrode iniciador als sistemes de deposició comercial de grafit; açò va causar el fracàs dels reactors nuclears alemanys de la Segona Guerra Mundial basats en grafit. Com els alemanys no foren capaços de determinar la naturalesa del problema, es varen vore forçats a usar com a substància moderadora aigua pesant, molt més cara. El grafit usat als reactors nuclears s'anomena freqüentment grafit nuclear.
- Amb el grafit es pot crear grafè, un material d'alta conductivitat elèctrica i tèrmica, potencial futur substitut del silici en la fabricació de xips.
Llapis[modifica]
La possibilitat de deixar marques en el paper i altres objectes donen el seu nom al grafit. El grafit del llapis, o plom negre, és més comunament una barreja de pols de grafit i argila; va ser inventat per Nicolas-Jacques Conté el 1795.[5] Plumbago és un terme més antic per al grafit natural utilitzat per dibuixar, tradicionalment com un tros de mineral sense l'embolcall de fusta. Avui en dia, els llapis són encara un mercat petit però significatiu per al grafit natural. Al voltant del 7% dels 1,1 milions de tones produïdes en 2011 es va emprar per fer llapis.[6]
Referències[modifica]
- ↑ «Graphite» (en anglès). Mindat. [Consulta: 1r agost 2014].
- ↑ «Graphite-2H» (en anglès). Mindat. [Consulta: 1r agost 2014].
- ↑ «Graphite-3R» (en anglès). Mindat. [Consulta: 1r agost 2014].
- ↑ «Graphite». A: Anthony, John W.; Bideaux, Richard A.; Bladh, Kenneth W. and Nichols, Monte C.. Handbook of Mineralogy (PDF). I (Elements, Sulfides, Sulfosalts). Mineralogical Society of America, 1990. ISBN 0962209708.
- ↑ «The History of the Pencil». University of Illinois at Urbana–Champaign. Arxivat de l'original el 2017-09-09. [Consulta: 1r agost 2014].
- ↑ «Electric Graphite Growing Demand From Electric Vehicles & Mobile Electronics». galaxycapitalcorp.com, 20-07-2011. Arxivat de l'original el 4 d’octubre 2013. [Consulta: 1 d’agost 2014].