Síndrome de Lesch-Nyhan
 | |
| Tipus | trastorn congènit del metabolisme purina-pirimidina, malaltia recessiva lligada al cromosoma X, deficiència en hipoxantina-guanina fosforibosil-transferasa i malaltia |
|---|---|
| Epònim | Michael Lesch i William Nyhan |
| Especialitat | endocrinologia |
| Clínica-tractament | |
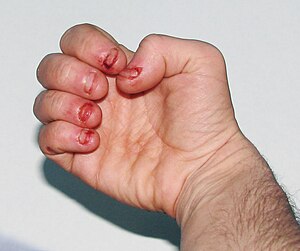
| Símptomes | autolesió |
Medicació | |
| Patogènia | |
| Associació genètica | HPRT1 (en) |
| Causat per | Hypoxanthine phosphoribosyltransferase 1 (en) |
| Classificació | |
| CIM-11 | 5C55.01 |
| CIM-10 | E79.1 |
| CIM-9 | 277.2 |
| Recursos externs | |
| Enciclopèdia Catalana | 0037017 |
| OMIM | 300322 |
| DiseasesDB | 7415 |
| MedlinePlus | 001655 |
| eMedicine | 1181356 |
| Patient UK | Lesch-Nyhan-Syndrome-(LNS) |
| MeSH | D007926 |
| GeneReviews | Panoramica |
| Orphanet | 510 |
| UMLS CUI | C0023374 |
| DOID | DOID:1919 |
La síndrome de Lesch-Nyhan (SLN), també coneguda com la síndrome de Nyhan, i gota juvenil és una malaltia hereditària poc freqüent causada per una deficiència total de l'enzim hipoxantina-guanina fosforibosiltranferasa (HGPRT), produïda per mutacions al gen HPRT. La manca de HGPRT provoca l'acumulació d'àcid úric als líquids corporals i dona lloc a hiperuricèmia i a hiperuricosúria.
Això condueix a problemes com la gota severa i problemes de ronyó, mal control dels músculs i endarreriment mental moderat. Aquestes complicacions normalment apareixen en el primer any de vida. Un tret cridaner del SLN és un comportament d'automutilació, caracteritzat per mossegades als dits i llavis i que comença al segon any de vida. Els símptomes neuronals inclouen ganyotes facials, retorciments involuntaris i moviments repetitius de braços i cames, semblants als d'aquells que pateixen la malaltia de Huntington. La causa directa d'anormalitats neurològiques encara no es coneix. Com que la manca d'HGPRT causa un mal ús de vitamina B₁₂, alguns nois poden desenvolupar anèmia megablàstica.
La malaltia s'associa al cromosoma X i l'al·lel causant és de tipus recessiu: la mare és normalment portadora del gen mutat i aquesta el passa als fills, encara que a un terç dels casos la mutació no és hereditària, sinó que sorgeix de nou. Aquells que pateixen la SLN pateixen de problemes físics i mentals al llarg de la seva vida i normalment són nois, rarament afecta a noies.
Els símptomes produïts per l'excés d'àcid úric (gota i símptomes renals) responen bé al tractament amb medicaments com l'al·lopurinol, el qual redueix els nivells d'àcid úric en sang. Els danys neuronals i el comportament auto mutilant no poden ser tractats. Malgrat no haver-hi cura, alguns pacients arriben a l'adultesa i amb tractaments experimentals s'ha arribat a alleujar alguns símptomes. La malaltia fou reconeguda per Michael Lesch i el seu mestre, el pediatre Bill Nyhan, que publicaren els seus descobriments el 1964. Hi ha també la síndrome de Kelley-Seegmiller, en qué només hi ha una deficiència parcial de l'enzim provocant símptomes més lleus, els afectats no pateixen d'autolesió, però és hereditària i es transmet de forma igual que el primer.
Signes i símptomes[modifica]
La SLN es caracteritza per tres grans trets: disfunció neurològica, alteracions cognitives i del comportament, automutilació inclosa, i sobreproducció d'àcid úric (hiperuricèmia). Els danys als ganglis basals provoquen que els malalts adoptin una característica postura d'esgrima. Alguns, a més, poden patir una anèmia macrocítica. Pràcticament tots els afectats són homes; els homes pateixen un creixement i una pubertat retardats. A més, la majoria desenvolupen una disminució de la mida dels testicles o atròfia testicular. D'altra banda, les dones, pateixen un augment dels risc de patir artritis gotosa però, normalment no són afectades per cap símptoma
Sobreproducció d'àcid úric[modifica]
Un dels primers símptomes de la malaltia és la presència de cristalls d'àcid úric, de la mida de grans de sorra, als bolquers dels infants afectats. La sobreproducció d'àcid úric pot conduir a la formació de cristalls o pedres d'àcid úric als ronyons, a l'urèter, o la bufeta urinària. Aquests cristalls poden dipositar-se a les articulacions podent arribar a produir artritis gotosa. La sobreproducció d'àcid úric es troba present des del naixement però, pot no ser reconeguda per proves rutinàries al laboratori. La concentració d'àcid úric és la majoria de cops normal, ja que l'excés de purines és eliminat des del començament a través de l'orina. Els cristalls normalment tenen un aspecte granulat de color taronja però, poden arribar a unir-se formant múltiples pedres petites o, fins i tot, grans pedres difícils d'expulsar. Les pedres, o càlculs, normalment causen hematúria (sang a l'orina) i augmenten el risc de patir infeccions al tracte urinari. Alguns afectats de LNS pateixen danys als ronyons deguts als càlculs renals. El símptoma més present de la malaltia són les pedres però, poden passar desapercebudes durant mesos o, fins i tot, anys.
Danys al sistema nerviós[modifica]
Durant el període anterior al naixement i poc temps després els individus que pateixen de LNS no pateixen cap anomalia. El fet més comú que es presenta és una disminució del to muscular (hipotonia) i endarreriment del desenvolupament, anomalies evidents entre els tres i sis mesos d'edat. Els afectats presenten retard a l'hora de seure i molts, fins i tot, mai caminen ni gategen. La manca de parla és també un fet comú associat a la síndrome de Lesch-Nyhan. La irritabilitat es fa notable més endavant, amb els primers signes de danys als sistema nerviós. Durant els primers anys, pateixen contraccions musculars involuntàries, pèrdua del control motor (distònia), moviments de retorciment (coreoacetosi) i un encorbament de la columna vertebral (opistotonus), causats pel desenvolupament extrapiramidal. A banda d'altres signes que inclouen espasmes, hiperreflèxia i reflex plantar (signe de Babinski). Aparentment s'observa una semblança als moviments deguts a una paràlisi cerebral, per aquest motiu, molts afectats són diagnosticats inicialment de paràlisi cerebral. El desordre motor és tan extens que la majoria dels malalts de LNS mai caminen, per tant, es veuen destinats a utilitzar una cadira de rodes de per vida.
Conducta d'autolesió[modifica]
Els afectats són retardats cognitivament i pateixen alteracions del comportament, aquests signes són presents entre els dos i tres anys. L'autolesió incontrolable, comunament associada a la síndrome de Lesch-Nyhan, apareix als tres anys. S'inicia amb mossos als llavis i la llengua; a mesura que la malaltia progressa, els malalts comencen a mossegar-se els dits i colpejar-se el cap. Durant períodes d'estrès la conducta d'autolesió pot incrementar. L'automutilació és una característica distintiva de l'afecció, afecta el 85% dels barons malalts. El retard cognitiu que pateixen la majoria dels afectats és difícil de distingir dels altres símptomes associats a la malaltia (alteracions del comportament i disfuncions del sistema motor). Moltes ocasions, la conducta és vista com una extensió psicològica de la tendència a l'autolesió: rebutgen plaers desitjats, responen l'amabilitat de forma freda o furiosa, no són capaços de contestar preguntes correctament (malgrat haver estudiat i desitjar aprovar), etc. El comportament compulsiu també inclou agressivitat, vòmits, escopinades i coprolàlia (grolleries involuntàries). Els desenvolupament d'aquest tipus de conducta es fa visible durant el primer any d'edat o la infància però, altres no apareixen fins a una edat avançada.
La SLN en dones[modifica]
Les dones portadores són generalment asimptomàtiques però, experimenten un increment en l'excreció d'àcid úric. Algunes poden desenvolupar els símptomes d'hiperuricèmia i patir gota durant els seus darrers anys. Les proves per ha detectar l'afecció són útils per a revelar la possibilitat de transmetre la malaltia a un fill mascle. Quan neix un fill que pateix de LNS la mare ha de fer una prova per a detectar la malaltia. En cas de no ser portadora, és a dir, tenir un resultat negatiu a la prova, indica que l'afecció del fill és resultat d'una mutació. Per tant, el risc de transmetre la malaltia als germans no augmenta. Les dones portadores del gen defectuós tenen un 50% de possibilitats de transmetre la malaltia als seus fills. Perquè una dona sigui afectada necessita tenir dues còpies del gen mutat, una d'elles hauria de ser heretada del seu pare, malalt de SLN. Els homes que pateixen d'aquesta malaltia no acostumen a tenir descendència degut als efectes de la síndrome. També és possible per a una dona heretar el cromosoma X del seu pare sense que aquest estigui afectat, degut a una mutació del gen HPRT. Baix aquestes circumstàncies una noia pot néixer amb la malaltia, encara que es coneixen alguns casos que això hagi ocorregut, és molt poc comú. La gran majoria de pacients amb la síndrome de Lesch-Nyhan són homes.
Diagnòstic[modifica]
Quan un individu afectat ha desenvolupat completament els tres elements clínics de la sobreproducció d'àcid úric, disfunció neurològica i disturbis cognitius i del comportament, és fàcil fer el diagnòstic de la SLN. Les dificultats d'aquest, però, són abundants durant els primers estadis de la malaltia, quan els trets principals encara no són visibles. Normalment la sospita ve donada quan l'endarreriment en el desenvolupament de l'individu ve acompanyat d'hiperuricèmia o pedres al ronyó (litiasi renal) junt amb sang a l'orina (hematúria),causades per càlculs formats per àcid úric. Però la major part de les vegades, la SLN s'identifica en manifestar-se el comportament auto mutilant, malgrat que aquest símptoma també sorgeixen altres malalties com ara retards mentals, autisme, síndrome de Rett, síndrome de Cornelia de Lange, síndrome de Tourette, síndrome de Riley-Day i neuropatia sensorial entre altres malalties psiquiàtriques. En alguns d'aquests trastorns sovint es perd teixit per les lesions auto produïdes. El fet de mossegar-se dit i llavis és un tret molt característic de la SLN; en altres síndromes el comportament consisteix més a copejar-se el cap i altres mutilacions menys específiques. Per tant, la SLN és clarament identificable quan s'ajunten la hiperuricèmia, la disfunció neuronal i el comportament auto mutilant.
Apropament al diagnòstic[modifica]
La proporció de sals d'àcid úric a l'orina en proporció a la creatinina és elevada i demostra la seva sobreproducció. La hiperuricèmia, malgrat estar present freqüentment, no és un símptoma en el qual podem confiar del tot per diagnosticar la malaltia. Si l'activitat de l'enzim HGPRT en cèl·lules de qualsevol teixit és menor de l'1,5% de l'activitat normal es pot confirmar la SLN. També l'estudi del gen HPRT podrien assegurar el diagnòstic i són particularment útils per posteriors proves a dones amb risc de ser portadores com, per exemple, familiars del sexe femení de l'afectat.
Proves[modifica]
L'ús de proves bioquímiques per detectar portadors exigeix molt treball i és utilitzada poques vegades. Les anàlisis bioquímiques dutes a terme al fol·licle pilós han donat lloc poques vegades a falsos positius i negatius. Seria apropiat fer créixer els limfòcits d'una dona baix sospita de ser portadora en tioguanina-6 (un anàleg de la purina), el qual només permet sobreviure a les cèl·lules amb deficiència de HGPRT. El test genètic molecular és el més efectiu conegut, ja que el gen HPRT1 és l'únic conegut associat a la SLN. Es disposen de seqüències d'ARNm que permeten detectar mutacions a l'esmentat gen d'homes afectats per la malaltia. Tècniques com la RT-PCR(reacció en cadena de la polimerasa), el complex genòmic PCR i l'anàlisi de seqüències (ADNc i ADN genòmic) són emprades pel diagnòstic de malalties genètiques. Si el test de RT-PCR mostra ADNc amb manca d'un exó sencer o de més d'un, aleshores es realitza la prova del complex genòmic PCR. Aquesta tècnica amplifica els nou exons del gen HPRT1 com vuit productes de la PCR. Si l'exó en qüestió està esborrat, la banda corresponent no hi serà al complex PCR. Malgrat això, en cas que l'exó sigui present, aquest està seqüenciat per identificar la mutació, causant així l'exclusió de l'exó del ADNc, és a dir, que no s'observarà aquella seqüència en el ADNc. Així, gràcies als buits en el ADNc, es pot saber que o bé hi ha una mutació o bé falta un exó al gen.
Genètica[modifica]

La síndrome de Lesch-Nyhan és deguda a una mutació del gen HPRT1. Aquest codifica l'enzim hipoxantina-guanina fosforibosiltransferasa (HPRT o HGPRT). L'HPRT està involucrat amb les rutes bioquímiques que el cos utilitza per a produir nucleòtids de purina, un dels components de l'ADN i l'ARN. Els defectes en aquest enzim produeixen una sobreproducció d'àcid úric. El gen HPRT es troba al cromosoma X, per tant, la LNS és una malaltia hereditària lligada al cromosoma X.
El pare d'un nen afectat no té per què ser portador de l'al·lel mutant per aquest motiu, no té per què patir la malaltia. Però, la mare d'un nen afectat ha de ser per força portadora, a més de tenir algun altre parent afectat a la línia materna. Si una dona és la primera de la família a tenir un fill amb la síndrome, la regla de Haldane prediu que amb un 66% de possibilitats la mare és portadora i amb un 33% que el fill ha patit una nova mutació genètica. De totes maneres, en aquest cas, la predicció de Haldane és incorrecta deguda a un major risc de patir una mutació per part del pare en comparació amb la mare. Una dona portadora té un 50% de possibilitats de transmetre la mutació del gen HPRT1 a cada embaràs. Els fills que heretin la mutació patiran la malaltia mentre que les filles que l'heretin seran portadores. Així que, una dona portadora, per cada embaràs té un 25% de possibilitats de tenir un fill afectat, un 25% de tenir una filla portadora i un 50% de tenir un fill o una filla normal (sense la mutació). Els homes amb la síndrome de Lesch-Nyhan no es reprodueixen degut a les característiques de la malaltia. De totes maneres, si un home amb un fenotip menys sever es reprodueix, totes les seves filles serien portadores però, cap dels seus fills estaria afectat.
Fisiopatologia[modifica]
Igual que en altre malalties lligades al cromosoma X, els homes són afectats per tenir només una còpia d'aquest. En la SLN el gen defectuós conté la informació per la formació de l'enzim (HGPRT), el qual participa en el reciclatge de les purines. Les dones portadores posseeixen un segon cromosoma X, el qual conté una còpia “normal” del gen HPRT1, prevenint així que la malaltia en desenvolupi malgrat que el risc de patir hiperuricèmia és alt.
Es coneixen un gran nombre de mutacions del HPRT. Aquelles que fan decréixer suaument la funció de l'enzim només un provoquen una tènue manifestació de la malaltia on s'identifica la sobreproducció de purines, susceptibilitat a la gota i la formació de càlculs renals mentre que aquelles on la inactivació de l'enzim és pràcticament total van associades a greus trastorns motors i cognitius.
Normalment els nucleòtids se sintetitzen de novo a partir d'aminoàcids i altres precursors, però una petita part es sintetitzen a partir de nucleòsids od e bases. Aquesta segona via es coneix com a via de reciclatge (salvage pathway). L'enzim HGPRT és l'enzim de síntesi de nucleòtids de purina per reciclatge de bases; dirigeix la hipoxantina i la guanina a la síntesi de nucleòtids. Un error en aquest enzim te dos resultats:
- Les bases puríniques no poden ser reutilitzats, i per tant són degradades. Això augmenta els nivells d'àcid úric, el producte de la degradació de les purines.
- S'estimula la síntesi de novo de nucleòtids de purina per la disminució en la via de reciclatge.
Abans no era clar si les anormalitats neurològiques de la SLN eren a causa de la neurotoxicitat de l'àcid úric o per una manca de nous nucleòtids de purina durant els passos essencials de la síntesi. Les mutacions genètiques que afecten els enzims de la síntesi de novo contribueixen a manifestar la malaltia, encara que aquestes mutacions són gairebé desconegudes. Encara no s'ha provat que l'àcid úric sigui la causa de la neurotoxicitat, però és la hipòtesi més emprada actualment.
Hi ha proves que suggereixen que una o més lesions en el nucli estriat depenent de dopamina poden ser la principal causa del dèficits neuronals, sobretot la disquinèsia i l'automutilació. La connexió entre les síntesi de la dopamina i de les purines és un nucleòtid, el guanosin trifosfat (GTP). El primer pas per sintetitzar dopamina és la GTP ciclohidrolasa i una falta d'aquesta biomolècula no permet la síntesi de dopamina, produint així una síndrome amb una neuropatologia similar a la SLN. El dèficit de HGPRT pot donar lloc a la manca de nucleòtids GTP, ja que la guanina és una base púrica, donant lloc d'aquesta manera a una deficiència de dopamina. Es creu en la teoria que l'àcid úric és un poderós agent reductor i probablement un important antioxidant humà que es troba en alta concentració a la sang. Per un altre costat, l'àcid úric també podria actuar com un prooxidant, és a dir, que afavoreix l'estrès oxidatiu. Per tant, es pensa que els radicals lliures, l'estrès oxidatiu i les espècies reactives de l'oxigen poden tenir algun paper en la neuropatologia de la SLN.
Malgrat això, es descarta que l'àcid úric tingui res a veure amb la neuropatologia per dos arguments de molta rellevància:
- La hiperuricèmia associada amb gota primària, la qual és causada per un mal funcionament renal que no permet una bona excreció d'àcid úric més que per una sobreproducció d'aquesta biomolècula, mai ha estat associada amb neuropatologies. Tampoc hi ha cap prova que nivells elevats d'àcid úric o la gota estiguin associats amb altres malalties o efectes atribuïts a l'activitat antioxidant o prooxidant d'aquesta.
- La hipouricèmia sorgeix en algunes malalties relacionades amb purines com la xantinúria. Malgrat tenir absència completa d'àcid úric en sang, els pacients de xantinúria no pateixen neuropatologia, malgrat que sí que tenen càlculs renals formats per acumulació de xantina insoluble.
En definitiva, les proves apunten que la patofisiologia de la SLN sorgeix d'una manca de nucleòtids més que d'un dany oxidatiu, cosa que té implicacions importants pel tractament. La “teràpia antioxidant” no sembla alleujar els símptomes de la SLN, mentre que la suplementació de nucleòtids gràcies a una medicació presa via oral mostra bons resultats, tal com s'explica a l'apartat següent.
Tractament[modifica]
El tractament per a la síndrome és, únicament, simptomàtic. La gota pot ser tractada amb al·lopurinol per a controlar l'excés d'àcid úric. Els càlculs renals es poden tractar amb litotrícia, una tècnica per a rompre pedres dels ronyons mitjançant ones de xoc o làser. No existeix cap tractament estàndard per als símptomes neurològics de la SLN. Alguns malalts poden alleugerir el mal amb fàrmacs com carbidopa/levodopa, diazepam, fenobarbital o haloperidol.
La sobreproducció d'àcid úric ha de ser controlada necessàriament per a reduir el risc de nefropatia, nefrolitiasis i artritis gotosa. L'al·lopurinol s'utilitza per a aturar la transformació d'oxopurines a àcid úric i així, prevenir el desenvolupament d'inflamacions a les articulacions (produïdes després de patir gota crònica), càlculs als ronyons i nefropatia, evitant mals als ronyons. L'al·lopurinol es pren oralment, amb una dosi típica entre 3-20mg/kg per dia. La dosi s'ajusta per disminuir la quantitat d'àcid úric a un nivell normal (<3mg/dL). Els individus més afectats són tractats amb al·lopurinol tota la seva vida.
No existeix cap medicació efectiva per a controlar les característiques motores produïdes pel sistema extrapiramidal. Encara que, els espasmes poden reduir administrant baclofen o benzodiazepines.
No s'ha descobert cap tractament efectiu per a controlar o evitar els aspectes del comportament que porta la malaltia associats. Fins i tot els nens tractats des del naixement amb al·lopurinol desenvolupen problemes neurològics i de comportament, encara sense haver tingut mai concentracions elevades d'àcid úric. L'autolesió i altres conductes es poden controlar millor amb una combinació d'intervencions mèdiques, físiques i de comportament. L'automutilació normalment es redueix mitjançant la restricció, normalment per part de les famílies. Per exemple, al 60% dels afectats els han hagut de treure les dents per a evitar l'autolesió. Com que l'estrès augmenta l'autolesió, la utilització de tècniques de repulsió (que normalment redueixen l'autolesió) realment l'augmenta amb malalts de SLN. Pràcticament tots els afectats necessiten restriccions per a prevenir les lesions i han de ser controlats més del 75% del temps. El temps de dedicació varia segons l'individu i la persona que el controla. Algunes famílies afegeixen que els malalts es troben més tranquils quan són controlats.
El Centre Mèdic i Educatiu de Matheny (The Matheny Medical and Educational Center) a Peapack, NJ, té nou pacients amb Lesch-Nyhan. Es tracta de la concentració més gran de malalts de la síndrome a una localitat i també és reconeguda com la primera en informació sobre la cura de la malaltia.
El tractament per als pacients que pateixen la síndrome, d'acord amb Gary E Eddey, director mèdic, ha d'incloure: l'ús encertat d'artefactes de protecció, la utilització de tècniques de conducta d'“ignorància selectiva” amb la re direcció d'activitats, i, ocasionalment, l'ús de medicaments.
Un article del 13 d'agost de 2007 a The New Yorker magazine, escrit per Richard Preston, tracta l'estimulació profunda del cervell com a possible tractament. S'ha dut a terme amb diversos pacients amb SLN pel Doctor Takaomi Taira a Tokio, i un grup a França encapçalat pel Doctor Philippe Coubes. Alguns pacients van experimentar una disminució amb els símptomes d'autolesió. La tècnica es va dur a terme per a tractar malalts de Parkinson fa 20 anys, segons Preston.[1] El tractament inclou cirurgia invasiva per a col·locar cables amb un corrent elèctric associat en una zona específica del cervell. Un avanç esperançador en el tractament dels aspectes neurològics i de conducta de la SNL va ser publicat a l'Octubre de 2006 al Journal of Inherited Metabolic Disease sobre una teràpia experimental donant S-adenosilmetionina (SAMe) oralment. Aquest medicament és un nucleòtid precursor que proporciona una purina llesta per a ser absorbida. Aquesta és transportada per la sang al cervells. L'administració de SAMe a adults amb la SNL va mostrar una millora en els aspectes de conducta i neurològics. El medicament no necessita prescripció i ha estat utilitzat per a la depressió però, el seu ús per a tractar la SLN només es pot consentir baix una estricta supervisió mèdica pels seus efectes secundaris.
La SAMe també s'ha utilitzat recentment per a tractar altres malalties associades als nucleòtids de purina, com la Síndrome d'Art, amb resultats esperançadors. Per tant la SAMe pot ser útil per a tractar afeccions dels nucleòtids de purina, incloent la Síndrome de Lesch-Nyhan.
Pronòstic[modifica]
Pels individus amb LNS sever l'esperança és pràcticament nul·la. La mort arriba normalment per un mal funcionament renal o complicacions amb l'hipotònia (flacidesa muscular) durant la primera o segona dècada de vida. Els malalts menys afectats tenen un millor pronòstic.
Història[modifica]
Michael Lesch era un estudiant de medicina a la Universitat John Hopkins i Bill Nyhan, pediatre i genetista bioquímic, era el seu mentor. Ambdós van identificar la síndrome de Lesch-Nyhan i la hiperuricèmia associada a ella en dos germans afectats de 4 i 8 anys. Lesch i Nyhan van publicar els seus descobriments el 1964. Tres anys després, les causes metabòliques van ser identificades per J. Edwin Seegmiller i els seus col·laboradors del NIH (National Institutes of Health, Institut Nacional de la Salut dels EUA).
Formes menys severes[modifica]
Pot aparèixer una afecció menys severa del LNS quan es produeix una manca parcial de l'HPRT. Aquesta deficiència és coneguda com la Síndrome de Kelley-Seegmiller (Kelley-Seegmiller Syndrome), la Síndrome de Lesch-Nyhan inclou un dèficit total de HPRT. Els símptomes generalment inclouen menys afeccions neurològiques però, la malaltia encara causa gota i càlculs renals.
Referències[modifica]
- ↑ Preston, Richard. «An Error in the Code» (en anglès). Annals of Medicine. The New Yorker magazine, 2007. Arxivat de l'original el 2012-09-05. [Consulta: 6 juny 2013].
Bibliografia[modifica]
|
|
Aquest article té bibliografia, però no se sap quina referència verifica cada part. Podeu millorar aquest article assignant cadascuna d'aquestes obres a frases o paràgrafs concrets. |
- James, William D.; Berger, Timothy G.; et al. (2006). Andrews' Diseases of the Skin: clinical Dermatology. Saunders Elsevier. ISBN 0-7216-2921-0.
- lesch_nyhan Arxivat 2007-06-08 a Wayback Machine. a NINDS.
- Hladnik U, Nyhan WL, Bertelli M (September 2008). "Variable expression of HPRT deficiency in 5 members of a family with the same mutation". Arch. Neurol. 65 (9): 1240–3. doi:10.1001/archneur.65.9.1240PMID: 18779430
- Lesch-Nyhan syndrome. Genetics Home Reference. Retrieved on 2007-05-24.
- Ole Daniel Enersen. Lesch-Nyhan syndrome at Who Named It?
- Lesch-Nyhan syndrome. NCBI Genes and disease. Retrieved on 2007-04-12
- Nyhan WL (2000). "Dopamine function in Lesch-Nyhan disease". Environ. Health Perspect. 108 Suppl 3: 409–11. doi:10.2307/3454529PMID: 10852837
- Proctor P, McGinness JE (1970). "Levodopa side-effects and the Lesch-Nyhan syndrome". Lancet 2 (7687): 1367. doi:10.1016/S0140-6736(70)92399-8PMID: 4098945
- Visser J, Smith D, Moy S, Breese G, Friedmann T, Rothstein J, Jinnah H (2002). "Oxidative stress and dopamine deficiency in a genetic mouse model of Lesch-Nyhan disease". Brain Res Dev Brain Res 133 (2): 127-39. doi:10.1016/S0165-3806(02)00280-8PMID: 11882343
- Breese GR, Knapp DJ, Criswell HE, Moy SS, Papadeas ST, Blake BL (2005). "The neonate-6-hydroxydopamine-lesioned rat: a model for clinical neuroscience and neurobiological principles". Brain Res. Brain Res. Rev. 48 (1): 57–73. doi:10.1016/j.brainresrev.2004.08.004PMID: 15708628
- Deutsch SI, Long KD, Rosse RB, Mastropaolo J, Eller J. (Jan-Feb 2005). "Hypothesized deficiency of guanine-based purines may contribute to abnormalities of neurodevelopment, neuromodulation, and neurotransmission in Lesch-Nyhan syndrome". Clin Neuropharmacol. 28 (1): 28–37. doi:10.1097/01.wnf.0000152043.36198.25 PMID: 15711436
- Proctor P (1972). "Electron-transfer factors in psychosis and dyskinesia". Physiol. Chem. Phys. 4 (4): 349–60. PMID: 4680784
- Bavaresco C, Chiarani F, Matté C, Wajner M, Netto C, de Souza Wyse A (2005). "Effect of hypoxanthine on Na+,K+-ATPase activity and some parameters of oxidative stress in rat striatum". Brain Res 1041 (2): 198–204. doi:10.1016/j.brainres.2005.02.012PMID: 15829228 Visser J, Smith D, Moy S, Breese G, Friedmann T, Rothstein J, Jinnah H (2002). "Oxidative stress and dopamine deficiency in a genetic mouse model of Lesch-Nyhan disease". Brain Res Dev Brain Res 133 (2): 127-39. doi:10.1016/S0165-3806(02)00280-8PMID: 11882343 Saugstad O, Marklund S (1988). "High activities of erythrocyte glutathione peroxidase in patients with the Lesch-Nyhan syndrome". Acta Med Scand 224 (3): 281–5 PMID: 3239456
- Kudo M, Moteki T, Sasaki T, Konno Y, Ujiie S, Onose A, Mizugaki M, Ishikawa M, Hiratsuka M. (March 2008). "Functional characterization of human xanthine oxidase allelic variants". Pharmacogenet Genomics. 18 (3): 243–51. doi:10.1097/FPC.0b013e3282f55e2ePMID: 18300946
- Preston, Richard (August 2007). "An Error in the Code". The New Yorker: p. 30.
- Glick N (October 2006). "Dramatic reduction in self-injury in Lesch-Nyhan disease following S-adenosylmethionine administration". J. Inherit. Metab. Dis. 29 (5): 687. doi:10.1007/s10545-006-0229-8PMID: 16906475
- de Brouwer AP, Williams KL, Duley JA, van Kuilenburg AB, Nabuurs SB, Egmont-Petersen M, Lugtenberg D, Zoetekouw L, Banning MJ, Roeffen M, Hamel BC, Weaving L, Ouvrier RA, Donald JA, Wevers RA, Christodoulou J, van Bokhoven H. (September 2007). "Arts syndrome is caused by loss-of-function mutations in PRPS1". Am. J. Hum. Genet. 81 (3): 507–18. doi:10.1086/520706 PMID: 17701896
- Nyhan WL (1997). "The recognition of Lesch-Nyhan syndrome as an inborn error of purine metabolism"[Enllaç no actiu]. J. Inherit. Metab. Dis. 20 (2): 171–8. doi:10.1023/A:1005348504512PMID: 9211189 http://www.kluweronline.com/art.pdf?issn=0141-8955&volume=20&page=171[Enllaç no actiu]
- Lesch M, Nyhan WL (1964). "A familial disorder of uric acid metabolism and central nervous system function". Am. J. Med. 36: 561–70 doi:10.1016/0002-9343(64)90104-4PMID: 14142409.
- Seegmiller JE, Rosenbloom FM, Kelley WN (1967). "Enzyme defect associated with a sex-linked human neurological disorder and excessive purine synthesis". Science (journal) 155 (770): 1682–4. PMID: 6020292. http://www.sciencemag.org/cgi/pmidlookup?view=long&pmid=6020292
- Augoustides-Savvopoulou P, Papachristou F, Fairbanks LD, Dimitrakopoulos K, Marinaki AM, Simmonds HA (2002). "Partial hypoxanthine-Guanine phosphoribosyltransferase deficiency as the unsuspected cause of renal disease spanning three generations: a cautionary tale". Pediatrics 109 (1): E17. doi:10.1542/peds.109.1.e17PMID: 11773585
Enllaços externs[modifica]
- CLIMB (Children Living with Inherited Metabolic Diseases)
- Lesch-Nyhan Syndrome Registry Arxivat 2004-12-02 a Wayback Machine.
- GeneReview/NIH/UW entry on Lesch-Nyhan Syndrome
- National Institute of Child Health and Human Development (NICHD)
- Philip Baker's Homepage Arxivat 2018-08-09 a Wayback Machine.
- Lesch-Nyhan Syndrome. Arxivat 2005-01-22 a Wayback Machine. The Cleveland clinic. Retrieved on 2007-04-12.
- Lesch-Nyhan Syndrome. Joseph F. Smith medical library. Retrieved from the internet archive, April 3 2005
