Zeolita
| Grup de minerals | |
 Cristall d'analcima, un mineral del grup de les zeolites | |
| Classificació | |
| Categoria | silicats |
| Propietats | |
| Més informació | |
| Símbol | Zeo |
| Referències | [1] |
Zeolita és el nom d'un grup de minerals que inclou una gran quantitat d'aluminosilicats (i en rares ocasions, beril·losilicats, zincosilicates i beril·lofosfats) formats per tetraedres AlO₄- i SiO₄ units pels vèrtexs d'oxigen i que contenen cations intercanviables (ions positius), tals com el Na+, K+, Ca2+, Mg2+ entre altres. Tenen una estructura micro-porosa. Aquests ions positius són normalment lligats de forma força feble (depenent de la seva càrrega) i permeten fàcilment l'intercanvi iònic.
A més d'intercanviar cations, les zeolites són capaces d'absorbir espècies no carregades, un exemple podria ser l'absorció de nitrogen als processos d'enriquiment d'oxigen de relativament baixa concentració per aplicació en hospitals. Algunes de les zeolites més comunes són: analcima, cabazita, heulandita, natrolita, phil·lipsita, i estilbita. Un exemple d'una fórmula mineral és: Na₂Al₂Si₃O10 · 2H₂O,[2] fórmula de la natrolita.
Història
[modifica]Es coneix que el seu ús es remunta als Asteques i Maies, qui les utilitzaven en tasques de construcció,[3] amb posterioritat, els romans de forma paral·lela en van millorar el seu ús, usant les zeolites per fabricar morters de calç amb putzolana, que s'utilitzava per fabricar ciments.
La descoberta de les seves propietats desintoxicants daten de 2300[4] anys enrere, els romans les utilitzaven per purificar les aigües a les conduccions o emmagatzematges d'aigua. Com a ús medicinal, data de 800 anys enrere per part de la Xina, Japó i Russia.
El seu nom, del grec, zein, "bullir", i lithos, "pedra", va ser establert en el segle xviii, l'any 1756 pel mineralogista suec Axel Fredrik Cronstedt, el qual observà, en escalfar ràpidament un mineral natural, que les pedres començaven a ballar tan bon punt l'aigua s'evaporava. Emprant els mots grecs que signifiquen "pedra que bull", va anomenar aquest material Zeolita.[5] Aquest fet s'explica perquè, en deshidratar-la per escalfament i deixar-la refredar, obtenim un sòlid amb molta tendència a absorbir l'aigua, que s'integra formant-hi ponts d'hidrogen, el que allibera molta energia, fins i tot per fer bullir la resta d'aigua.
Al 1858, Eichhorn va demostrar la reversibilitat de l'intercanvi iònic dels minerals zeolites, poc temps després, al 1862 Henri Étienne Sainte-Claire Deville va aconseguir la primera síntesi hidrotermal de zeolites, en concret la levinita.
Al 1930, poc després de l'aparició dels mètodes de difracció de raigs X en la identificació estructural dels minerals el 1927, l'estructura de la zeolita va ser determinada per Pauling i Taylor, donant origen a una gran quantitat d'estudis sobre aquesta (aplicacions, capacitat d'intercanvi...).
Zeolites naturals
[modifica]Les zeolites pertanyen al grup dels tectosilicats, que conformen prop del 75%[6] de l'escorça terrestre. No sorprèn per tant que siguin relativament senzilles de trobar en estat natural. Una de les mines de zeolites actualment més activa es troba a Pentalofos (nord de Grècia), una extracció a cel obert amb un contingut estimat de 6 MTm de zeolites, en la qual no fan falta ni tan sols explosius per fer l'extracció. Aquest fet esdevé en una extracció molt més segura i redueix el preu d'explotació. L'únic tractament que reben per poder ésser venudes és un trossejat de les roques mares i un tamisat (selecció segons la mida del gra) del resultat, ja que el seu contingut en zeolites excedeix el 75% en forma de clinoptilolita.[7]
No vol dir, però, que aquest en sigui l'únic jaciment. També existeixen dipòsits a regions tan diferenciades com Australia, Armenia o Nova Zelanda.[8]
Les zeolites es formen allà on les roques volcàniques i les capes de cendra reaccionen amb l'aigua subterrània alcalina. Les zeolites també cristal·litzen en ambients post-sedimentaris durant períodes que comprenen de milers a milions d'anys en jaciments marins superficials. Les zeolites de formació natural són rarament pures i es troben contaminades en diferents graus per altres metalls, quars o d'altres zeolites. Per aquest motiu, les zeolites de formació natural es troben excloses de moltes aplicacions comercials importants on la uniformitat i la puresa són essencials.
La sedimentació de cendres volcàniques arrossegades pel vent en forma d'autèntics núvols. En alguns casos, aquests núvols queien a llacs i en altres al propi sòl, on formaren un gruix de sediments on l'aigua hi penetrava. De la reacció entre l'aigua salada i aquesta deposició varen crear-se les zeolites naturals, d'estructura variable segons temperatura o zona de dipòsit,[9] ja sigui per composició de les cendres volcàniques com les substàncies dissoltes a l'aigua.
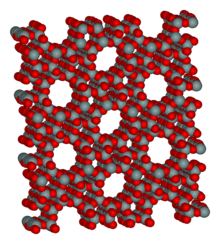
Fonts de zeolites
[modifica]L'extracció de zeolites naturals es fa mitjançant tècniques convencionals d'extracció en pedrera. En el processament, la mena es tritura, s'asseca i es mol. La mena molta pot ser classificada en funció de la mida de partícula. Del producte triturat se'n pot enretirar la part més fina quan cal un producte granular, i del material fi se'n poden fer productes de tipus pellet. Els productors també poden modificar les propietats de la zeolita o mesclar-ne els productes amb altres materials per millorar-ne les prestacions abans de vendre'ls.
Actualment la producció mundial de zeolita natural és d'uns 4 milions de tones l'any. D'aquesta quantitat, 2.6 milions de tones s'envien al mercat xinès per a ser emprats en la indústria del ciment. Europa, Austràlia i Àsia encapçalen el subministrament de la demanda mundial de zeolita natural. En comparació, als Estats Units d'Amèrica només se'n produeixen 57.400 tones mètriques (Font: U.S. Geological Survey, 2004), un 1% de la producció mundial.
Hi ha diferents tipus de zeolites sintètiques formades per un procés de cistal·lització lenta de gel de sílica-alúmina en presència de motlles alcalins i orgànics. Un dels processos més importants per portar a terme la síntesi de la zeolita és el processat sol-gel. Les propietats del producte depenen de la composició de la mescla de reacció, del pH del sistema, de la temperatura d'operació, del temps de 'cultiu' de prereacció, i del temps de reacció, així com dels motlles emprats.
Usos com a catalitzador
[modifica]Les zeolites són capaces de catalitzar un conjunt ample de reaccions molt selectives de les que en farem breu esment a continuació:
De provada eficàcia, les zeolites són capaces d'alquilar el toluè de forma selectiva, per formar xilens d'interès, normalment el p-xilè, en diferents proporcions segons el tipus de zeolita i condicions. En el cas citat, la zeolita ZSM-5 amb certes modificacions.
És un mètode d'alquilació relativament net, ja que l'únic residu que genera és aigua, ja que les zeolites, encara que es desactiva ràpidament, són recuperables i en cualsevol cas tampoc són, en principi, nocives pel medi ambient.
Tot i això, aquest procés no és totalment perfecte, sol presentar alguna reacció indesitjada, la més representativa de la qual és l'alquilació del toluè per donar etilbenzè:[11]
Un producte que, encara i ser útil (ja que es pot deshidrogenar a estirè, un producte molt útil per la síntesi de polímers), és costós i monetàriament car de separar de la mescla xilènica.
- Isomerització de xilens:
Com ja hem esmentat, no tots els xilens són igualment útils. El més demandat és el p-xilè, la producció mundial del qual és de 1,7·10^7 Tones per fer fibres de poliésters i 3,5·10^6 Tones per fer-ne envasos.[12]
Amb aquest procés s'aconsegueix obtenir el producte més útil (p-xilè) de la mescla de xilens provinents del cracking dels destil·lats del petroli, en un procés acoblat. Les zeolites són capaces de retenir amb més força l'o-xilè i el m-xilè, ja que, simplement per geometria, la seva integració dins els canals de la zeolita és molt menys afavorida.
- Catàlisi: Els processos ja descrits, a la indústria petroquímica[14] i algunes aplicacions més.
- Bateria tèrmica[15]
- Detergents i sals de rentavaixelles:[16][17] com a component per estovar (baixar el contingut en Ca2+ i Mg2+) de les aigües. Als rentavaixelles, capta la calç de l'aigua, culpable de l'emblanquinament de la cristalleria.
- Dessecadors:[18] La zeolita és capaç de captar aigua dins dels seus porus amb bastant avidesa, resultant en una disminució de la humitat ambient, també s'usa com a dessecant de casos[19]
- Producte per les mascotes i animals:També són capaces de captar els mals olors produïts per animals, i s'usa com a complement alimentari per la cura de la salut del bestiar.
- Captador de nutrients: En agricultura, els nitrats són uns nutrients que es filtren amb rapidesa a través de la terra, i això fa difícil per a les plantes captar-lo. Les zeolites són capaces de captar-los i alliberar-los gradualment, s'utilitzen actualment a l'agricultura.[20]
- Captació de contaminants: diòxid de sofre en gasos, amoníac en aigües...
- Purificació d'aire: Existeixen sistemes d'obtenció d'oxigen enriquit per aplicació en hospitals. Les zeolites capten el nitrogen i deixen un aire més oxigenat.
- Tractament residus radioactius: La capacitat complexativa de metalls pesants en la zeolita redueix l'activitat radioactiva dels àtoms emissors.[21] Van ser usades a Txernòbil, per tractar (amb clinoptilolita) les persones afectades.[22]
Impacte medioambiental
[modifica]Tot i que les zeolites no provoquen un impacte visible a la natura, si que poden presentar algunes inconveniències en ambients concrets. Per exemple, en aigües pobres en nutrients s'ha demostrat que les zeolites carregades amb sodi provoquen una inhibició del creixement de les algues, ja que capten els oligoelements essencials per aquestes en forma d'àtoms pesats com el coure o el manganès. D'igual manera, s'ha observat aquest efecte en plantes sensibles com Raphanus Sativus (el rave comú).
Tanmateix, aquest efecte es mitiga amb les zeolites carregades amb calci. Una part molt important de les zeolites s'usen per estovar les aigües, com ja hem dit, per tant les zeolites que s'abocaran estaran carregades amb ions dicarregats, que provoquen un efecte pràcticament irrisori.
Toxicologia
[modifica]No presenten riscos directes en la salut, de fet a la Xina s'usava com a medicina sense efectes aparents, per tant el seu consum, sempre que sigui convenientment triturada, és en principi segur. L'únic risc que comporta és que la seva mineria, sobretot la de l'erionita, provoca una pols semblant a l'asbest, que per inhalació podria provocar greus danys.[23]
Espècies minerals de zeolites
[modifica]El grup de les zeolites inclou:[1]
Referències
[modifica]- ↑ 1,0 1,1 «Zeolite Group» (en anglès). Mindat. [Consulta: 27 abril 2014].
- ↑ «Zeolite Group: Zeolite Group mineral information and data.». [Consulta: 25 maig 2017].
- ↑ Ibérica (en castellà), 1922.
- ↑ Castells, Xavier Elías. Residuos destinados a la fabricación de materiales densos: Reciclaje de residuos industriales (en castellà). Ediciones Díaz de Santos, 2012-10-10. ISBN 9788499693750.
- ↑ Jacobs, P. A.; Flanigen, E. M.; Jansen, J. C.; Bekkum, Herman van. Introduction to Zeolite Science and Practice (en anglès). Elsevier, 2001-06-26. ISBN 9780080534794.
- ↑ Inglezakis, Vassilis J.; Zorpas, Antonis A. Handbook of Natural Zeolites (en anglès). Bentham Science Publishers, 2012. ISBN 9781608052615.
- ↑ Scott, P. W.; Bristow, Colin Malcolm. Industrial Minerals and Extractive Industry Geology: Based on Papers Presented at the Combined 36th Forum on the Geology of Industrial Minerals and 11th Extractive Industry Geology Conference, Bath, England, 7th-12th May, 2000 (en anglès). Geological Society, 2002. ISBN 9781862390997.
- ↑ «Commission of Natural Zeolites» (en anglès).
- ↑ «ZEO Inc. – Zeolite Formation» (en anglès). [Consulta: 25 maig 2017].
- ↑ KAEDING, W «Selective alkylation of toluene with methanol to produce para-Xylene» (en anglès). Journal of Catalysis, 67, 1, pàg. 159–174. DOI: 10.1016/0021-9517(81)90269-4.
- ↑ Hu, Hualei; Lyu, Jinghui; Rui, Jiayao; Cen, Jie; Zhang, Qunfeng «The effect of Si/Al ratio on the catalytic performance of hierarchical porous ZSM-5 for catalyzing benzene alkylation with methanol» (en anglès). Catal. Sci. Technol., 6, 8, 20-04-2016, pàg. 2647–2652. DOI: 10.1039/c5cy01976a. ISSN: 2044-4761.
- ↑ «Química Orgánica Industrial». [Consulta: 28 maig 2017].
- ↑ «Zeolitas aplicaciones - Lenntech». [Consulta: 28 maig 2017].
- ↑ Antonio, Jose Santiago Pozo. Puesta en Marcha de Un Reactor Aerobio de Lecho Fluidizado Para la (en castellà). Lulu.com, 2011. ISBN 9781447851639.
- ↑ «Zeolith-Wärmespeicher: Funktion & Anwendungen [Bateries tèrmiques amb zeolites: funcionament i aplicacions]» (en alemany). energie-experten, 06-11-2020. [Consulta: 12 juliol 2022].
- ↑ «Sal del lavavajillas | Por que es tan eficaz | Finish». Arxivat de l'original el 2017-05-06. [Consulta: 28 maig 2017].
- ↑ «Zeolite and Water Purification - Zeolite Applications | Turkish Zeolites» (en anglès). Arxivat de l'original el 2017-07-25. [Consulta: 28 maig 2017].
- ↑ «Lavavajillas con zeolitas» (en espanyol europeu). [Consulta: 28 maig 2017].
- ↑ Pedro, Bosch Giral. La zeolita (en castellà). Fondo de Cultura Economica, 1988. ISBN 9786071603296.
- ↑ Portocarrero, Nicolas Obregón; Ortíz, Jaime Ernesto Díaz; Daza, Martha Constanza; Rodríguez, Héctor Fabio Aristizabal «Efecto de la aplicación de zeolita en la recuperación de nitrógeno y el rendimiento de maíz» (en castellà). Acta Agronómica, 65, 1, 01-01-2016, pàg. 24–30. DOI: 10.15446/acag.v65n1.47762. ISSN: 2323-0118.
- ↑ León, María Isabel Carretero; Rodríguez, Manuel Pozo. Mineralogía aplicada: salud y medio ambiente (en castellà). Editorial Paraninfo, 2007. ISBN 9788497324878.
- ↑ Cuns-Rial, Frank. Su Salud, Su Tesoro (en castellà). Lulu.com, 2015-07-09. ISBN 9781483428185.
- ↑ «Los minerales más peligrosos del mundo» (en castellà). Fieras de la Ingeniería, 06-05-2014. Arxivat de l'original el 2017-06-06 [Consulta: 28 maig 2017]. Arxivat 2017-06-06 a Wayback Machine.



