Activitat òptica

L'activitat òptica és la capacitat que presenten certes substàncies de fer girar el pla de vibració de la llum polaritzada plana que les travessa.
L'angle de rotació, α, és directament proporcional a la distància travessada per la llum, l; a la densitat, ρ, si és una substància pura; o a la concentració, c, d'aquesta substància quan es troba en dissolució. La constant de proporcionalitat, [α]tλ, depèn de la natura de la substància òpticament activa; de la temperatura, t; de la longitud d'ona de la llum, λ; i del dissolvent si la substància està en dissolució. Aquesta constant s'anomena rotació òptica específica o poder rotatori específic.[1] La fórmula que ho relaciona tot per a substàncies en dissolució és deguda al físic francès Jean-Baptiste Biot i s'anomena llei de Biot:
En el cas dels cristalls la constant és [α0]tλ i s'anomena rotació òptica o poder rotatori i l'angle de rotació només depèn de la longitud del camí recorregut l:
[α]tλ i [α0]tλ es consideren positius quan el pla de polarització de la llum gira en el mateix sentit que les busques d'un rellotge, negatiu en el cas contrari. Segons que tinguin poder rotatori positiu o negatiu, les substàncies són anomenades dextrogires o levogires.[2]
Història[modifica]
L'activitat òptica fou descoberta el 1811 pel científic francès Francesc Aragó en els cristalls de quars. El 1822, l'astrònom anglès John F.W. Herschel descobrí que els cristalls de quars es presenten en formes cristal·lines que són imatge especular l'una de l'altra, i no són superposables, això condueix a la desviació del pla de la llum polaritzada i diferent per a cada forma.[3] Després es descobrí el mateix fenomen en altres cristalls que també presentaven formes especulars diferents. Per tant aquesta activitat òptica dels cristalls és un fenomen a causa de la dissimetria del reticle cristal·lí i desapareix per fusió, evaporació o dissolució.
El 1815 el físic francès Jean-Baptiste Biot descobrí un altre tipus d'activitat òptica, estudiant dissolucions de sacarosa, càmfora i àcid tàrtric, que persisteix sigui quin sigui l'estat físic de la substància.[4] El químic francès Louis Pasteur quan estudiava l'àcid tàrtric descobrí que es presentava en dos tipus de cristalls, cristalls polièdrics que eren imatge especular l'un de l'altre i no superposables. Separà de forma molt laboriosa els dos tipus de cristalls amb un microscopi i unes pinces, i després es dissolgué en aigua. Comprovà que les dissolucions eren òpticament actives i que desviaven la llum en sentit oposat però en la mateixa magnitud.[5] El 1860 deduí que, per aquestes substàncies, la causa no podia ésser altra que una dissimetria en l'estructura de la mateixa molècula i, per això, s'anomena activitat òptica molecular. El 1874, Jacobus Henricus van 't Hoff i Joseph Achille Le Bel, independentment, proposaren que el fenomen de l'activitat òptica podia ser explicat a partir de la disposició dels enllaços del carboni orientats segons els vèrtexs d'un tetraedre regular. Les substàncies òpticament actives existeixen en dues formes (enantiòmers) de propietats físiques exactament idèntiques a tots els altres punts de vista, però que difereixen pel signe de llur activitat òptica. Giren el pla de vibració de la llum el mateix angle però en sentits oposats. Hom diu que aquestes substàncies presenten el fenomen de la isomeria òptica. L'estudi de l'activitat òptica, en posar de manifest aquesta isomeria i tot el que sobre l'estructura molecular pot deduir-se'n, ha estat una eina poderosa que ha contribuït eficaçment a l'avançament de la química.[1]

També el 1845 l'anglès Michael Faraday descobrí que un tros de vidre sotmès a un fort camp magnètic es convertia en òpticament actiu efecte Faraday. Posteriorment aquest efecte fou descobert en molts sòlids, líquids i gasos, essent en tots els casos l'angle de gir proporcional, no només al camí recorregut, sinó també a la intensitat del camp magnètic, com demostrà el físic francès Marcel Émile Verdet.[6]
Teoria[modifica]
La radiació electromagnètica està constituïda per ones transversals on vibren un camp elèctric i un camp magnètic perpendiculars. Aquests camps produeixen en les molècules de les substàncies òpticament actives un moviment helicoidal dels electrons dels seus àtoms. Aquest moviment dels electrons és oscil·lant en consonància amb l'ona electromagnètica. Com que els electrons oscil·len, per la llei de Faraday-Henry emeten radiació electromagnètica, que s'anomena radiació dispersada. Aquesta radiació es pot demostrar que està en fase amb la radiació incident, però no oscil·la en els mateixos plans que la radiació incident. A la sortida de la substància òpticament activa emergeixen dues radiacions, la incident i la dispersada, que es combinen i, per això no tenen la mateixa direcció d'oscil·lació que la radiació incident, produint una rotació del pla de polarització.[7]
Activitat òptica molecular[modifica]
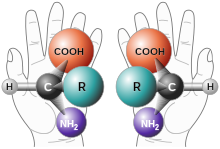
L'existència de l'activitat òptica pot ser explicada qualitativament de manera satisfactòria a partir de les diferències dels isòmers òptics, composts que presenten un o més carbonis asimètrics, és a dir substituïts per quatre substituents diferents. En aquests composts apareixen enantiòmers, que són imatge especular l'un de l'altre, i que només es diferencien pel desviament del pla de vibració de la llum polaritzada. L'angle de desviament és exactament el mateix, però cada isòmer òptic el desvia en sentit oposat a l'altre. Una mescla equimolecular d'ambdós isòmers, mescla racèmica, no desvia el pla de vibració, ja que els efectes de cada isòmer es compensen.
Rotació òptica específica[modifica]
Per a les dissolucions de concentració c (g per ml de solució) en una substància activa (a una temperatura t i per a una certa longitud d'ona de la llum, λ) és anomenada rotació òptica específica o poder rotatori específic [α]tλ el quocient:
on:
- α és l'angle de rotació (en graus sexagesimals i fraccions decimals de grau),
- l és el pas òptic, la llargada del camí que recorre la llum dins la dissolució (en dm).
Les unitats, que no s'especifiquen habitualment, són:
Si es tracta d'un líquid pur, se substitueix la concentració c per la densitat ρ (en g per ml):
Hom usa la notació [α]tD per a indicar que λ és la longitud d'ona de la línia D del sodi, és a dir, 5 839 Å. Malauradament la rotació específica d'una substància varia amb la naturalesa del dissolvent. Per consideracions de solubilitat, no és possible establir cap dissolvent de referència. Fins i tot, la rotació específica del dissolvent pot no ser completament independent de la concentració, si bé la variació en una dissolució diluïda és molt petita. Per aquests motius s'indica el tipus de dissolvent i la concentració. La variació de la rotació específica amb la temperatura és aproximadament lineal, però el coeficient de temperatura difereix àmpliament d'una substància a una altra.
| Poder rotatori específic d'alguns glúcids a 20 °C, dissolts en aigua | |||||||||
| Glúcid | Sacarosa | Lactosa | Maltosa | Midó | D-Ribosa | D-Glucosa | D-Fructosa | D-Galactosa | |
|---|---|---|---|---|---|---|---|---|---|
| [α]20D | + 66,5 | + 52,4 | + 138,5 | + 196,0 | - 19,5 | + 52,5 | – 92,0 | + 81,5 | |

L'activitat òptica molecular és mesurada, a l'estat líquid o en solució, amb els aparells anomenats polarímetres. La tècnica emprada en aquestes determinacions s'anomena polarimetria.
Rotació òptica molecular[modifica]
El producte de [α]tλ per la massa molecular M de la substància activa s'anomena rotació òptica molecular o poder rotatori molecular:
Referències[modifica]
- ↑ 1,0 1,1 «Activitat òptica». Gran Enciclopèdia Catalana. Barcelona: Grup Enciclopèdia Catalana.
- ↑ Fernández, J; Pujal, M. Iniciación a la física,. Barcelona: Reverte, 1992. ISBN 9788429142730.
- ↑ Rodríguez, J; Virgós, J.M. Fundamentos de óptica ondulatoria. Oviedo: Universidad de Oviedo, 1998. ISBN 9788483171172.
- ↑ Font, J. Els Premis Nobel de l'any 2001: cicle de conferències. Barcelona: Institut d'Estudis Catalans, 2002. ISBN 9788472836556.
- ↑ Weininger, S.J; Stermitz, F.R. Química orgánica. Barcelona: Reverté, 1988. ISBN 9788429175271.
- ↑ Catalá, J. Física, 1979. ISBN 84-400-5184-0.
- ↑ Alonso, M; Finn, E.J. Física. Campos y ondas. II. México: Fondo Educativo Interamericano, 1967. ISBN 968-6630-02-3.

![{\displaystyle \alpha =\left[\alpha \right]_{\lambda }^{t}\cdot l\cdot c}](https://wikimedia.org/api/rest_v1/media/math/render/svg/adf8d0e52f8b929f9d52615865842fa05dffda0c)
![{\displaystyle \alpha =\left[\alpha _{0}\right]_{\lambda }^{t}\cdot l}](https://wikimedia.org/api/rest_v1/media/math/render/svg/eac1e584f74f677a3c75621003e8c009fc1c096b)


![{\displaystyle \left[\alpha \right]_{\lambda }^{t}={\frac {\alpha }{l\cdot c}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/5be75364f44418aa8d91066d2bdadfa7915663bb)

![{\displaystyle \left[\alpha \right]_{\lambda }^{t}={\frac {\alpha }{l\cdot \rho }}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/7d7ed6abeb624c5b8179dedf91d48608fce4146d)
![{\displaystyle \left[M\right]_{\lambda }^{t}={\frac {M\cdot \left[\alpha \right]}{100}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/3786979aea4c2d3090ab939d41f7aa639c973591)