Cristal·lització


La cristal·lització és la formació d'un cristall. Es pot donar en un medi natural o de manera sintètica. És el procés de formació de cristalls sòlids que precipiten des d'una solució, una substància fosa o, més rarament, dipositada directament des d'un gas.[1] La cristal·lització també és una tècnica de separació sòlid-líquid, en la qual succeeix que la massa es transfereix d'un solut, des d'una solució líquida, a una fase cristal·lina sòlida pura. En enginyeria química, la cristal·lització passa dins un cristal·litzador. La cristal·lització és, per tant, un aspecte de la precipitació química obtinguda amb la variació de les condicions de solubilitat del solut en el solvent, en contrast amb la precipitació química deguda a una reacció química.
La cristal·lització s'empra amb força freqüència en química per purificar una substància sòlida.[2]
Història
[modifica]En època prehistòrica, ja s'utilitzava la sal comuna cristal·litzada obtinguda, per exemple, de l'aigua de mar dipositada en les esquerdes de les roques i assecada pel sol; el mateix principi encara es fa servir en les salines marines i en corrents salats d'aigua.
En temps més recents, es produeixen mitjançant la cristal·lització també de productes com la sacarosa, el sulfat de sodi i la urea, entre molts d'altres.
Procés
[modifica]El procés de la cristal·lització té dues etapes principals, la nucleació i el creixement del cristall.
En la nucleació, les molècules del solut que es dispersen en el solvent comencen a fer agregats a escala nanomètrica i en formen el nucli.
En el creixement del cristall, el nucli continua creixent i l'agregat aconsegueix arribar a la mida crítica. La supersaturació és la força conductora de la cristal·lització.
Molts compostos tenen la capacitat de cristal·litzar amb diferents estructures cristal·lines, fenomen que rep el nom de polimorfisme. Cada polimorf mostra diferents propietats físiques, com la taxa de dissolució, forma, punt de fusió, etc. Per això, el polimorfisme és de gran importància en la fabricació industrial de productes cristal·lins.
Cristal·lització natural
[modifica]

Hi ha molts exemples de processos naturals que impliquen la cristal·lització. A escala geològica alguns exemples són:
- Formació natural de cristalls en minerals;
- Formació dels anells en les estalactites i estalagmites.
Un exemple de cristal·lització natural és la de la sal marina en els llocs relativament càlids del món. Aquest procés natural s'utilitza en algunes zones costaneres o llacs per a l'obtenció de la sal comuna.
En temps més curts s'inclou:
- Els flocs de la neu;
- La cristal·lització de la mel (gairebé tots els tipus de mel poden cristal·litzar).
Mètodes artificials
[modifica]Per a la cristal·lització des d'una solució, aquesta ha d'estar sobresaturada, cosa que vol dir que la solució ha de contenir més molècules o ions dissolts dels que podria contenir sota l'equilibri (solució saturada). Això es pot aconseguir per diversos mètodes, entre els quals hi ha el d'evaporar el solvent. La cristal·lització esfèrica té certs avantatges (com el de biodisponibilitat) en la formulació de medicaments farmacèutics.
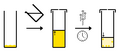
Al laboratori, la cristal·lització és un procés que consisteix a fer que el sòlid dissolt es vagi dipositant lentament, bé sigui per l'evaporació del dissolvent, o bé per la disminució de la seva solubilitat amb el refredament de la solució. El sòlid no dissolt apareix en forma de cristalls al fons i a les parets del recipient.
La cristal·lització al laboratori té com a objectiu purificar les diverses substàncies que es poden trobar en una dissolució. Si una solució que conté un solut acompanyat d'impureses es concentra per evaporació, les impureses solubles no arriben a formar, en general, una solució saturada, ja que es troben en quantitats petites, per la qual cosa els cristalls que s'obtenen són pràcticament de la substància que es vol purificar. Podem reduir aquestes impureses amb unes recristal·litzacions successives.
Aplicacions
[modifica]Hi ha dos grups principals d'aplicacions per a la cristal·lització artificial: producció de cristalls i la purificació.
- Producció de cristalls, com els cristalls macroscòpics que poden ser d'enllaç iònic o d'enllaç covalent i els cristalls petits de la mida de la pols o la sorra utilitzats en la indústria química i en bioquímica; la recristal·lització es fa servir per a determinar l'estructura de moltes molècules.
De forma massiva, es fa servir la cristal·lització en la producció de sal comuna, els cristalls de silici, l'extracció de la sacarosa de la remolatxa i en el refinament del sucre.
- Purificació: es fa servir per a millorar o verificar l'obtenció de substàncies molt pures, ja que la cristal·lització separa un producte, sovint, en una forma extremadament pura.
Recristal·lització
[modifica]Es repeteix el procés de cristal·lització en una dissolució en què ja s'havia fet aquest procés. Les aigües que queden encara contenen solut dissolt que es pot cristal·litzar. Per a un procés de cristal·lització més ràpid, cal aplicar un nucli de cristal·lització.
Referències
[modifica]- ↑ «Cristal·lització». Gran Enciclopèdia Catalana. Barcelona: Grup Enciclopèdia Catalana.
- ↑ «Universidad de Burgos». Arxivat de l'original el 23 d'octubre de 2014. [Consulta: 18 octubre 2015].
Vegeu també
[modifica]Bibliografia
[modifica]- A. Mersmann, Crystallization Technology Handbook (2001) CRC; 2nd ed. ISBN 0-8247-0528-9.
- Tine Arkenbout-de Vroome, Melt Crystallization Technology (1995) CRC ISBN 1-56676-181-6.
- DTB Crystallizer Arxivat 2011-12-28 a Wayback Machine..
- Oslo Type Crystallizer.
- "Small Molecule Crystallization" Arxivat 2016-03-03 a Wayback Machine. (PDF) at Illinois Institute of Technology website.
- Glynn P.D. and Reardon E.J. (1990) "Solid-solution aqueous-solution equilibria: thermodynamic theory and representation". Amer. J. Sci. 290, 164–201.
- Geankoplis, C.J. (2003) "Transport Processes and Separation Process Principles". 4th Ed. Prentice-Hall Inc.
- Stanley SJ. (2006) Tomographic imaging during reactive precipitation: mixing with chemical reaction, Chemical Engineering Science, 61 (23), pp 7850–7863.
- Nocent M, Bertocchi L, Espitalier F. & al. (2001) "Definition of a solvent system for spherical crystallization of salbutamol sulfate by quasi-emulsion solvent diffusion (QESD) method", Journal of Pharmaceutical Sciences, 90, 10, 1620–1627.