Mucor
 Mucor mucedo. | |
| Taxonomia | |
|---|---|
| Super-regne | Eukaryota |
| Regne | Fungi |
| Fílum | Mucormycota |
| Ordre | Mucorales |
| Família | Mucoraceae |
| Gènere | Mucor L., 1753 |
| Tipus taxonòmic | Mucor mucedo |
Mucor spp. és un gènere de fongs dins la família Mucoraceae, el qual compta amb unes 50 tàxons coneguts. És àmpliament distribuït pel sòl, tot i que també el trobem a l'aire o a la superfície de plantes i fruites. La majoria d'espècies són mesòfiles (poden créixer en un rang de 10-40 °C, amb un creixement òptim a 20-35 °C), encara que algunes en poden créixer fins als 60 °C (Mucor miehei i Mucor pusillus).[1] Algunes espècies (com Mucor dimorphosporus) han estat responsables de grans pèrdues econòmiques per l'alliberament de micotoxines, tals com l'anaflatoxina, a la superfície de productes gastronòmics de botigues i supermercats.[2] És també un agent causant de la mucormicosi, una malaltia rara però perillosa.[1]
Taxonomia
[modifica]Tot i la seva importància clínica i industrial, la taxonomia de l'ordre Mucorales i per tant del gènere Mucor està relativament poc estudiada, i és possible que rebi canvis significatius a mesura que apareguin noves investigacions. Anteriorment Mucor estava comprés en la divisió Zigomicota, avui considerada polifilètica[3] i en desús. Ha sigut dividit en dos fílums, Mucoromicota i Zoopagomycota.[4] El gènere Mucor, en classificacions recents, és considerat del regne fongs, fílum Mucoromicota, sub-fílum Mucoromicotines, ordre Mucorales, família Mucoraceae, i gènere Mucor.[5][4]
Hi ha, també, nombroses proves que el gènere Mucor i la família Mucoraceae són també polifilètics, de manera que és possible que rebin canvis en la seva taxonomia.[5]
Característiques morfològiques
[modifica]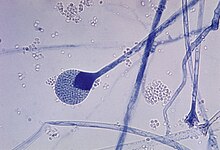
En un medi de cultiu sòlid, les colònies del gènere Mucor creixen amb una morfologia filamentosa. Creixen ràpidament i tenen un aspecte de floridura blanca entre esponjosa i cotonosa, que pot tenir alguns centímetres d'altura. A mesura que es desenvolupa l'esporangi (organ reproductor del fong), la floridura pren un color més grisós o marronós.[1][6] Si creix en un medi líquid en anaerobiosi, adopta un estat de llevat o rent però retorna a l'estat filamentós en presència d'oxigen. La capacitat d'alternar entre els dos estats, floridura i rent, s'anomena dimorfisme fungic.[1]
Els esporangiòfors (micelis que suporten els esporangis) poden ser simples o ramificats. Tenen una columnel·la (part suportada per l'estípit i que manté les espòres fins que es dispersin) que culmina en un gran esporangi globós on hi ha un gran nombre d'espores. Un cop s'ha dispersat, en l'esporangiòfor pot quedar un collaret que és de les restes de la paret de l'esporangi. Els esporangiòfors són hialins, grisos o marrons.[1][6]
Creixement
[modifica]Cicle cel·lular
[modifica]En la seva forma miceliana, el miceli és gruixut, cenocític (multinuclear) i molt ramificat. Les branques de la hifa es van comprimint fins a arribar a una punta fina. A mesura que creix el fong, poden aparèixer septes en les hifes, que separen parts especialitzades del miceli com clamidòspores.[1] Presenten autotropisme negatiu: les hifes s'eviten per no tocar-se entre elles i competir pels recursos. Els mecanismes d'aquest procés poden ser la falta d'oxigen, alta presència de CO₂, o algun altre metabòlit secundari no identificat.[7]
Reproducció asexual
[modifica]La reproducció asexual es dona per esporangiòspores. Trobem múltiples esporangiòspores en un esporangi globulat, que es troba en un esporangiòfor simple o ramificat. Els esporangis són fototròpics positius i poden detectar la gravetat, per tant, poden modificar el seu creixement per créixer cap amunt i alliberar les espores en l'aire lliure.[1]
Reproducció sexual
[modifica]
La reproducció sexual és per la conjugació de gametangis que forma zigòspores. Generalment són heterotal·lics: són necessaris dos individus diferenciats i separats però compatibles per reproduir-se. El procés està regulat per una hormona anomenada àcid trisporic, però no la sintetitza completament un sol individu, sinó que cada individu produeix diferents precursors metabòlics. Si dos individus es troben, intercanvien els precursors metabòlics i, si són compatibles, produiran àcid trisporic i es podran reproduir sexualment.[1][7]
L'àcid trisporic induirà la formació d'unes estructures reproductives en les puntes de les hifes, els gametangis, que entraran en contacte amb els gametangis de l'altre individu. A dintre de cada gametangi hi ha els nuclis haploides separats per un septe. El septe s'hidrolitza i es dona una plasmogàmia, fusió dels citoplasmes; i una cariogàmia, fusió dels nuclis haploides, el que dona un zigot diploide multinuclear.[1]
El zigot realitzarà la meiosi i al seu voltant es generarà l'estructura de zigòspora molt rica en esporopol·lenina. En algunes circumstàncies, els fongs del gènere Mucor poden desenvolupar un esporangi similar al vist a la reproducció asexual. Quan les circumstàncies siguin favorables, les espores s'alliberaran i formaran nous individus.[1]

Aïllament i cultiu
[modifica]Depenent del l'àmbit en el que volguem cultivar o detectar la presència d'una espècie de Mucor s'utilitzarà un tipus de cultiu o un altre. Per exemple en diferents articles d'estudi de la presència d'espècies de Mucor en aliments s'ha utilitzat agar dextrosa de patata. Aquest medi té antibiotics per inhibir el creixement de bacteris i és àcid.[8]
En l'àmbit clínic normalment s'intenta aïllar el fong en un medi de cultiu en casos sospitosos de mucormicosis, per tal de realitzar un diagnòstic i d'identificar l'agent patogen. El cultiu recomanat és el Agar Sabouraud.[9] La incubació es realitza en una temperatura d'entre 25 °C i 30 °C durant un període 3 a 5 dies,[10] tot i que es recomana mantenir el cultiu fins a 4 setmanes.[9]
La identificació es realitza de forma visual, o si hi ha dificultats, en el microscopi òptic.[9]
També existeixen noves tècniques basades en mètodes moleculars com PCR o mètodes de detecció immunològica.[9]
Nínxol ecològic
[modifica]Les espècies de Mucor són molt ubiqües en la natura, es troben en ambients molt diversos. S'han trobat espècies sapròfites (s'alimenten de matèria orgànica morta o que prové d'altres organismes) i espècies oportunistes d'animals (que poden causar malalties a animals ja afectats per altres patologies).[5] Poden utilitzar monosacàrids de la matèria orgànica en descomposició.[11] No s'han observat espècies de Mucor que facin simbiosi en plantes, encara que això és molt comú en altres gèneres de l'ordre Mucormycotina.[5]
Tot i que es poden trobar en molts substrats diferents prefereixen ambients humits amb una alta activitat hídrica. Les espores d'aquest grup tenen una gran capacitat d'absorció d'aigua i poden adherir-se a diversos substrats. Es dispersen per aire humit i quan arriben a un substrat favorable (on troben l'aliment necessari per créixer) germinen ràpidament. “Les seves condicions de creixement òptimes es troben a 20-35 °C, pH de 5.0-6.0, humitat relativa de 90-95% i activitat hídrica major a 0.95”.[5] A més a més, algunes espècies són termotolerants (com per exemple les espècies patògenes d'humans). Encara que aquestes són les condicions de creixement òptimes els trobem en un rang ecològic més ampli, ja que tenen enzims que poden degradar matèria orgànica en diferents nínxols ecològics (els quals poden ser aprofitats a la indústria). [5]
Utilitats i problemes a la indústria
[modifica]Encara que hi ha diversos efectes negatius del gènere Mucor tant en animals, humans i en la indústria alimentaria, també poden ser beneficiosos en diferents àmbits com el biotecnològic, la indústria alimentaria o la indústria dels biocombustibles. [5]
Indústria alimentaria
[modifica]Beneficis
[modifica]Aquest fong és molt utilitzat en diverses branques de la indústria alimentaria. És utilitzat en la producció d'aliments fermentats en Àsia i Àfrica on l'ús de fongs filamentosos durant la fermentació és molt comú, ja que permet modificar l'acidesa, el sabor i la textura dels aliments.[11] Un altre exemple són Mucor indicor i Mucor cirinelloides, que s'utilitzen a la indústria alimentària per degradar polisacàrids com el midó en arròs, iuca o sorgo obtenint monosacàrids per a la fermentació d'aliments o d'alcohol.[1] També és molt comú en la fermentació del formatge.[8]
El gènere Mucor té molta importància en coagulació enzimàtica i la fermentació dels formatges. Històricament, l'origen de l'enzim per la coagulació de la llet ha sigut d'origen animal, concretament el quall, en l'estómac de remugants, que conté quimosina. Amb el temps i les noves tecnologies disponibles, però, han aparegut enzims d'origen no animal.[12]
Aquestes alternatives són bacteris o fongs, en els quals destaca Mucor, així com Aspergillus i Penicillium.[7] Durant el procés de producció del formatge la llet sofreix molts canvis de temperatura que poden desnaturalitzar els enzims d'origen animal i donar un lot de baixa qualitat o no comercial, donant pèrdues econòmiques. Els enzims fúngics tenen l'avantatge que són molt resistents als canvis de temperatura que es donen durant el procés de fabricació del formatge respecte als enzims del quall, sense que la qualitat del formatge es vegi molt afectada.[13]
Actualment, els enzims d'origen no animal representen el 80% de la producció mundial de formatges, sent en part gràcies a l'eficiència dels enzims dels fongs com Mucor.[7] L'aplicació de tècniques d'enginyeria genètica pot donar una producció d'enzims més eficients i evitar pèrdues econòmiques en indústries alimentàries.[13]
El gènere Mucor es fa servir o es pot fer servir per obtenir formatges com Cheddar, Gamalost, Tomme, Saint Nectaire,[12] Mozzarela,[14] Brick o Parmesà,[15] entre altres.
Problemàtica
[modifica]
Mucor és un gènere molt important i problemàtic en la indústria alimentaria. S'han observat unes 20 espècies de Mucor que poden créixer en aliment en bon estat com en fruita fresca, fruits secs, verdura fresca, cereals, nous, espècies de cuina i productes carnis. Però es destaquen 5 espècies de gran importància: Mucor circinelloides, Mucor hiemalis, Mucor piriformes, Mucor plumbeus i Mucor racemous. De manera que la presència d'aquests organismes en els aliments indica de que no s'han tractat correctament durant la preparació o l'emmagatzematge (en certs casos). Si no es prenen les mesures de control precises, es poden donar diferents afectacions a aliments.[5]
Per exemple, M. circinelloides i M. piriformes són possibles patògens de mangos, préssecs i maduixes. S'ha observat que els casos en què aquests aliments han estat afectats ha sigut una vegada ja collits i emmagatzemats a l'època freda (ja que aquestes dues espècies s'han observat que poden créixer a baixes temperatures). Aquests fongs també poden afectar a l'emmagatzematge en fred d'altres aliments com ous i es pot observar el creixement de floridures en cansalades, cereals o mantega.[5]
M. circinelloides és molt important en el deteriorament de diferents aliments, però encara no es té molta informació. S'ha trobat que la presencia de M. circinelloides en iogurts pot no deteriorar l'aliment però si que afecta a la qualitat. En un temps més avançat si que pot ser deteriorant si no es controla. S'ha trobat que aquest fong no pot sobreviure a la pasteurització de la llet. Per tant, si es troba M. circinelloides en llet, la contaminació ha estat després de la pasteurització. En condicions aeròbiques, si un aliment està contaminat creix el miceli i es pot veure a simple vista.[16] Es sospita que M. cirinelloides pot causar nàusees, vòmits i diarrea i fins i tot una mucormicosi rinocerrebral després de la ingestió de iogurts contaminats.[17]
Pot haver creixement de floridures en formatges suaus. Les zones d'emmagatzematges no controlades poden tenir espores de Mucor a l'aire i als estris.[5]
Biotecnologia
[modifica]La capacitat de síntesi d'enzims proteolítics i lipolítics (que trenquen proteïnes i lípids respectivament), la presència d'una fase de llevat i l'alt rang de tolerància a diferents temperatures en les espècies de Mucor fa que aquests siguin molt interessants per la biotecnologia. En particular Mucor circinelloides, que té totes aquestes característiques i a més a més, es pot transformar fàcilment (accepta material genètic del medi que prové de d'altres organismes).[5]
Biocombustibles
[modifica]Algunes espècies de Mucor (com per exemple M. circinelloides) han estat estudiades per la seva capacitat productora de lípids i les diverses fonts de carboni de la que obtenen energia. Aquestes característiques són beneficioses en la indústria de biocombustibles i a la indústria química. Aquests microorganismes poden créixer en fonts de carboni molt econòmiques i ecològiques com residus d'olis de cuina, pells de taronja, sèrum de formatge ricotta... Les indústries aprofiten la capacitat acumulativa de lípids d'aquests fongs quan creixen de manera exponencial per obtenir el màxim benefici possible.[18]
El biodièsel és una font renovable d'energia molt interessant per reduir les fonts d'emissió de diòxid de carboni. Es va estudiar la utilitat de M. cicrcinelloides en aquests àmbit i es va trobar que pot formar estructures que contenen algues que poden generar biocombustible amb aigües residuals. També s'han vist espècies que podrien implicar-se amb aquesta producció directament gràcies a les seves activitats biològiques. L'activitat que es pot aprofitar és l'emmagatzematge de lípids, ja que per exemple, el 20% del pes sec de M. circinelloides són els lípids emmagatzemats. A més a més són productors d'àcids gamma-linoleics i en matèria saponificable que poden ser transesterificats a àcids grassos metil-esters purs (FAMEs), que són un constituent bàsic de les molècules del biodièsel. Encara no està en ús a escala industrial, però els primers resultats indiquen que serà una font factible tant econòmicament com a escala de producció.[5]
Altres beneficis i problemes
[modifica]D'altra banda, s'han fet investigacions amb M. indicus i Mucor rouxii per a l'eliminació de metalls pesants en el tractament d'aigües residuals, amb l'obtenció de resultats molt optimistes.[19][20]
| Espècies | Hàbitat | Possibles utilitats o problemes |
| M. racemosus | Formatge, iogurt, nous, embotits, sól, verdures en descomposició, humans | Contaminant alimentari, patògen i s'utilitza en la producció de formatge |
| Mucor fuscus | Formatge, fang, sediments | Ús en la producció de formatge |
| Mucor lanceolatus | Formatge | Ús en la producció de formatge |
| Mucor endophyticus | Pot ser endófit de Triticum aestivum | No s'ha trobat cap |
| M. circinelloides | Sufú, blat de moro, fongs (basidiomicota), terra humida, humans i verdures en descomposició | Contaminant alimentari, ús en la producció de formatge i patògen |
En aquesta taula trobem diferents espècies de Mucor relacionades amb llocs on poden estar presents i amb les seves possibles utilitats.[8]
Importància clínica
[modifica]Unes poques espècies del gènere Mucor són patògenes i fan la Mucormycosis ("mucormicosi", en català), que és una malaltia causada per organismes de l'ordre de les Mucorales. Encara no es pot dir que sigui específica del gènere Mucor sp. perquè encara no se n'ha identificat la implicació dels micelis en la infecció dels teixits afectats. Aquesta malaltia ha estat relacionada amb Mucor cirinelloides, Mucor hiemalis i Mucor racemous, que són patògens oportunistes que infecten a través de les seves esporangiòspores, les quals són sovint al sòl o a l'aire.[1] L'agent etiològic també entra a l'hoste per inoculació a través de ferides cutànies i de les mucoses.[21] La mucormicosi afecta sobretot a persones amb altres malalties com la diabetis, SIDA, leucèmia…, però no hi ha cap registre de la seva transmissió entre persones.[1] La incidència de mortalitat arriba a ser fins i tot del 54%, doncs els símptomes de la mucormicosi es confonen amb els d'infeccions pulmonars, sinusítiques o epitelials. Quan la diagnosi es fa a temps, hi ha casos que es poden tractar amb antifúngics que requereixen prescripció mèdica. Normalment s'empra l'ampotericina B, el posaconazol o l'isavuconazol. Aquests medicaments s'administren via intra-venosa (en el cas de l'amfotericina B, el posaconazol i l'isavuconazol) o oral (posaconazol o isavuconazol). En alguns casos, el tractament de la mucormicosi requereix de la retirada del teixit infectat mitjançant mètodes quirúrgics per evitar la invasió a altres teixits per part de l'agent etiològic.[22]
Quadre clínic de la mucoromicosi
[modifica]Segons la localització anatòmica de la infecció, la mucormicosi pot ésser de tipus: Rhinocerebral, pulmonar, cutània, gastrointestinal, disseminada o com a malaltia rara.[21]
La mucormicosi és una malaltia oportunista no gaire habitual, d'origen fúngic, la qual afecta pacients molt immunodeprimits que també poden presentar hiperglicèmia i/o cetoacidosi, així com excés de ferro a la sang (cosa que no és només un desordre, sinó que succeeix quan una persona ha estat sotmesa a moltes transfusions sanguínies). També es pot donar el cas en què pacients sans siguin inoculats amb espores a través de ferides de tipus traumàtic o a través d'injecció durant el consum de drogues.[23]
És fàcil que un pacient amb mucormicosi sigui tractat tard, doncs al principi no hi ha manifestacions clíniques gaire òbvies de diferenciar respecte d'altres tipus dinfecció. Però, si la diagnosi no és ràpida i el tractament agressiu, la malaltia gairebé sempre acaba i és fatal per aquell qui la pateix.[23] Les espores inhalades o inoculades provoquen una reacció inflamatòria desmesesurada en pacients sans. Per tal què es doni la infecció les espores han d'escapar les cèl·lules NK per mitjà de la seva entrada a fagòcits mononuclears i poli. Així, les seves hifes hi germinen i es dona una forma d'infecció angioinvasiva, que eventualment dissemina cap a altres òrgans. És per aquesta raó que qui més risc té de patir la malaltia és la gent amb una resposta fagocítica deficient.[24]
Població de risc i ambients contaminats de la mucoromicosi
[modifica]Els agents causants de la mucormicosi són associats a ambients tals com els sistemes de ventilació d'hospitals (això suposa un factor de risc a la seva exposició, especialment en pacients immunodeprimits) i a llocs on hi ha hagut catàstrofes naturals, així com al sòl i sobre matèria vegetal en descomposició. D'altra banda, no s'ha observat que les infeccions causants de mucormicosi segueixin cap patró estacional.[25]
Els pacients immunodeprimits més susceptibles a la mucormicosi són aquells que presenten mancances funcionals en la resposta immune innata, especialment en el cas de persones amb la via de formació/ús dels fagòcits.[26] Altra causa comuna d'immunodepressió en pacients amb mucormicosi és l'ús de medicaments immunosupressors, però també hi ha altres amb especial risc de patir la malaltia:
- Pacients amb diabetis miellitus, especialment els que pateixen cetoacidosi diabètica.[23] [27]
- Pacients amb càncer, i sobretot en casos en què també presenten neutropènia.[28]
- Gent que ha rebut un trasplantament, ja sigui d'òrgans o de cèl·lules mare.[23] [27]
- Pacients amb neutropènia.[23] [27]
- Pacients que han emprat corticoesteroides durant un gran lapse de temps.[23]
- Gent que ha pres drogues via intravenosa (això és, per injecció).[23]
- Gent amb hemocromatosi.[23]
- Gent amb cicatrius a l'epiteli, resultants de cirurgies prèvies, o bé amb cicatrius a les mucoses.[23]
- Gent que va néixer en condicions de prematuritat i/o amb bas pes, en el cas de la mucormicosi gastrointestinal neonatal.[23]
D'altra banda, no s'ha enregistrat cap cas de contagi entre humans i animals no-humans.[27]
Relació de la mucormicosi amb el canvi climàtic
[modifica]Nombrosos estudis alerten que és possible que augmentin les infeccions fúngiques com les causants de mucormicosi a causa del canvi climàtic.[29][30] Això es donaria en part per sequeres més llargues, que farien que més fongs de Mucor sp. formin espores i tinguin una major expansió geogràfica.[30] L'augment de desastres naturals per culpa del canvi climàtic,[31] com huracans o inundacions, està molt relacionat amb l'expansió de la mucormicosi, que és molt freqüent després de desastres climàtics.[29]
L'augment d'infeccions fúngiques després d'un desastre natural es dona perquè els supervivents acostumen a entrar en contacte amb grans quantitats d'aigua molt contaminada, que com hem dit prèviament poden aspirar o produir infeccions a través de ferides. La dificultat per obtenir aigua i aliments nets, medicines i ferides augmenten molt el risc d'infecció després del desastre.[29]
Prevenció de la mucoromicosi
[modifica]No existeix una vacuna contra la mucormicosi, l'agent etiològic entra al cos via espores. Existeixen una sèrie de recomanacions per a evitar-ne la infecció, però no se n'ha demostrat la seva efectivitat amb models experimentals.[25] Segons el CDC, l'objectiu principal de la prevenció consistiria en adoptar pràctiques orientades a evitar-ne la seva aspiració en ambients on puguin ésser a l'aire, així com la presa preventiva d'antifúngics (en el cas de pacients que han estat sotmesos a un trasplantament, ja sigui d'òrgan o de cèl·lules mare).[32]
Com podem evitar aspirar les espores de Mucor? Es recomana evitar àrees amb molt polsim, com zones de construcció o d'excavació, i quan s'hi hagi de ser a aquests llocs fer servir un respirador tipus N95 (els quals és recomanat per la FDA com a part de la prevenció de la infecció per aspiració de partícules líquides i/o gasoses).[33] També es recomana evitar ésser a edificis amb un malfuncionament dels sistemes del corrent de l'aigua i a edificis fets malbé per l'efecte d'huracans i altres desastres naturals.[34][35][36] Finalment, es recomana dur proteccions quan es portin a terme tasques de jardineria (portar sabates i guants apropiats) i curar les ferides que es pugui fer la persona durant el procés.[32]
Existeixen mètodes de desinfecció dels sistemes de ventilació dels hospitals, que com hem mencionat abans són un dels llocs on podem trobat espores de Mucor. Aquests mètodes són principalment processos de filtració, ús de radiació ultraviolada i la gasificació per diòxid de clor, però les espores dels fongs en són generalment resistens, ja que la seva paret cel·lular actua com a barrera física envers aquests compostos.[37]
Pel que fa a la transmissió de les espores als laboratoris, cal considerar que la transmissió per via aèria es dona per la disseminació de microgotes de nuclis i/o de partícules petites. Això és, que per tal d'evitar la inhalació d'espores (les quals poden ésser transportades via aèria a grans distàncies per mitjà de corrents d'aire) es requereix l'ús de sistemes de manipulació i ventilació específics, així com ho són les AIIR:[38] es tracta d'habitacions d'aïllament amb pressió negativa, a les quals hi és només un pacient (que serà en quarantena, si el context mèdic ho ha requerit, i que tenen filtres especials (filtres HEPA) al seu sistema de ventilació.[39]
Al·lèrgies
[modifica]Un altre problema mèdic que poden causar algunes espècies de Mucor sp. són les al·lèrgies. Els darrers anys les al·lèrgies a espores de fongs han augmentat, tot i que no se'n coneix la causa. Aquestes al·lèrgies es presenten amb més prevalença en nens que en adults, i poden representar un risc a desenvolupar asma. S'ha observat que com més espores hi ha a l'aire més hospitalitzacions i morts per causa de l'asma hi ha.[40]
Referències
[modifica]- ↑ 1,00 1,01 1,02 1,03 1,04 1,05 1,06 1,07 1,08 1,09 1,10 1,11 1,12 Webster, John i Weber, Roland W.S.. Introduction to fungi. 3a edició. Cambridge, UK: Cambridge University Press, 2007, p. 180-181. ISBN 0521807395.
- ↑ «Mites and Fungi in Heavily Infested Stores in the Czech Republic». 1 de Desembre del 2004, pàg. 2144–2153.
- ↑ Hibbett, David S.; Binder, Manfred; Bischoff, Joseph F.; Blackwell, Meredith; Cannon, Paul F. «A higher-level phylogenetic classification of the Fungi». Mycological Research, 111, 5, 01-05-2007, pàg. 509–547. DOI: 10.1016/j.mycres.2007.03.004. ISSN: 0953-7562.
- ↑ 4,0 4,1 Spatafora, Joseph W.; Chang, Ying; Benny, Gerald L.; Lazarus, Katy; Smith, Matthew E. «A phylum-level phylogenetic classification of zygomycete fungi based on genome-scale data» (en anglès). Mycologia, 108, 5, 2016-9, pàg. 1028–1046. DOI: 10.3852/16-042. ISSN: 0027-5514. PMC: PMC6078412. PMID: 27738200.
- ↑ 5,00 5,01 5,02 5,03 5,04 5,05 5,06 5,07 5,08 5,09 5,10 5,11 Morin-Sardin, Stéphanie; Nodet, Patrice; Coton, Emmanuel; Jany, Jean-Luc «Mucor: A Janus-faced fungal genus with human health impact and industrial applications». Fungal Biology Reviews, 31, 1, 01-01-2017, pàg. 12–32. DOI: 10.1016/j.fbr.2016.11.002. ISSN: 1749-4613 [Consulta: 2 novembre 2019].
- ↑ 6,0 6,1 «Mucor» (en angles). The University of Adelaide. Arxivat de l'original el 2019-10-29. [Consulta: 29 octubre 2019].
- ↑ 7,0 7,1 7,2 7,3 Moore, D. (David), 1942-. 21st century guidebook to fungi. Cambridge: Cambridge University Press, 2011. ISBN 9781107006768.
- ↑ 8,0 8,1 8,2 Lebreton, Annie; Meslet-Cladière, Laurence; Morin-Sardin, Stéphanie; Coton, Emmanuel; Jany, Jean-Luc «Comparative analysis of five Mucor species transcriptomes». Genomics, 111, 6, 2019-12, pàg. 1306–1314. DOI: 10.1016/j.ygeno.2018.09.003. ISSN: 0888-7543 [Consulta: 19 novembre 2019].
- ↑ 9,0 9,1 9,2 9,3 Gadea, Ignacio; Cuenca-Estrella, Manuel; Martín, Estrella; Pemán, Javier; Pontón, José «Procedimientos de diagnóstico microbiológico de las micosis y estudios de sensibilidad a los antifúngicos». Enfermedades Infecciosas y Microbiología Clínica, 25, 5, 2007-05, pàg. 336–340. DOI: 10.1157/13102270. ISSN: 0213-005X.
- ↑ Lass-Flörl, C. «Zygomycosis: conventional laboratory diagnosis». Clinical Microbiology and Infection, 15, 2009, pàg. 60–65. DOI: 10.1111/j.1469-0691.2009.02999.x. ISSN: 1198-743X.
- ↑ 11,0 11,1 Botha, A.; Botes, A. Mucor. Oxford: Academic Press, 2014, p. 834–840. ISBN 9780123847331 [Consulta: 2 novembre 2019].
- ↑ 12,0 12,1 Anton,, Alexander «EDA/EUCOLAIT Guidance on Cheese as Raw Material as adopted on 1st February 2018». Comissió Europea, 01-02-2018, pàg. 8 [Consulta: 20 novembre 2019].
- ↑ 13,0 13,1 Yegin, Sirma; Fernandez-Lahore, Marcelo; Jose Gama Salgado, Antonio; Guvenc, Ulgar; Goksungur, Yekta «Aspartic proteinases from Mucor spp. in cheese manufacturing» (en anglès). Applied Microbiology and Biotechnology, 89, 4, 01-02-2011, pàg. 949–960. DOI: 10.1007/s00253-010-3020-6. ISSN: 1432-0614 [Consulta: 20 novembre 2019].
- ↑ Rusdan, I H; Kusnadi, J «Production of Mozzarella Cheese Using Rennin Enzyme from Mucor miehei Grown at Rice Bran Molasses Medium». IOP Conference Series: Materials Science and Engineering, 193, Abril 2017, pàg. 1-6. DOI: 10.1088/1757-899X/193/1/012011. ISSN: 1757-8981 [Consulta: 20 novembre 2019].
- ↑ Richardson, G.H.; Nelson, J.H.; Lubnow, R.E.; Schwarberg, R.L. «Rennin-like Enzyme from Mucor pusillus for Cheese Manufacture». Journal of Dairy Science, 50, 7, 1967-07, pàg. 1066–1072. DOI: 10.3168/jds.s0022-0302(67)87566-0. ISSN: 0022-0302 [Consulta: 20 novembre 2019].
- ↑ Snyder, Abigail B.; Churey, John J.; Worobo, Randy W. «Characterization and control of Mucor circinelloides spoilage in yogurt». International Journal of Food Microbiology, 228, 2016-07, pàg. 14–21. DOI: 10.1016/j.ijfoodmicro.2016.04.008. ISSN: 0168-1605 [Consulta: 19 novembre 2019].
- ↑ Morin-Sardin, Stéphanie; Rigalma, Karim; Coroller, Louis; Jany, Jean-Luc; Coton, Emmanuel «Effect of temperature, pH, and water activity on Mucor spp. growth on synthetic medium, cheese analog and cheese». Food Microbiology, 56, 2016-06, pàg. 69–79. DOI: 10.1016/j.fm.2015.11.019. ISSN: 0740-0020 [Consulta: 20 novembre 2019].
- ↑ Kamoun, Omama; Muralitharan, Gangatharan; Belghith, Hafedh; Gargouri, Ali; Trigui-Lahiani, Hèla «Suitable carbon sources selection and ranking for biodiesel production by oleaginous Mucor circinelloides using multi-criteria analysis approach». Fuel, 257, 01-12-2019, pàg. 116117. DOI: 10.1016/j.fuel.2019.116117. ISSN: 0016-2361 [Consulta: 2 novembre 2019].
- ↑ Yan, G., & Viraraghavan, T. (2003). Heavy-metal removal from aqueous solution by fungus Mucor rouxii. Water research, 37(18), 4486-4496.
- ↑ Karimi, K., & Zamani, A. (2013). Mucor indicus: biology and industrial application perspectives: a review. Biotechnology advances, 31(4), 466-481.
- ↑ 21,0 21,1 Petrikkos, G., Skiada, A., Lortholary, O., Roilides, E., Walsh, T. J., & Kontoyiannis, D. P. (2012). Epidemiology and clinical manifestations of mucormycosis. Clinical Infectious Diseases, 54(suppl_1), S23-S34.
- ↑ «Treatment for Mucormycosis | Mucormycosis | Fungal Diseases | CDC» (en anglès americà), 26-05-2019. [Consulta: 8 novembre 2019].
- ↑ 23,00 23,01 23,02 23,03 23,04 23,05 23,06 23,07 23,08 23,09 Lewis, R. E., & Kontoyiannis, D. P. (2013). Epidemiology and treatment of mucormycosis. Future microbiology, 8(9), 1163-1175.
- ↑ Spellberg, B., Edwards, J., & Ibrahim, A. (2005). Novel perspectives on mucormycosis: pathophysiology, presentation, and management. Clinical microbiology reviews, 18(3), 556-569.
- ↑ 25,0 25,1 Richardson, M. (2009). The ecology of the Zygomycetes and its impact on environmental exposure. Clinical Microbiology and Infection, 15, 2-9.
- ↑ Inglesfield, S., Jasiulewicz, A., Hopwood, M., Tyrrell, J., Youlden, G., Mazon-Moya, M., ... & Voelz, K. (2018). Robust phagocyte recruitment controls the opportunistic fungal pathogen Mucor circinelloides in innate granulomas in vivo. MBio, 9(2), e02010-17.
- ↑ 27,0 27,1 27,2 27,3 Walsh TJ, Gamaletsou MN, McGinnis MR, Hayden RT, Kontoyiannis DP. Early clinical and laboratory diagnosis of invasive pulmonary, extrapulmonary, and disseminated mucormycosis (zygomycosis). Clin Infect Dis. 2012 Feb;54 Suppl 1:S55-60.
- ↑ Petrikkos G, Skiada A, Lortholary O, Roilides E, Walsh TJ, Kontoyiannis DP. Epidemiology and clinical manifestations of mucormycosis. Clin Infect Dis. 2012 Feb;54 Suppl 1:S23-34.
- ↑ 29,0 29,1 29,2 Benedict, Kaitlin; Park, Benjamin J. «Invasive Fungal Infections after Natural Disasters» (en anglès americà). Volume 20, Number 3—March 2014 - Emerging Infectious Diseases journal - CDC, Març 2014, pàg. 349-355. DOI: 10.3201/eid2003.131230 [Consulta: 20 novembre 2019].
- ↑ 30,0 30,1 USGCRP. «Fungal Diseases and Climate Change | Climate and Health Assessment» (en anglès). [Consulta: 20 novembre 2019].[Enllaç no actiu]
- ↑ Change, Intergovernmental Panel on Climate.. Climate Change 2013 : the Physical Science Basis.. Cambridge University Press, 2014. ISBN 9781107415324.
- ↑ 32,0 32,1 «People at Risk For Mucormycosis | Mucormycosis | CDC» (en anglès americà), 31-05-2019. [Consulta: 1r novembre 2019].
- ↑ «Masks and N95 Respirators» (en anglès), 18-05-2015. [Consulta: 19r novembre 2001].
- ↑ Brandt, M., Brown, C., Burkhart, J., Burton, N., Cox-Ganser, J., Damon, S., ... & Morgan, J. (2006). Mold prevention strategies and possible health effects in the aftermath of hurricanes and major floods. Morbidity and Mortality Weekly Report: Recommendations and Reports, 55(8), 1-CE.
- ↑ Benedict, K., Adebanjo, T., Harris, J., Lockhart, S., Peterson, J., McClinton, S., ... & Whitney, A. (2011). Notes from the field: Fatal fungal soft-tissue infections after a Tornado---Joplin, Missouri, 2011. Morbidity and Mortality Weekly Report, 60(29).
- ↑ Chow, N. A., Toda, M., Pennington, A. F., Anassi, E., Atmar, R. L., Cox-Ganser, J. M., ... & Leining, L. M. (2019). Hurricane-Associated Mold Exposures Among Patients at Risk for Invasive Mold Infections After Hurricane Harvey—Houston, Texas, 2017. Morbidity and Mortality Weekly Report, 68(21), 469.
- ↑ Rutala, W. A., & Weber, D. J. (2008). Guideline for disinfection and sterilization in healthcare facilities, 2008.
- ↑ Siegel, J. D., Rhinehart, E., Jackson, M., & Chiarello, L. (2007). 2007 Guideline for isolation precautions preventing transmission of infectious agents in healthcare settings.
- ↑ «Glossary | Isolation Precautions | Guidelines Library | Infection Control | CDC» (en anglès americà), 28-03-2019. [Consulta: 1r novembre 2019].
- ↑
Bibliografia
[modifica]- ed.. Diccionario Enciclopédico Ilustrado de Medicina Dorland (en castellà). vol. 4. McGraw-Hill - Interamericana de España, 1996. ISBN 84-7615-986-2.
