Portal:Proves d'accés a la universitat/Quimica
Aparença
| << PAU | Ciències de la naturalesa | Física | Química | Biologia | CC. Terra i medi ambient |
Química
[modifica]Conceptes generals
[modifica]La radiació, els àtoms i les molècules
[modifica]
Model atòmic de Rutherford.
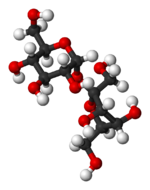
Molècula de sacarosa.
- Radiació electromagnètica
- Àtom
- Molècula
- Massa molecular
- Energia química
- Absorció
- Radiació infraroja
- Efecte d'hivernacle
- Radiació ultraviolada
- Ozó
- Orbital molecular
- Volum atòmic
- Ionització
- Electronegativitat
- Espectroscòpia infraroja
- Ressonància magnètica nuclear
- Espectrometria de masses
- Temperatura
- Energia cinètica
- Gas
- Liqüefacció de gasos
Els canvis d'energia en les reaccions químiques
[modifica]

- Reacció química
- Reacció orgànica
- Energia interna
- Entalpia
- Calor de reacció
- Llei de Hess
- Energia d'enllaç
- Longitud d'enllaç
- Polaritzabilitat
- Ordre d'enllaç
- Doble enllaç
- Triple enllaç
- Energia reticular
- Electrostàtica
- Compost iònic
- Compost binari iònic
- Atomització
- Ionització
L’equilibri de fases i l’equilibri químic
[modifica]
- Equilibri de fases
- Equilibri químic
- Diagrama de fases
- Aigua
- Diòxid de carboni
- Equilibri homogeni
- Equilibri heterogeni
- Constant d'equilibri
- Constant d'equilibri de concentració
- Constant d'equilibri de pressió
- Amoníac
- Carbonat de calci
- Esterificació
Els equilibris químics iònics
[modifica]
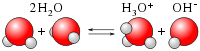

- Ió
- Àcid
- Base
- Reacció àcid-base
- Teoria àcid-base de Brønsted-Lowry
- Autoionització de l'aigua
- Acidesa
- Alcalinitat
- pH
- Indicador de pH
- Solució àcida
- Sal
- Corba de valoració
- Valoració química
- Punt d'equivalència
- Dissolució
- Equilibri de solubilitat
- Funció
- Qps
- Kps
- Complex químic
L’espontaneïtat i la velocitat de les reaccions químiques
[modifica]
- Reacció química
- Termodinàmica
- Procés espontani
- Entropia
- Cinètica química
- Velocitat de reacció
- Teoria de les col·lisions
- Teoria de l'estat de transició
- Catàlisi
- Reacció en cadena
- CFC
Les piles i cel·les electrolítiques
[modifica]Esquema de l'electròlisi ígnia.
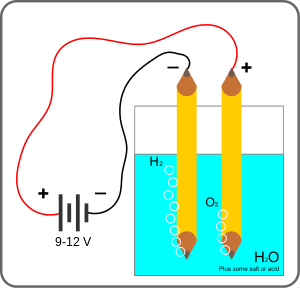
Esquema de l'electròlisi de l'aigua.
- Cel·la electroquímica
- Cel·la electrolítica
- Força electromotriu
- Corrosió de metalls
- Electròlisi
- Cromatge
- Refinació electrolítica
- Electròlisi de la salmorra
- Clor
- Lleixiu
- Pila de combustible
- Hidrogen
 Qualitat
Qualitat
Referències
[modifica]
- Orientacions per la prova de la matèria Química de les PAU - 2017 Generalitat de Catalunya.