Esteatosi hepàtica
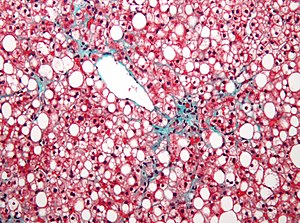 Micrografia d'una esteatosi hepàtica no alcohòlica, mostrant una esteatosi macrovesicular marcada. Tinció: Tricròmic de Masson/Verhoeff. | |
| Tipus | lipidosi i malaltia |
|---|---|
| Especialitat | gastroenterologia |
| Patogènesi | |
| Associació genètica | LCP1 (en) |
| Classificació | |
| CIM-10 | K70, K76.0 |
| CIM-9 | 571.0, 571.8 |
| Recursos externs | |
| OMIM | 228100 |
| DiseasesDB | 18844 |
| eMedicine | 175472 i 170409 |
| MeSH | D005234 |
| UMLS CUI | C0015695 i C0015696 |
| DOID | DOID:9452 |
L'esteatosi hepàtica,[1] també coneguda com a lipoïdosi hepàtica,[1] és una condició patològica potencialment reversible amb vacúols de triacilglicerols de mida diversa que s'acumulen en les cèl·lules del fetge a través del procés d'esteatosi (emmagatzematge excessiu de greix). Si bé té múltiples causes, el fetge gras pot ser considerat una sola malaltia que es produeix a tot el món en aquells amb consum excessiu d'alcohol i en els quals són obesos (amb efectes de la resistència a la insulina o sense).[2][3] La malaltia també s'associa amb altres processos que influeixen en el metabolisme dels greixos.
L'enolisme altera els normals processos bioquímics del teixit adipós; això inclou una activació inadequada de la lipòlisi, una absorció anòmala de la glucosa mediada per la insulina i pertorbacions en la secreció i expressió de les adipocines −entre elles l'adiponectina−, uns canvis que promouen un estat inflamatori persistent. La lipòlisi indueix l'aparició de l'esteatosi hepàtica i les adipocines poden afectar altres teixits corporals. El ritme de progressió i la gravetat l'esteatosi hepàtica varia segons paràmetres individuals, com ara l'estat nutricional de base.[4] Existeix una resposta sexual dimòrfica davant l'alcohol i, per tant, en la gènesi de l'esteatosi alcohòlica. Les dones són més proclius a desenvolupar malalties relacionades amb l'alcohol i la inflamació que aquest provoca, possiblement a causa de factors hormonals i de la seva distribució i proporció corporal del teixit adipós.[5]
Morfològicament és difícil distingir l'esteatosi hepàtica alcohòlica de la no alcohòlica, ja que totes dues mostren canvis grassos micro i macrovesiculars en diferents etapes de la seva evolució. Pel diagnòstic de l'esteatosi són fonamentals els estudis ecogràfics i/o de RM, la qual determina la relació aigua-greix en el fetge amb una bona especificitat (~93%) i alta sensibilitat (~96%) i detecta bé l'esteatosi quan és >20% del parènquima.[6] La espectroscòpia de ressonància magnètica nuclear és un procediment de molta fiabilitat, si bé no és una tècnica a l'abast de la majoria de centres mèdics.[7] La TC d'energia única quantitativa també és una eina diagnòstica vàlida, ja que diferencia la densitat del teixit hepàtic sa i la de l'esteatòsic.[8] Sobretot en malalts obesos, l'elastografia per ressonància magnètica, un procediment d'imatge avançat, obté millors resultats detectant la progressió fibrosa en el fetge gras que les proves ultrasonogràfiques de darrera generació,[9] encara que les millores en l'elastografia realitzada amb puls ecogràfic amb tecnologia de control de paràmetres atenuats mostren uns alts índexs de sensibilitat i especificitat.[10] A banda de les habituals analítiques de perfil hepàtic i lipídic, les proves d'alè amb metacetina tenen utilitat a l'hora de diferenciar les esteatosis simples de les esteatohepatitis no alcohòliques.[11]
El fetge gras simple té un curs benigne, mentre que un 25% dels pacients sense tractar que presenten esteatosi hepàtica amb canvis d'inflamació i fibrosi poden desenvolupar una cirrosi en un període d'uns 10 anys. Cal recordar que la cirrosi apareix en el fetge d'un alcohòlic i també en el de un no alcohòlic. Els principals factors de risc per a sofrir aquestes complicacions a partir d'un fetge gras són: edat (més de 45 anys), concurrència de diabetis tipus II i elevació dels nivells de triglicèrids i transaminases en les analítiques de sang. És recomanable efectuar una biòpsia hepàtica a les persones amb criteris de fetge gras que presentin almenys dos dels factors abans esmentats.[12]
Una presentació poc freqüent del trastorn és l'esteatosi hepàtica focal multinodular, que es caracteritza per lesiones hiperecòiques, de vegades confluents i de marges definits; les quals necessiten un acurat diagnòstic diferencial amb altres malalties del fetge com abscessos, adenomatosi, hemangiomatosi o hepatocarcinoma multicèntric.[13]
L'esteatosi no alcohòlica (EHNA) s'acompanya d'alteracions electrocardiogràfiques relacionades amb el sistema de conducció cardíac.[14] Per aquest motiu, es considera que pot ser un factor aritmogènic que es correlaciona també amb la presència de greix ectòpic a miocardi i pericardi.[15] S'ha fet palès que la malnutrició materna o durant el primer període postnatal provoca canvis epigenètics que condicionen el desenvolupament de l'EHNA, principalment alterant les circuits hipotalàmics que regulen l'homeòstasi energètica.[16] Altres estudis fan èmfasi en la importància de l'estrès oxidatiu i dels nivells de coure orgànic en la patogènesi de l'EHNA.[17] L'EHNA pot potenciar els efectes adversos de determinats fàrmacs, com ara el paracetamol,[18] alguns antibiòtics (telitromicina,[19] piperacilina/tazobactam[20]), certs agents antihipertensius i anestèsics inhalatoris o de la ticlopidina.[21]
En el món occidental és l'hepatopatia predominant amb una prevalença del 20-30%, segons diferents estudis, i ocasiona un cost sanitari considerable.[22][23] Afecta el 25% dels europeus adults i és la principal causa de malaltia hepàtica avançada al nostre continent; associada a un increment dels casos de síndrome metabòlica.[24] Diversos estudis epidemiològics indiquen que existeix una relació, no vinculada amb el normal procés d'envelliment o la menopausa, entre l'EHNA i malalties en aparença independents del dipòsit de lípids al fetge, com la sarcopènia i l'osteoporosi.[25] Pel que fa a l'osteoporosi, encara no es coneixen del tot les complexes interaccions mútues entre l'esquelet, el teixit adipós i el fetge; en les quals intervenen múltiples factors, com ara la inflamació crònica, els nivells de vitamina D3, d'irisina,[26] de somatotropina o d'osteopontina,[27] per exemple. Les evidències indiquen, però, que és recomanable fer un seguiment de la densitat mineral òssia en les persones amb EHNA.[28]
Un problema preocupant és l'augment de la incidència d'EHNA entre la població pediàtrica i juvenil. Es creu que en els propers 10 anys serà en els països occidentals la principal causa de patologia hepàtica, fallida hepàtica i trasplantament de fetge en dits grups d'edat. Molts especialistes consideren que el fet té uns orígens que van més enllà de la modificació dels hàbits alimentaris i que la investigació al respecte es escassa o limitada a camps excessivament concrets, de forma que el coneixement de la patofisiologia del trastorn es pobre i ha reduït les opcions de teràpies efectives des que aquesta malaltia fou descrita per primera vegada en nens a mitjans de la dècada de 1970. Per exemple, es desconeix el possible paper del FXR (un receptor nuclear d'hormones expressat al fetge i l'intestí, en anglès: Farnesoid X Receptor)[29] en la gènesi d'EHNA durant l'etapa de desenvolupament infantil/juvenil.[30] El FXR intervé en la regulació del metabolisme de l'àcid araquidònic i el desequilibri entre els metabòlits d'aquesta substància es considera un dels elements implicats en la progressió de l'EHNA.[31] Farmacòlegs japonesos treballen en l'obtenció de nous medicaments antidislipidèmics basats en antagonistes del FXR.[32] Diversos estudis posen l'accent sobre la coincidència de fetge gras i alteracions de la microbiota intestinal en nens i adolescents obesos, indicant que l'ús de probiòtics podria ser beneficiós per tractar el trastorn.[33] Ara bé, altres treballs adverteixen que probiòtics, prebiòtics i simbiòtics no tenen activitat en diferents cohorts de la mateixa població, un fet que fa recomanable l'estudi del perfil metagenòmic i metabolòmic de la flora per identificar els subgrups de pacients en els que aquest tipus de teràpia podria ser útil.[34] Alguns autors alerten del risc de mercantilització medicamentosa en l'abordatge de l'esteatosi hepàtica en aquest grup etari, poc adherent[35] a les dietes hipocalòriques i l'exercici físic, ja que recórrer a intervencions farmacològiques en aparença innòcues pot ser una opció senzilla amb efectes contraproduents.[36] S'ha observat que en els malalts sotmesos a cirurgia bariàtrica es produeix una significativa millora dels marcadors histològics i bioquímics d'EHNA.[37] No és, però, un procediment aplicable a tots els pacients amb aquesta patologia.[38]
Els darrers avenços en proteòmica intenten aclarir les complexes disfuncions mitocondrials que provoquen la transformació de l'EHNA en una esteatohepatitis no alcohòlica.[39] A hores d'ara, nous fàrmacs orientats a tractar específicament aquesta variant d'esteatosi hepàtica en persones amb alt risc de progressió es troben en diferents fases d'assaig (elafibranor, ácid obeticòlic, emricasan, liraglutida o aramchol, per mencionar alguns).[40] Els àcids grassos omega 3 tenen un efecte beneficiós sobre la funcionalitat hepàtica i redueixen l'hipertrigliceridèmia i els nivells de transaminases, però -histològicament- la seva capacitat de reducció de l'esteatosi no sembla gaire significativa, siguin aportats per la dieta o en forma de suplements.[41] Un inhibidor per via oral de l'acetil-CoA carboxilasa, el GS-0976, disminueix significativament la quantitat de greix hepàtic dels malalts d'esteatohepatitis no alcohòlica, però augmenta el nivell de triglicèrids en sang.[42]

Experiments fets en ratolins indiquen que el resveratrol, juntament amb una certa restricció calòrica, pot tenir un efecte protector davant l'esteatosi hepàtica; ja que activa el procés autofàgic i disminueix l'estrès del reticle endoplasmàtic dels hepatòcits.[43] Aquestes troballes concorden amb observacions anteriors sobre el paper de dita substància en la prevenció de l'esteatosi no alcohòlica i la reparació d'un metabolisme lipídic alterat.[44] Diverses combinacions de productes vegetals propis de la farmacopea oriental han estat proposades com suplements dietètics o agents preventius.[45][46] La silimarina, una substància extreta del card marià i ja utilitzada com a tònic hepàtic pels herbolaris occidentals, ha demostrat tenir efectes benèfics in vivo i in vitro sobre els fetges de ratolins sotmesos a una esteatohepatitis no alcohòlica induïda.[47] S'han realitzat treballs en animals d'experimentació per valorar l'acció terapèutica de l'eugenol (4-alil-2-metoxifenol) sobre el fetge gras, un oli extret principalment del clavell d'espècia de l'arbre Syzygium aromaticum, com que sembla regular determinats mecanismes que controlen l'acumulació lipídica en el fetge.[48] La major part d'aquests productes són polifenols d'origen natural, que oscil·len entre agrupacions moleculars molt petites i compostos altament polimeritzats. A banda de la seva diversitat química, l'avaluació rigorosa de l'activitat que tenen sobre el fetge gras i altres patologies hepàtiques depèn de múltiples factors (per exemple: genotip del vegetal, cultivar, temps de collita, condicions d'emmagatzematge), sent difícil aconseguir una sistematització metodològica dels experiments i/o assajos relacionats amb el seu efecte sobre la salut.[49] La pioglitazona (un fàrmac emprat per tractar la diabetis tipus 2) també sembla tenir la capacitat d'atenuar l'esteatosi, al millorar l'expressió dels gens hepàtics relacionats amb la lipòlisi i inhibir la dels responsables de la lipogènesi.[50] Segons treballs experimentals, l'ezetimiba (un hipolipemiant) podria reduir el grau d'esteatosi;[51] encara que estudis recents afirmen que dit fàrmac millora els indicadors de lesió hepàtica en el fetge gras no alcohòlic, però no disminueix quantitativament l'esteatosi.[52] La vildagliptina, un altre compost hipolipemiant que és un inhibidor de la dipeptidil peptidasa-4 (DPP4), actua afavorint l'acció de les incretines GLP-1 i GIP (polipèptid inhibidor gàstric, en anglès: Gastric Inhibitory Polypeptide), un fet que disminueix els nivells de triglicèrids hepàtics amb independència del pes corporal i sense alterar la resistència perifèrica a la insulina.[53] Un problema de molts d'aquests compostos és que els seus efectes secundaris a llarg termini poden ocasionar més perjudicis en determinats pacients que els beneficis que aporten al tractament de l'esteatosi hepàtica. Per exemple, cal tenir una precaució especial a l'hora de prescriure inhibidors de la DPP4 en persones amb problemes cardíacs.[54] Estudis en murins indiquen que dosis baixes de CO augmenten els mecanismes d'autofàgia i tenen un efecte protector davant l'esteatosi hepàtica induïda, sense provocar danys als hepatòcits.[55] L'autofàgia cel·lular té un paper important en la degradació de les macromolècules lipídiques i l'excés d'etanol limita aquesta funció, fet que -a més de generar esteatosi- comporta una hepatotoxicitat greu i afavoreix l'apoptosi de les cèl·lules del fetge. Per tant, recuperar la normalitat dels processos autofàgics és un objectiu terapèutic en el tractament del fetge gras alcohòlic i les seves serioses complicacions. Proves en animals posen de manifest que fàrmacs ja clínicament disponibles com la rapamicina o la carbamazepina podrien tenir aplicacions en aquest camp de recerca.[56][57]
Per quantificar amb valor pronòstic la mida dels vacúols en determinats casos, s'ha crear un mètode automatitzat d'anàlisi d'imatges de les preparacions histològiques hepàtiques tenyides amb hematoxilina-eosina.[58]
Causes
[modifica]L'esteatosi hepàtica s'associa comunament amb la ingesta d'alcohol o la síndrome metabòlica (diabetis, hipertensió, obesitat i dislipidèmia), però també pot tenir moltes altres causes:[59][60][61]
- Metabòliques
Abeta-lipoproteïnèmia (una malaltia genètica autosòmica recessiva)[62] caracteritzada per una absorció alterada dels greixos i també anomenada síndrome de Bassen-Kornzweig),[63] malalties d'emmagatzematge de glicogen, malaltia de Weber-Christian (un tipus de panniculitis que pot cursar amb afectació hepàtica),[64] esteatosi aguda de l'embaràs (una rara i seriosa complicació que apareix en el tercer trimestre de gestació i provoca una greu esteatosi hepatocitària sense inflamació o necrosi),[65] lipodistròfia (un trastorn del teixit adipós que pot tenir un origen genètic, autoimmune o tòxic).[66] La síndrome de Chanarin-Dorfman (una malaltia hereditària infreqüent caracteritzada per l'acumulació de triglicèrids en el citoplasma cel·lular derivada d'un error del funcionament lisosòmic) ocasiona esteatosis macrovacuolars que ponen convertir-se en esteatohepatitis importants.[67] L'esteatosi hepàtica pot ser causada per polimorfismes de nucleòtids simples de l'apolipoproteïna C3, que estan associats amb la resistència a la insulina i la hipertrigliceridèmia.[68] L'hiperlipidèmia familiar combinada, una malaltia lipídica autosòmica dominant caracteritzada per la sobreproducció d'apoB-100, és també una rara causa d'hepatoesteatosi.[69] Els trastorns de l'oxidació dels àcids grassos (un grup de malalties hereditàries que altera el catabolisme mitocondrial de dites substàncies)[70] provoquen greus esteatosis hepàtiques, a més de cardiomiopaties aritmogèniques i, sobretot en nens, encefalopaties progressives que poden ser fatals.[71] Han estat identificats com a origen de presumptes morts sobtades infantils.[72]
L'hipopituïtarisme/panhipopituïtarisme[73] i el dèficit de somatotropina són causes d'EHNA,[74] la qual pot ser reversible amb una correcta teràpia de substitució hormonal.[75] De vegades, l'origen de les disfuncions metabòliques de l'eix hipotàlem-hipòfisi i de la EHNA derivada d'elles és un craniofaringioma (un tumor cerebral derivat del teixit embrionari de la glàndula pituïtària) d'inici infantil.[76] Els nens amb hipopituïtarisme i EHNA han de seguir controls periòdics estrictes, ja que el seu risc de progressió de l'esteatosi a la fibrosi hepàtica és alt.[77]
- Nutricionals
Desnutrició, nutrició parenteral total, dejú perllongat i pèrdua de pes severa (factors bioquímics individuals poden condicionar la gravetat de l'esteatosi en aquests casos),[78] síndrome de realimentació, derivació jejunoileal, derivació gàstrica, diverticulosi jejunal amb sobrecreixement bacterià.[79]
En malalties nutricionals greus, com el kwashiorkor infantil, l'esteatosi es provocada per alteracions en les organel·les hepatocitàries (peroxisomes i mitocòndries) que regulen el metabolisme lipídic.[80] La malnutrició postnatal, especialment l'escassetat de proteïnes, s'associa a un major risc de presentar resistència a la insulina i esteatosi hepàtica en l'adultesa.[81] El paper de l'excés o del dèficit de diversos micronutrients en la patogènesi de l'EHNA és, ara per ara, poc conegut. Es creu, però, que aquests desequilibris poden tenir importància en l'alteració de l'homeòstasi lipídica i la producció d'espècies reactives de l'oxigen, sospitant-se que influeixen en el desenvolupament de fetge gras no alcohòlic en persones no obeses.[82][83] Encara que sovint s'observa un baix nivell de folat circulant en els pacients amb EHNA, es desconeix ara per ara si la depleció d'aquesta vitamina és causa o conseqüència de l'esteatosi hepàtica.[84] Xifres anormalment baixes de folat i B12 en sèrum es correlacionen amb una major gravetat histològica en les esteatohepatitis no alcohòliques.[85]
- Fàrmacs i toxines
Amiodarona[86] (un antiarrítmic bloquejador dels canals de potassi), metotrexat, capecitabina[87] (un agent quimioteràpic de la classe de les fluoropirimidines),[88] diltiazem[89] (un bloquejador dels canal de calci), tetraciclina, àcid valproic, teràpia antiretroviral de gran activitat, glucocorticoides, tamoxifè[90] (un regulador dels receptors estrogènics utilitzat per tractar el càncer de mama),[91][92] hepatotoxines ambientals (per exemple, fòsfor, alguns enverinaments per bolets com ara els produïts per les toxines de certes espècies d'Amanita)[93] o intoxicacions alimentàries per Bacillus cereus.[94] L'aspirina provoca hepatoesteatosis greus en cas de sobredosi.[95] L'excés d'àcid oròtic (un compost heterocíclic àcid, anomenat erròniament vitamina B13 i emprat com a suplement dietètic) provoca esteatosis microvesiculars importants, potencialment evitables amb fibrats hipolipemiants.[96] No són infreqüents les esteatosis derivades d'una reacció idiosincràtica a una substància en particular.[97] La contaminació xenobiòtica ambiental és un factor que pot induir l'esteatosi hepàtica o accelerar la seva progressió.[98]
- Alcohol
L'alcoholisme és una de les principals causes d'esteatosi per la producció de metabòlits tòxics com aldehids durant el metabolisme de l'alcohol en el fetge. Aquest fenomen es produeix amb més freqüència amb l'alcoholisme crònic.
- Altres
Celiaquia,[99] malaltia inflamatòria intestinal, infecció pel VIH, hepatitis C (especialment genotip 3), i deficiència d'alfa-1-antitripsina.[100] La síndrome de Reye provoca una esteatosi hepàtica microvesicular i de distribució panlobular.[101] El trastorn per afartament s'associa amb el desenvolupament d'EHNA.[102] En nens petits, el fetge gras pot ser la primera i agressiva manifestació d'una síndrome congènita d'intolerància a la fructosa,[103] la qual provoca una esteatosi microvesicular amb focus de necrosi citoplasmàtica.[104]
En diabètics que pateixen insuficiència renal crònica avançada sotmesos a diàlisi peritoneal amb administració intraperitoneal d'insulina, una de les possibles complicacions del procediment és l'esteatosi hepàtica subcapsular, un tipus de fetge gras molt específic que fa necessari un canvi de teràpia.[105] Aquest patró esteatòsic peculiar ha estat descrit alguna vegada en malalts sense malaltia renal crònica i no dialitzats, però sense un control adequat de la seva diabetis.[106]
Alguns autors opinen que les infeccions per l'adenovirus adipogènic 36 poden ser un factor coadjuvant en l'origen de determinades esteatosis hepàtiques,[107] ja que s'associen al desenvolupament de sobrepès en humans i animals.[108]
Referències
[modifica]- ↑ 1,0 1,1 «Esteatosi hepàtica». Cercaterm. TERMCAT, Centre de Terminologia.
- ↑ Buqué, X; Aspichueta, P; Ochoa, B «Fundamento molecular de la esteatosis hepática asociada a la obesidad» (en castellà). Rev Esp Enferm Dig, 100, 9, 2008, pàg. 565-578. ISSN: 1130-0108 [Consulta: 6 juliol 2017].
- ↑ Wanless, IR; Lentz, JS «Fatty liver hepatitis (steatohepatitis) and obesity: an autopsy study with analysis of risk factors». Hepatology, 12, 5, 1990, pàg. 1106-10. PMID: 2227807.
- ↑ Steiner, JL; Lang, CH «Alcohol, Adipose Tissue and Lipid Dysregulation» (en anglès). Biomolecules, 7, 1, 16-02-2017, pàg. E16. DOI: 10.3390/biom7010016. PMC: 5372728. PMID: 28212318 [Consulta: 27 març 2018].
- ↑ Fulham, MA; Mandrekar, P «Sexual Dimorphism in Alcohol Induced Adipose Inflammation Relates to Liver Injury» (en anglès). PLoS One, 11, 10, 06-10-2016, pàg. e0164225. DOI: 10.1371/journal.pone.0164225. PMC: 5053524. PMID: 27711160 [Consulta: 27 març 2018].
- ↑ Gaillard, F «Diffuse hepatic steatosis» (en anglès). Radiopaedia.org, 2015, Nov, pàg. 9 [Consulta: 8 juliol 2017].
- ↑ Szczepaniak, LS; Nurenberg, P; Leonard, D; Browning, JD «Magnetic resonance spectroscopy to measure hepatic triglyceride content: prevalence of hepatic steatosis in the general population» (en anglès). Am J Physiol Endocrinol Metab, 288, 2, 2005, pàg. E462-8. DOI: 10.1152/ajpendo.00064.2004. PMID: 15339742 [Consulta: 19 setembre 2017].
- ↑ Cheng X, Blake GM, Brown JK, Guo Z, et al «The measurement of liver fat from single-energy quantitative computed tomography scans» (en anglès). Quant Imaging Med Surg, 7, 3, 2017, pàg. 281–291. DOI: 10.21037/qims.2017.05.06. PMC: 5537127. PMID: 28811994 [Consulta: 26 agost 2017].
- ↑ Cui J, Heba E, Hernandez C, Haufe W, et al «Magnetic resonance elastography is superior to acoustic radiation force impulse for the Diagnosis of fibrosis in patients with biopsy-proven nonalcoholic fatty liver disease: A prospective study» (en anglès). Hepatology, 63, 2, 2016 Feb, pàg. 453-461. DOI: 10.1002/hep.28337. PMC: 4818645. PMID: 26560734 [Consulta: 6 desembre 2017].
- ↑ Graffigna, M; Catoira, N; Soutelo, J; Azpelicueta, A; et al «Diagnóstico de esteatosis hepática por métodos clínicos, bioquímicos y por imágenes» (en castellà). Rev Argent Endocrinol Metab, 54, 1, 2017, pàg. 37-46. DOI: 10.1016/j.raem.2016.12.001. ISSN: 0326-4610 [Consulta: 22 març 2018].
- ↑ Bernal-Reyes, R «Hígado graso, esteatohepatitis alcohólica y esteatohepatitis no alcohólica» (en castellà). Rev Gastroenterol Mex, 77, Supl. 1, 2012, pàg. 84-86. DOI: 10.1016/j.rgmx.2012.07.032. ISSN: 0375-0906. PMID: 22939493 [Consulta: 8 juliol 2017].
- ↑ Tannapfel, A; Flott-Rahmel, B «Liver Biopsy in Modern Medicine» (PDF) (en anglès). InTech. Dr. Yoshiaki Mizuguchi, 2011, pàg. 13-34 [Consulta: 8 juliol 2017].[Enllaç no actiu]
- ↑ Gallarín, IM; Galeano, F; Rubio, A; Blanco, G «Esteatosis hepática focal multinodular» (en castellà). Cir Esp, 94, 4, 2016, pàg. 240-241. DOI: 10.1016/j.ciresp.2015.02.006. ISSN: 0009-739X. PMID: 25912162 [Consulta: 4 desembre 2017].
- ↑ Mangi MA, Minhas AM, Rehman H, Pathan F, et al «Association of Non-alcoholic Fatty Liver Disease with Conduction Defects on Electrocardiogram». Cureus, 21, 3, 2017, pàg. e1107. DOI: 10.7759/cureus.1107. PMC: 5400518. PMID: 28439482 [Consulta: 28 juliol 2017].
- ↑ Mangi MA, Rehman H, Minhas AM, Rafique M, et al «Non-Alcoholic Fatty Liver Disease Association with Cardiac Arrhythmias». Cureus, 9, 4, 13-04-2017, pàg. e1165. DOI: 10.7759/cureus.1165. PMC: 5429146. PMID: 28507837 [Consulta: 28 juliol 2017].
- ↑
- ↑ Antonucci, L; Porcu, C; Iannucci, G; Balsano, C; Barbaro, B «Non-Alcoholic Fatty Liver Disease and Nutritional Implications: Special Focus on Copper» (en anglès). Nutrients, 9, 10, 18-10-2017, pàg. E1137. DOI: 10.3390/nu9101137. ISSN: 2072-6643. PMID: 29057834 [Consulta: 26 octubre 2017].
- ↑ Michaut A, Le Guillou D, Moreau C, Bucher S, et al «A cellular model to study drug-induced liver injury in nonalcoholic fatty liver disease: Application to acetaminophen» (en anglès). Toxicol Appl Pharmacol, 292, 01-02-2016, pàg. 40-55. DOI: 10.1016/j.taap.2015.12.020. PMC: 4904302. PMID: 26739624 [Consulta: 26 octubre 2017].
- ↑ PubChem «Telithromycin» (en anglès). Compound Summary. National Center for Biotechnology Information, US National Library of Medicine, CID 3002190 (rev), 20-10-2018, pàg. 47 [Consulta: 26 octubre 2018].
- ↑ PubChem «Piperacillin tazobactam» (en anglès). Compound Summary. National Center for Biotechnology Information, US National Library of Medicine, CID 9918881 (rev), 20-10-2018, pàg. 14 [Consulta: 26 octubre 2018].
- ↑ Massart, J; Begriche, K; Moreau, C; Fromenty, B «Role of nonalcoholic fatty liver disease as risk factor for drug-induced hepatotoxicity» (en anglès). J Clin Transl Res, 3, Supl 1, 2017, pàg. 212–232. DOI: 10.18053/jctres.03.2017S1.006. PMC: 5500243. PMID: 28691103 [Consulta: 26 octubre 2018].
- ↑ Caballería L, Saló J, Berzigotti A, Planas R, et al «Hígado graso no alcohólico. Documento de posicionamiento de la Societat Catalana de Digestologia» (en castellà). Gastroenterol Hepatol, 37, 6, 2014, pàg. 372-383. DOI: 10.1016/j.gastrohep.2014.03.005. ISSN: 0210-5705. PMID: 24746904 [Consulta: 4 desembre 2017].
- ↑ Williams CD, Stengel J, Asike MI, Torres DM, Shaw J, Contreras M et al. «Prevalence of nonalcoholic fatty liver disease and nonalcoholic steatohepatitis among a largely middle-aged population utilizing ultrasound and liver biopsy: a prospective study». Gastroenterology, 140, 1, 2011, pàg. 124-31. DOI: 10.1053/j.gastro.2010.09.038. PMID: 20858492 [Consulta: 22 juny 2024].
- ↑ Aller R, Fernández-Rodríguez C, Lo Iacono O, Bañares R, et al «Documento de consenso. Manejo de la enfermedad hepática grasa no alcohólica (EHGNA). Guía de práctica clínica» (en castellà). Gastroenterol Hepatol, 41, 5, 2018, pàg. 328-349. DOI: 10.1016/j.gastrohep.2017.12.003. ISSN: 0210-5705. PMID: 29631866 [Consulta: 17 octubre 2018].
- ↑ Poggiogalle, E; Donini, LM; Lenzi, A; Chiesa, C; Pacifico, L «Non-alcoholic fatty liver disease connections with fat-free tissues: A focus on bone and skeletal muscle» (en anglès). World J Gastroenterol, 23, 10, 14-03-2017, pàg. 1747-57. DOI: 10.3748/wjg.v23.i10.1747. PMC: 5352914. PMID: 28348479 [Consulta: 19 octubre 2018].
- ↑ Moreno-Navarrete JM, Ortega F, Serrano M, Guerra E, et al «Irisin is expressed and produced by human muscle and adipose tissue in association with obesity and insulin resistance» (en anglès). J Clin Endocrinol Metab, 98, 4, 2013, pàg. E769-78. Arxivat de l'original el 19 d'octubre 2018. DOI: 10.1210/jc.2012-2749. ISSN: 0021-972X. PMID: 23436919 [Consulta: 19 octubre 2018].
- ↑ UniProt «Osteopontin» (en anglès). Protein knowledgebase. UniProt Consortium, P10451 (OSTP_HUMAN) (rev), 12-09-2018, pàg. 21 [Consulta: 19 octubre 2018].
- ↑ Filip, R; Radzki, RP; Bieńko, M «Novel insights into the relationship between nonalcoholic fatty liver disease and osteoporosis» (en anglès). Clin Interv Aging, 13, 04-10-2018, pàg. 1879-91. DOI: 10.2147/CIA.S170533. PMC: 6174895. PMID: 30323574 [Consulta: 19 octubre 2018].
- ↑ Rasooly, RS «Nuclear Receptor Subfamily 1, Group H, Member 4; NR1H4» (en anglès). ONIM. Entry 603826. Johns Hopkins University School of Medicine, 03-03-2017, pàg. 10 [Consulta: 27 octubre 2017].
- ↑ Temple, JL; Cordero, P; Li, J; Nguyen, V; Oben, JA «A Guide to Non-Alcoholic Fatty Liver Disease in Childhood and Adolescence» (en anglès). Int J Mol Sci, 17, 6, 2016, pàg. E947. DOI: 10.3390/ijms17060947. PMC: 4926480. PMID: 27314342 [Consulta: 26 agost 2017].
- ↑ Gai Z, Visentin M, Gui T, Zhao L, et al «The effects of farnesoid X receptor activation on arachidonic acid metabolism, NF-kB signaling and hepatic inflammation» (PDF) (en anglès). Mol Pharmacol, 2018. DOI: 10.1124/mol.117.111047. ISSN: 0026-895X. PMID: 29743187 [Consulta: 28 maig 2018].
- ↑ Shinozawa E, Amano Y, Yamakawa H, Haba M, et al «Antidyslipidemic potential of a novel farnesoid X receptor antagonist in a hamster model of dyslipidemia: Comparative studies of other nonstatin agents» (en anglès). Pharmacol Res Perspect, 6, 2, 08-03-2018, pàg. e00390. DOI: 10.1002/prp2.390. PMC: 5842406. PMID: 29541476 [Consulta: 28 maig 2018].
- ↑ Famouri, F; Shariat, Z; Hashemipour, M; Keikha, M; Kelishadi, R «Effects of Probiotics on Nonalcoholic Fatty Liver Disease in Obese Children and Adolescents» (en anglès). J Pediatr Gastroenterol Nutr, 64, 3, 2017, pàg. 413-417. DOI: 10.1097/MPG.0000000000001422. ISSN: 1536-4801. PMID: 28230607 [Consulta: 22 març 2018].
- ↑ Nobili, V; Cucchiara, S «The Use of Probiotics in Pediatric Nonalcoholic Fatty Liver Disease: Teachable Moment or Missed Opportunity?» (en anglès). J Pediatr Gastroenterol Nutr, 64, 3, 2017, pàg. 336-337. DOI: 10.1097/MPG.0000000000001431. ISSN: 1536-4801. PMID: 27749611 [Consulta: 22 març 2018].
- ↑ OMS «Adherencia a los tratamientos a largo plazo: Pruebas para la acción» (en castellà). Organización Panamericana de la Salud, 2003 (rev. 2012, Set), pàg. 202 [Consulta: 22 març 2018].
- ↑ Ranucci, G; Spagnuolo, MI; Iorio, R «Obese children with fatty liver: Between reality and disease mongering» (en anglès). World J Gastroenterol, 23, 47, 21-12-2017, pàg. 8277-82. DOI: 10.3748/wjg.v23.i47.8277. PMC: 5743498. PMID: 29307987 [Consulta: 22 març 2018].
- ↑ Nostedt JJ, Switzer NJ, Gill RS, Dang J, et al «The Effect of Bariatric Surgery on the Spectrum of Fatty Liver Disease» (en anglès). Can J Gastroenterol Hepatol, 2016, 2016, pàg. 2059245. DOI: 10.1155/2016/2059245. PMC: 5061986. PMID: 27777925 [Consulta: 17 octubre 2018].
- ↑ Cazzo, E; Pareja, JC; Chaim, EA «Nonalcoholic fatty liver disease and bariatric surgery: a comprehensive review» (en anglès). Sao Paulo Med J, 135, 3, 2017, pàg. 277-295. DOI: 10.1590/1516-3180.2016.0306311216. ISSN: 1806-9460. PMID: 28562737 [Consulta: 17 octubre 2018].
- ↑ Nuño-Lámbarri, N; Barbero-Becerra, VJ; Uribe, M; Chávez-Tapia, NC «Mitochondrial Molecular Pathophysiology of Nonalcoholic Fatty Liver Disease: A Proteomics Approach» (en anglès). Int J Mol Sci, 17, 3, 15-03-2016, pàg. 281. DOI: 10.3390/ijms17030281. PMC: 4813145. PMID: 26999105 [Consulta: 26 agost 2017].
- ↑ Lonardo A, Nascimbeni F, Targher G, Bernardi M, et al «AISF position paper on nonalcoholic fatty liver disease (NAFLD): Updates and future directions» (en anglès). Dig Liver Dis, 49, 5, 2017, pàg. 471-483. DOI: 10.1016/j.dld.2017.01.147. ISSN: 1590-8658. PMID: 28215516 [Consulta: 26 octubre 2017].
- ↑ Brea Á, Pintó X, Ascaso JF, Blasco M, et al «Enfermedad del hígado graso no alcohólico, asociación con la enfermedad cardiovascular y tratamiento (II). Tratamiento de la enfermedad del hígado graso no alcohólico» (en castellà). Clin Invest Arterioscl, 29, 4, 2017, pàg. 185-200. DOI: 10.1016/j.arteri.2016.06.002. ISSN: 0214-9168. PMID: 27692632 [Consulta: 4 desembre 2017].
- ↑ McNamara, D «New Drug Trims Liver Fat, but Triglyceride Levels Perplex» (en anglès). Medscape, 25-10-2017, pàg. 3 [Consulta: 28 octubre 2017].
- ↑ Ding S, Jiang J, Zhang G, Bu Y, et al «Resveratrol and caloric restriction prevent hepatic steatosis by regulating SIRT1-autophagy pathway and alleviating endoplasmic reticulum stress in high-fat diet-fed rats» (en anglès). PLoS One, 12, 8, 17-08-2017, pàg. e0183541. DOI: 10.1371/journal.pone.0183541. PMID: 28817690 [Consulta: 26 agost 2017].
- ↑ Andrade JM, Paraíso AF, de Oliveira MV, Martins AM, et al «Resveratrol attenuates hepatic steatosis in high-fat fed mice by decreasing lipogenesis and inflammation» (en anglès). Nutrition, 30, 7-8, 2014, pàg. 915-919. DOI: 10.1016/j.nut.2013.11.016. PMID: 24985011 [Consulta: 26 agost 2017].
- ↑ Lee JH, Lee JJ, Cho WK, Yim NH, et al «KBH-1, an herbal composition, improves hepatic steatosis and leptin resistance in high-fat diet-induced obese rats» (en anglès). BMC Complement Altern Med, 16, 13-09-2016, pàg. 355. DOI: 10.1186/s12906-016-1265-z. PMC: 5020448. PMID: 27618865 [Consulta: 28 agost 2017].
- ↑ Kim J, Lee H, Lim J, Oh J, et al «The Angiogenesis Inhibitor ALS-L1023 from Lemon-Balm Leaves Attenuates High-Fat Diet-Induced Nonalcoholic Fatty Liver Disease through Regulating the Visceral Adipose-Tissue Function» (en anglès). Int J Mol Sci, 18, 4, 17-04-2017, pàg. E846. DOI: 10.3390/ijms18040846. PMC: 5412430. PMID: 28420164 [Consulta: 28 agost 2017].
- ↑ Marin, V; Gazzin, S; Gambaro, SE; Dal Ben, M «Effects of Oral Administration of Silymarin in a Juvenile Murine Model of Non-alcoholic Steatohepatitis» (en anglès). Nutrients, 9, 9, setembre 2017, pàg. E1006. DOI: 10.3390/nu9091006. ISSN: 2072-6643. PMID: 28895929.
- ↑ Jo, HK; Kim, GW; Jeong, KJ; Kim, DY; Chung, SH «Eugenol ameliorates hepatic steatosis and fibrosis by down-regulating SREBP1 gene expression via AMPK-mTOR-p70S6K signaling pathway» (en anglès). Biol Pharm Bull, 37, 8, 2014, pàg. 1341-1351. ISSN: 1347-5215. PMID: 25087956 [Consulta: 26 octubre 2017].
- ↑ Li S, Tan HY, Wang N, Cheung F, et al «The Potential and Action Mechanism of Polyphenols in the Treatment of Liver Diseases» (en anglès). Oxid Med Cell Longev, 04-02-2018, pàg. 8394818. DOI: 10.1155/2018/8394818. PMC: 5817364. PMID: 29507653 [Consulta: 22 març 2018].
- ↑ Hsiao PJ, Chiou HC, Jiang HJ, Lee MY, et al «Pioglitazone Enhances Cytosolic Lipolysis, β-oxidation and Autophagy to Ameliorate Hepatic Steatosis» (en anglès). Sci Rep, 7, 1, 22-08-2017, pàg. 9030. DOI: 10.1038/s41598-017-09702-3. PMID: 28831172 [Consulta: 26 agost 2017].
- ↑ Chang E, Kim L, Park SE, Rhee EJ, et al «Ezetimibe improves hepatic steatosis in relation to autophagy in obese and diabetic rats» (en anglès). World J Gastroenterol, 21, 25, 07-07-2015, pàg. 7754-7763. DOI: 10.3748/wjg.v21.i25.7754. PMC: 4491962. PMID: 26167075 [Consulta: 28 agost 2017].
- ↑ Lee HY, Jun DW, Kim HJ, Oh H, et al «Ezetimibe decreased nonalcoholic fatty liver disease activity score but not hepatic steatosis» (en anglès). Korean J Intern Med, 2018; Mar 20 [Epub AoP], pàg. 9. DOI: 10.3904/kjim.2017.194. ISSN: 2005-6648. PMID: 29551054 [Consulta: 22 març 2018].
- ↑ Macauley M, Hollingsworth KG, Smith FE, Thelwall PE, et al «Effect of vildagliptin on hepatic steatosis» (en anglès). J Clin Endocrinol Metab, 100, 4, 2015, pàg. 1578-1585. DOI: 10.1210/jc.2014-3794. PMC: 4399299. PMID: 25664602 [Consulta: 28 setembre 2017].
- ↑ Verma S, Goldenberg RM, Bhatt DL, Farkouh ME, et al «Dipeptidyl peptidase-4 inhibitors and the risk of heart failure: a systematic review and meta-analysis» (en anglès). CMAJ Open, 5, 1, 24-02-2017, pàg. E152-E177. DOI: 10.9778/cmajo.20160058. PMC: 5403656. PMID: 28459046 [Consulta: 28 setembre 2017].
- ↑ Kim HJ, Joe Y, Kim SK, Park SU, et al «Carbon monoxide protects against hepatic steatosis in mice by inducing sestrin-2 via the PERK-eIF2α-ATF4 pathway» (en anglès). Free Radic Biol Med, 110, 2017, pàg. 81-91. DOI: 10.1016/j.freeradbiomed.2017.05.026. PMID: 28578014 [Consulta: 9 octubre 2017].
- ↑ Ding WX, Li M, Chen X, Ni HM, Lin CW, et al «Autophagy reduces acute ethanol-induced hepatotoxicity and steatosis in mice» (en anglès). Gastroenterology, 139, 5, 2010, pàg. 1740-1752. DOI: 10.1053/j.gastro.2010.07.041. PMC: 4129642. PMID: 20659474 [Consulta: 11 novembre 2017].
- ↑ Khambu, B; Wang, L; Zhang, H; Yin, XM «The Activation and Function of Autophagy in Alcoholic Liver Disease» (en anglès). Curr Mol Pharmacol, 10, 3, 2017, pàg. 165-171. DOI: 10.2174/1874467208666150817112654. PMC: 5585070. PMID: 26278385 [Consulta: 11 novembre 2017].
- ↑ Nativ NI, Chen AI, Yarmush G, Henry SD, et al «Automated image analysis method to detect and quantify macrovesicular steatosis in human liver hematoxylin and eosin-stained histology images» (en anglès). Liver Transpl, 20, 2, 2014, pàg. 228-236. DOI: 10.1002/lt.23782. PMC: 3923430. PMID: 24339411 [Consulta: 14 setembre 2017].
- ↑ Angulo, P «Nonalcoholic fatty liver disease» (en anglès). N. Engl. J. Med., 346, 16, 2002, pàg. 1221–31. DOI: 10.1056/NEJMra011775. ISSN: 1533-4406. PMID: 11961152.
- ↑ Bayard M, Holt J, Boroughs E «Nonalcoholic fatty liver disease» (en anglès). American Family Physician, 73, 11, 2006, pàg. 1961–8. ISSN: 1532-0650. PMID: 16770927.
- ↑ Kneeman, JM; Misdraji, J; Corey, KE «Secondary causes of nonalcoholic fatty liver disease» (en anglès). Therap Adv Gastroenterol, 5, 3, 2012, pàg. 199–207. DOI: 10.1177/1756283X11430859. PMC: 3342568. PMID: 22570680 [Consulta: 27 octubre 2017].
- ↑ McKusick, VA «Abetalipoproteinemia; ABL» (en anglès). ONIM. Johns Hopkins University School of Medicine, Entry 200100, 09-09-2016, pàg. 8 [Consulta: 27 octubre 2017].
- ↑ Suarez L, Valbuena ML, Moreno A, Santonja C, et al «Abetalipoproteinemia associated with hepatic and atypical neurological disorders» (en anglès). J Pediatr Gastroenterol Nutr, 6, 5, 1987, pàg. 799-802. ISSN: 0277-2116. PMID: 3694376 [Consulta: 5 juliol 2017].
- ↑ Amarapurkar, DN; Patel, ND; Amarapurkar, AD «Panniculitis and liver disease (hepatic Weber Christian disease)» (PDF) (en anglès). Journal of Hepatology, 42, 2005, pàg. 149-150. DOI: 10.1016/j.jhep.2004.07.026. ISSN: 0168-8278 [Consulta: 5 juliol 2017].
- ↑ Ko, H; Yoshida, EM «Acute fatty liver of pregnancy» (en anglès). Can J Gastroenterol, 20, 1, 2006, pàg. 25–30. PMC: 2538964. PMID: 16432556 [Consulta: 6 juliol 2017].
- ↑ Hegele, RA «Molecular basis of partial lipodystrophy and prospects for therapy» (en anglès). Trends Mol Med, 7, 3, 2001, pàg. 121-126. DOI: 10.1016/S1471-4914(01)01930-X. PMID: 11286783 [Consulta: 29 juliol 2017].
- ↑ Ersoy O, Alkım C, Onuk MD, Demirsoy H, Argon D «A rare cause of fatty liver and elevated aminotransferase levels: Chanarin-Dorfman syndrome: a case report» (en anglès). Int J Hepatol, 2011, pàg. 341372. DOI: 10.4061/2011/341372. PMC: 3170759. PMID: 21994851 [Consulta: 12 setembre 2017].
- ↑ Petersen KF, Dufour S, Hariri A, Nelson-Williams C, Foo JN, Zhang XM et al. «Apolipoprotein C3 gene variants in nonalcoholic fatty liver disease.». N Engl J Med, 362, 12, 2010, pàg. 1082-9. DOI: 10.1056/NEJMoa0907295. PMID: 20335584 [Consulta: 1r desembre 2023].
- ↑ de Bruin TW, Georgieva AM, Brouwers MC, Heitink MV, et al «Radiological evidence of nonalcoholic fatty liver disease in familial combined hyperlipidemia» (PDF) (en anglès). Am J Med, 116, 12, 15-06-2004, pàg. 847-849. DOI: 10.1016/j.amjmed.2003.12.031. PMID: 15178501 [Consulta: 27 octubre 2017].
- ↑ Wajner, M; Amaral, AU «Mitochondrial dysfunction in fatty acid oxidation disorders: insights from human and animal studies» (en anglès). Biosci Rep, 36, 1, 20-11-2015, pàg. e00281. Arxivat de l'original el 9 de novembre 2017. DOI: 10.1042/BSR20150240. PMC: 4718505. PMID: 26589966 [Consulta: 8 novembre 2017].
- ↑ Alonso, EM «Acute liver failure in children: the role of defects in fatty acid oxidation» (en anglès). Hepatology, 41, 4, 2005, pàg. 696-699. DOI: 10.1002/hep.20680. PMID: 15789368 [Consulta: 8 novembre 2017].
- ↑ Lovera C, Porta F, Caciotti A, Catarzi S, et al «Sudden unexpected infant death (SUDI) in a newborn due to medium chain acyl CoA dehydrogenase (MCAD) deficiency with an unusual severe genotype» (en anglès). Ital J Pediatr, 38, 24-10-2012, pàg. 59. DOI: 10.1186/1824-7288-38-59. PMC: 3502270. PMID: 23095120 [Consulta: 9 novembre 2017].
- ↑ Nyenwe, EA; Williamson-Baddorf, S; Waters, B; Wan, JY; Solomon, SS «Nonalcoholic Fatty liver disease and metabolic syndrome in hypopituitary patients» (en anglès). Am J Med Sci, 338, 3, 2009, pàg. 190-195. DOI: 10.1097/MAJ.0b013e3181a84bde. PMC: 2742767. PMID: 19745609 [Consulta: 5 abril 2018].
- ↑ Xu L, Xu C, Yu C, Miao M, et al «Association between Serum Growth Hormone Levels and Nonalcoholic Fatty Liver Disease: A Cross-Sectional Study» (en anglès). PLoS One, 7, 8, 2012, pàg. e44136. DOI: 10.1371/journal.pone.0044136. PMC: 3432067. PMID: 22952901 [Consulta: 5 abril 2018].
- ↑ Nishizawa H, Iguchi G, Murawaki A, Fukuoka H, et al «Nonalcoholic fatty liver disease in adult hypopituitary patients with GH deficiency and the impact of GH replacement therapy» (PDF) (en anglès). Eur J Endocrinol, 167, 1, 2012, pàg. 67-74. DOI: 10.1530/EJE-12-0252. ISSN: 0804-4643. PMID: 22535644 [Consulta: 5 abril 2018].
- ↑ Jung SY, Lee YJ, Lee HJ, Lee YA, et al «Nonalcoholic fatty liver disease in long-term survivors of childhood-onset craniopharyngioma» (en anglès). Ann Pediatr Endocrinol Metab, 22, 3, 2017, pàg. 189-196. DOI: 10.6065/apem.2017.22.3.189. PMC: 5642077. PMID: 29025206 [Consulta: 5 abril 2018].
- ↑ Yoon, JM; Ko, JS; Seo, JK; Shin, CH; et al «Nonalcoholic Fatty Liver Disease in Children with Hypopituitarism» (en anglès). Korean J Pediatr Gastroenterol Nutr, 13, 1, 2010, pàg. 51-57. DOI: 10.5223/kjpgn.2010.13.1.51. ISSN: 2093-5633 [Consulta: 6 abril 2018].
- ↑ Hashimoto T, Cook WS, Qi C, Yeldandi AV, et al «Defect in Peroxisome Proliferator-activated Receptor α-inducible Fatty Acid Oxidation Determines the Severity of Hepatic Steatosis in Response to Fasting» (en anglès). J Biol Chem, 275, 37, 15-09-2000, pàg. 28918-28. DOI: 10.1074/jbc.M910350199. PMID: 10844002 [Consulta: 9 juliol 2017].
- ↑ Bures J, Cyrany J, Kohoutova D, Förstl M, et al «Small intestinal bacterial overgrowth syndrome» (en anglès). World J Gastroenterol, 16, 24, 28-06-2010, pàg. 2978–90. DOI: 10.3748/wjg.v16.i24.2978. PMC: 2890937. PMID: 20572300 [Consulta: 9 juliol 2017].
- ↑ van Zutphen T, Ciapaite J, Bloks VW, Ackereley C, et al «Malnutrition-associated liver steatosis and ATP depletion is caused by peroxisomal and mitochondrial dysfunction» (en anglès). J Hepatol, 65, 6, 2016, pàg. 1198-1208. DOI: 10.1016/j.jhep.2016.05.046. PMID: 27312946 [Consulta: 29 juliol 2017].
- ↑ Dalvi PS, Yang S, Swain N, Kim J, et al «Long-term metabolic effects of malnutrition: Liver steatosis and insulin resistance following early-life protein restriction» (en anglès). PLoS One, 13, 7, 02-07-2018, pàg. e0199916. DOI: 10.1371/journal.pone.0199916. PMC: 6028108. PMID: 29965973 [Consulta: 14 octubre 2018].
- ↑ Pickett-Blakely, O; Young, K; Carr, RM «Micronutrients in Nonalcoholic Fatty Liver Disease Pathogenesis» (en anglès). Cell Mol Gastroenterol Hepatol, 6, 4, 23-08-2018, pàg. 451-462. DOI: 10.1016/j.jcmgh.2018.07.004. PMC: 6170520. PMID: 30294653 [Consulta: 13 octubre 2018].
- ↑ Sheth, SG; Gordon, FD; Chopra, S «Nonalcoholic steatohepatitis». Annals of Internal Medicine, 126, 1997, pàg. 137-45. PMID: 9005748.
- ↑ Sid, V; Siow, YL «Role of folate in nonalcoholic fatty liver disease» (PDF) (en anglès). Can J Physiol Pharmacol, 95, 10, Octubre 2017, pàg. 1141-1148. DOI: 10.1139/cjpp-2016-0681. ISSN: 0008-4212. PMID: 28460180 [Consulta: 27 octubre 2018].
- ↑ Mahamid M, Mahroum N, Bragazzi NL, Shalaata K, et al «Folate and B12 Levels Correlate with Histological Severity in NASH Patients» (en anglès). Nutrients, 10, 4, 02-04-2018, pàg. E440. DOI: 10.3390/nu10040440. PMC: 5946225. PMID: 29614799 [Consulta: 27 octubre 2018].
- ↑ PubChem «Amiodarone» (en anglès). Compound Summary. National Center for Biotechnology Information, US National Library of Medicine, CID 2157 (rev), 06-10-2018, pàg. 66 [Consulta: 13 octubre 2018].
- ↑ PubChem «Capecitabine» (en anglès). Compound Summary. National Center for Biotechnology Information, US National Library of Medicine, CID 60953 (rev), 20-10-2018, pàg. 83 [Consulta: 27 octubre 2018].
- ↑ Chin, SN; Kim, TK; Siu, LL «Hepatic steatosis secondary to capecitabine: a case report» (en anglès). J Med Case Rep, 4, 27-07-2010, pàg. 227. DOI: 10.1186/1752-1947-4-227. PMC: 2916012. PMID: 24576340 [Consulta: 27 octubre 2018].
- ↑ PubChem «Diltiazem» (en anglès). Compound Summary. National Center for Biotechnology Information, US National Library of Medicine, CID 39186 (rev), 06-10-2018, pàg. 67 [Consulta: 13 octubre 2018].
- ↑ PubChem «Tamoxifen» (en anglès). Compound Summary. National Center for Biotechnology Information, US National Library of Medicine, CID 2733526 (rev), 06-10-2018, pàg. 89 [Consulta: 13 octubre 2018].
- ↑ Osman KA, Osman MM, Ahmed MH «Tamoxifen-induced non-alcoholic steatohepatitis: where are we now and where are we going?». Expert Opinion on Drug Safety, 6, 1, Gener 2007, pàg. 1–4. DOI: 10.1517/14740338.6.1.1. ISSN: 1474-0338. PMID: 17181445.
- ↑ Pan, HJ; Chang, HT; Lee, CH «Association between tamoxifen treatment and the development of different stages of nonalcoholic fatty liver disease among breast cancer patients» (en anglès). J Formos Med Assoc, 115, 6, Juny 2016, pàg. 411-417. DOI: 10.1016/j.jfma.2015.05.006. ISSN: 0929-6646. PMID: 26071793 [Consulta: 12 novembre 2017].
- ↑ Allen, B; Desai, B; Lisenbee, N «Amatoxin: A Review» (en anglès). ISRN Emergency Medicine, 2012, pàg. 4. DOI: 10.5402/2012/190869. ISSN: 2090-5629 [Consulta: 11 novembre 2017].
- ↑ Yokoyama K, Ito M, Agata N, Isobe M, et al «Pathological effect of synthetic cereulide, an emetic toxin of Bacillus cereus, is reversible in mice» (en anglès). FEMS Immunology & Medical Microbiology, 24, 1, 01-05-1999, pàg. 115–120. DOI: 10.1111/j.1574-695X.1999.tb01272.x. ISSN: 0928-8244. PMID: 10340720 [Consulta: 26 octubre 2017].
- ↑ Bessone, F; Tanno, H «Hepatotoxicidad inducida por antiinflamatorios no esteroides» (en castellà). Gastroenterol Hepatol, 23, 4, 2000, pàg. 200-205. ISSN: 0210-5705. PMID: 10863862 [Consulta: 26 juliol 2017].
- ↑ Ferreira AV, Parreira GG, Porto LC, Mario EG, et al «Fenofibrate prevents orotic acid-induced hepatic steatosis in rats» (PDF) (en anglès). Life Sci, 82, 15-16, 09-04-2008, pàg. 876-883. Arxivat de l'original el 13 de novembre 2017. DOI: 10.1016/j.lfs.2008.02.003. ISSN: 0024-3205. PMID: 18374364 [Consulta: 12 novembre 2017].
- ↑ Tejada Cifuentes, F «Hepatotoxicidad por fármacos» (en castellà). Rev Clin Med Fam, 3, 3, 2010, pàg. 177-191. DOI: 10.4321/S1699-695X2010000300006. ISSN: 1699-695X [Consulta: 6 juliol 2017].
- ↑ Klaunig, JE; Li, X; Wang, Z «Role of xenobiotics in the induction and progression of fatty liver disease» (en anglès). Toxicol Res (Camb), 7, 4, pàg. 664-680. DOI: 10.1039/c7tx00326a. ISSN: 2045-452X. PMID: 30090613 [Consulta: 13 octubre 2018].
- ↑ Marciano F, Savoia M, Vajro P «Celiac disease-related hepatic injury: Insights into associated conditions and underlying pathomechanisms.». Dig Liver Dis, 48, 2, 2016, pàg. 112-9. DOI: 10.1016/j.dld.2015.11.013. ISSN: 1590-8658. PMID: 26711682.

- ↑ Valenti L, Dongiovanni P, Piperno A, Fracanzani AL, et al «Alpha 1-antitrypsin mutations in NAFLD: high prevalence and association with altered iron metabolism but not with liver damage» (PDF). Hepatology, 44, 4, octubre 2006, pàg. 857–64. Arxivat de l'original el 2018-10-27. DOI: 10.1002/hep.21329. PMID: 17006922 [Consulta: 27 octubre 2018].
- ↑ Glasgow, JF; Middleton, B «Reye syndrome—insights on causation and prognosis» (PDF) (en castellà). Arch Dis Child, 85, 5, 2001, pàg. 351–353. PMC: 1718987. PMID: 11668090 [Consulta: 26 juliol 2017].
- ↑ Zhang J, Abbasi O, Malevanchik L, Mohan N, Denicola R, et al «Pilot study of the prevalence of binge eating disorder in non-alcoholic fatty liver disease patients» (en anglès). Ann Gastroenterol, 30, 6, 2017, pàg. 664-669. DOI: 10.20524/aog.2017.0200. PMC: 5670286. PMID: 29118561 [Consulta: 14 novembre 2017].
- ↑ Baker, P; Ayres, L; Gaughan, S; Weisfeld-Adams, J «Hereditary Fructose Intolerance» (en anglès). GeneReviews. University of Washington, 27-12-2015, pàg. 20. PMID: 26677512 [Consulta: 28 març 2018].
- ↑ Stormon MO, Cutz E, Furuya K, Bedford M, et al «A six-month-old infant with liver steatosis» (en anglès). J Pediatr, 144, 2, 2004, pàg. 258-263. DOI: 10.1016/j.jpeds.2003.11.037. PMC: 2954655. PMID: 14760272 [Consulta: 28 març 2018].
- ↑ Jang EC, Kim G, Kim YS, Yoon SA, et al «Hepatic subcapsular steatosis in a diabetic CAPD patient receiving intraperitoneal insulin» (en anglès). Korean J Intern Med, 21, 3, 2006, pàg. 206-209. ISSN: 1226-3303. PMC: 3890728. PMID: 17017674 [Consulta: 14 octubre 2018].
- ↑ Chowdhary, V; Pernicka, JS; Sharma, R «Rare presentation of subcapsular hepatic steatosis in a woman with uncontrolled diabetes without peritoneal dialysis: a case report» (en anglès). J Med Case Rep, 10, 1, 20-12-2016, pàg. 370. DOI: 10.1186/s13256-016-1152-8. PMC: 5175298. PMID: 27998312 [Consulta: 14 octubre 2018].
- ↑ Trovato FM, Catalano D, Garozzo A, Martines GF, et al «ADV36 adipogenic adenovirus in human liver disease» (en anglès). World J Gastroenterol, 20, 40, 28-10-2014, pàg. 14706-16. DOI: 10.3748/wjg.v20.i40.14706. PMC: 4209536. PMID: 25356033 [Consulta: 13 octubre 2018].
- ↑ Ponterio, E; Gnessi, L «Adenovirus 36 and Obesity: An Overview» (en anglès). Viruses, 7, 7, 08-07-2015, pàg. 3719–40. DOI: 10.3390/v7072787. PMC: 4517116. PMID: 26184280 [Consulta: 13 octubre 2018].
Bibliografia
[modifica]- Santos, Sergio (Ed). Hepatic Steatosis: Clinical Risk Factors, Molecular Mechanisms and Treatment Outcomes (Hepatology Research and Clinical Developments). 1st Edition (en anglès). Nova Science Pub Inc, 2014, Ag 30; pàgs: 271. ISBN 9781633214033 [Consulta: 12 setembre 2017].
- Calleja, José L.; Crespo, Javier (Eds). Esteatosis hepàtica no alcohólica. A: Libro Blanco de la Hepatología en España. Cap. 3, 1ª Edición (en castellà). AEEH, 2015, Gen; pàgs: 189-194. ISBN 9788461737857 [Consulta: 9 octubre 2017]. Disponible a: http://aeeh.es/wp-content/uploads/2015/02/8f1dfdf8ff94bb6ed4bd1b41c5f363301.pdf Arxivat 2016-01-19 a Wayback Machine.
- Tirosh, Oren. Liver Metabolism and Fatty Liver Disease (en anglès). CRC Press, Taylor & Francis Group, 2014, Ag 27; pàgs: 338. ISBN 9781482212457 [Consulta: 27 octubre 2017].
