Telòmer
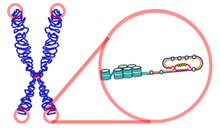
Un telòmer és una seqüència repetitiva de nucleòtids situada als extrems dels cromosomes lineals de la major part dels organismes eucariòtics, que serveix per a protegir aquests extrems de ser destruïts. El seu nom deriva dels mots grecs τἐλος telos ("final") i μέρος meros ("part").
Durant la divisió cel·lular, els enzims que dupliquen el cromosoma i el seu ADN no poden efectuar aquesta duplicació fins a la punta del cromosoma. Si les cèl·lules es dividissin sense telòmers, perdrien l'extrem dels cromosomes, juntament amb la informació necessària que conté (el 1972, James Watson donà a aquest fenomen el nom de "problema de replicació dels extrems"). El telòmer és un topall disposable, que és consumit durant la divisió cel·lular i que és recreat per un enzim, la telomerasa transcriptasa inversa,[1] codificat pel gen hTERT.[2]
Entre el 1975 i el 1977, Elizabeth Blackburn, que treballava després del seu doctorat a la Universitat Yale amb Joseph Gall,[3] descobrí estudiant l'estructura genètica del protozou Tetrahymena thermophila[4] la naturalesa inusual dels cromosomes, i el fet que les seves senzilles seqüències repetides d'ADN componien els extrems dels cromosomes. El seu treball fou publicat el 1978.[5] Blackburn, Greider i Szostak obtingueren conjuntament el Premi Nobel de Medicina o Fisiologia de 2009 per les seves investigacions sobre les característiques i funció dels telòmers i la telomerasa.[6]
L'acció fisiològica dels telòmers sol limitar les cèl·lules a un nombre determinat de divisions.[7] Estudis en animals i experiments emprant material de cultiu suggereixen que això és la causa de l'envelliment a nivell cel·lular i que afecta la longevitat.[8][9] La velocitat a la qual s'escurcen els seus telòmers és la que determina l'esperança de vida de cada espècie.[10] Cal tenir present, però, que en l'espècie humana els telòmers curts no són sempre perjudicials i que els telòmers llargs no comporten invariablement un avantatge biològic.[11][12]
S'ha observat que, tant en els humans[13] com en les aus, les diferències individuals en la longitud dels telòmers s'associen amb diferències individuals en el comportament. Hi ha experts que opinen que aquesta singular característica forma part del procés de selecció natural.[14]
Telòmers i salut[modifica]
Els telòmers eviten que els cromosomes d'una cèl·lula es fusionin o es recombinin. Aquestes anormalitats cromosòmiques podrien causar càncer, de manera que les cèl·lules són normalment destruïdes quan els telòmers són consumits. El mesurament in situ de la longitud dels telòmers és un mètode de biomarcatge amb valor pronòstic en determinats tipus de càncer,[15] com ara el melanoma[16] i altres neoplàsies malignes de pell no melanocítiques,[17] el càncer de pròstata,[18][19] el colorectal[20] o el de pulmó,[21] per esmentar alguns exemples. En la majoria de casos, el càncer és el resultat del fet que hi ha cèl·lules que s'escapen d'aquesta destrucció.[22] Els biòlegs especulen que aquest mecanisme és un intercanvi entre envelliment i càncer.[23] La importància dels telòmers en la salut és gran i existeix un ampli ventall d'anomalies mendelianes (síndromes d'escurçament telomèric o trastorns biològics dels telòmers, TBTs)[24] que inclou des de malalties multisistèmiques infantils a patologies locals aïllades en adults.[25] Fins ara, es coneixen mutacions causants de TBTs en almenys onze gens, cadascuna d'elles relacionada amb algun aspecte dels complexos processos de manteniment d'aquestes estructures cromosòmiques.[26]
Moltes cèl·lules tumorals desenvolupen canvis per evitar l'escurçament dels telòmers.[27] La majoria empra processos de reactivació de la telomerasa que mantenen la seva longitud. Algunes aconsegueixen aturar la senescència allargant-los a través de vies alternatives no relacionades amb dit enzim, com la inactivació de certes proteïnes.[28] El càncer tiroidal és un exemple paradigmàtic de la importància de la desregulació telomèrica en la gènesi i progressió de les neoplàsies malignes. Les mutacions en el gen TERT són unes de les anomalies genètiques més comunes observades en els tumors agressius de la tiroide, en particular les que modifiquen la codificació del component catalític central de la telomerasa. Per regla general, s'associen amb una major expressivitat del gen i de l'activitat de la telomerasa i, si bé no sempre van acompanyades d'un increment de la longitud dels telòmers, estan estretament relacionades amb el mal pronòstic, la disseminació metastàtica i la baixa supervivència global dels pacients.[29]
En les cirrosis criptogèniques[30] i les derivades d'hepatitis B/C s'observa una reducció de la mida dels telòmers dels limfòcits perifèrics, un fenomen indicatiu de la continua destrucció i regeneració dels nòduls parenquimatosos propis d'aquestes afeccions hepàtiques.[31] S'ha comprovat que diverses malalties víriques cròniques produeixen canvis topogràficament selectius en l'ADN de les cèl·lules T, causants de danys als seus telòmers amb la conseqüent pèrdua de longevitat d'aquestes cèl·lules. Es creu que el fet forma part dels mecanismes de desregulació del sistema immunitari utilitzats pels virus patògens.[32]
La longitud dels telòmers s'associa amb diverses malalties dels pulmons, com ara la pneumonitis crònica per hipersensibilitat o la bronquiolitis obliterant.[33] En el cas de la fibrosi pulmonar idiopàtica (FPI) es troben telòmers molt curts en els pneumòcits tipus II -cèl·lules fonamentals per la correcta regeneració de l'epiteli alveolar[34]- de les zones fibròtiques. La curtedat telomèrica està directament relacionada amb el temps de supervivència dels malalts que sofreixen aquesta patologia pulmonar.[35] En el 8–15% de FPIs de tipus familiar i en més del 11% de FPIs esporàdiques necessitades de trasplantament pulmonar s'han identificat mutacions en gens relacionats amb la telomerasa, com ara el TERT,[36] el RTEL1[37] o el PARN.[38] Inclús en individus afectes de FPI sense mutacions identificables presenten telòmers més curts que els dels grups de control, un fet motiu d'estudi i atribuït presumptivament a l'existència de variants encara no caracteritzades.[39]
També ha estat demostrada una correlació entre la longitud telomèrica i la gravetat de la cardiomiopatia hipertròfica, especialment en la forma obstructiva de la malaltia.[40] A més, s'ha comprovat l'existència d'un escurçament significatiu en els telòmers dels miocardiòcits de les persones afectes de cardiomiopaties de naturalesa genètica, com ara la que es desenvolupa en la distròfia muscular de Duchenne,[41] provocat per defectes hereditaris en proteïnes cardíaques essencials per una correcta funcionalitat contràctil de l'òrgan.[42] A banda d'això, se sap que durant el procés d'envelliment els cardiomiòcits humans i murins adquireixen un fenotip post-mitosi caracteritzat per un dany permanent de l'ADN telomèric a causa de disfuncions mitocondrials i que té lloc amb independència del nombre de divisions cel·lulars i de la longitud dels telòmers. El fenotip miocardiocitari associat amb la senescència resultant d'aquest dany és de tipus no canònic, pro-fibròtic i pro-hipertròfic.[43]
Determinades variacions en la telomerasa transcriptasa inversa materna s'associen amb la ruptura prematura de membranes i el part preterme.[44] Per una altra banda, l'exposició de la mare a diversos contaminants atmosfèrics durant el tercer trimestre de l'embaràs pot ocasionar un escurçament dels telòmers en el nounat,[45] de la mateixa manera que ho fa el tabaquisme matern.[46] També se sap que elevades concentracions ambientals de diversos metalls tòxics alteren la longitud relativa dels telòmers materns i fetals.[47]
Alguns especialistes afirmen que existeix una relació entre el desgast prematur dels telòmers i la síndrome de fatiga crònica i proposen que aquesta condició s'inclogui dins de la llista de malalties originades per un envelliment accelerat.[48] S'ha demostrat l'existència d'una associació negativa entre la depressió unipolar greu,[49] el trastorn bipolar[50] i la longitud telomèrica. L'escurçament dels telòmers podria també estar involucrat en altres patologies mentals[51][52] Segons indiquen estudis de neuroimatge funcional,[53] la longitud dels telòmers té una relació molt estreta amb l'activitat de diverses zones cerebrals implicades en el processament de les emocions.[54]
En la síndrome de Werner (un trastorn autosòmic recessiu rar, anomenat també progèria de l'adult i que comporta un alt risc de sofrir alguns càncers),[55] causat per mutacions en el gen WRN[56] codificador de la proteïna WRN (un membre de la família de les helicases RecQ);[57] la inestabilitat del genoma cel·lular depèn directament de la disfunció dels telòmers. Diverses línies d'evidència indiquen que els telòmers són substrats fisiològics de la WRN i que el seu manteniment aberrant en cas d'absència de dita proteïna és un important mecanisme patogènic causal dels fenotips progeroides de les persones amb la síndrome.[58][59]
La disqueratosi congènita (DC), o síndrome de Zinsser-Engman-Cole, és una genodermatosi descrita per primera vegada l'any 1906 i caracteritzada clàssicament per una triada clínica: leucoplàquia oral, distròfia unguial i hiperpigmentació reticular cutània.[60] Té un patró hereditari recessiu i lligat al sexe (cromosoma X). Molts malalts amb DC desenvolupen alguna forma de neoplàsia relacionada amb un augment de la divisió cel·lular. La seva causa fonamental és un defecte en el gen DKC1,[61] codificador de la proteïna disquerina,[62] la qual està fortament implicada en el manteniment de la longitud telomèrica. En la DC també s'han descrit mutacions en els gens TINF2,[63] TERC,[64] TERT,[65] C16orf57,[66] NOLA2,[67] NOLA3,[68] WRAP53/TCAB1,[69] i RTEL1.[70] Una variant molt greu de la DC, la síndrome de Hoyeraal-Hreidarsson,[71] cursa, a més a més, amb pancitopènia progressiva (disminució simultània dels valors de les tres sèries hematològiques: glòbuls blancs, glòbuls vermells i plaquetes), hipoplàsia del cerebel, microcefàlia i retard del creixement. Aquesta síndrome presenta, a banda de les moltes que comparteix amb la DC, determinades mutacions en els gens RTEL1 i DKC1 -els quals tenen funcions addicionals no relacionades amb els telòmers- que podrien ser l'origen de les seves manifestacions específiques.[72]
En la síndrome de Coats plus,[73] mutacions en el gen STN1 (membre del complex gènic CTC1–STN1–TEN1 humà)[74] provoquen una greu telomeropatia estructural i funcional.[75]
S'ha observat un escurçament telomèric significatiu en malalts afectes d'anèmia aplàstica de gravetat diversa i temps d'evolució diferent. Existeixen evidències que relacionen l'augment de l'erosió dels telòmers amb la progressió de la malaltia. Una part important de dita erosió té lloc a nivell de les cèl·lules mare hematopoètiques comprometent tant la fracció granulocítica com la mononuclear (monòcits i limfòcits), encara que és més accentuada en els granulòcits.[76] Es creu que la senescència de les esmentades cèl·lules hematopoètiques és el fenomen patofisiològic que condiciona l'aparició dels fenòmens de mielodisplàsia i d'hemoglobinúria paroxística nocturna propis dels casos avançats d'anèmia aplàstica.[77] Estudis en murins indiquen que la teràpia gènica restaura la longitud del telòmers, millora l'aplàsia medul·lar i augmenta la supervivència dels individus. Això suggereix que dita teràpia s'ha de considerar una nova opció pel tractament d'aquesta gravíssima forma d'anèmia[78] i el d'altres patologies d'índole molt dispar.[79] En els individus que pateixen anèmia de Fanconi també s'han apreciat diverses anomalies telomèriques (escurçament, increment de les fusions terminals, pèrdues o ruptures estructurals en els telòmers dels leucòcits perifèrics)[80]
No totes les malalties derivades d'imperfeccions en els telòmers es deuen a l'escurçament d'aquests. Diversos càncers de naturalesa familiar tenen el seu origen en mutacions que augmenten la longitud telomèrica.[81]
En casos de síndrome de l'ovari poliquístic, l'endocrinopatia més comuna entre les dones en edat reproductiva, s'ha detectat una longitud excessiva en els telòmers de les cèl·lules fol·liculars.[82]
Hi ha autors que posen l'accent en la importància de la dieta i de l'exercici moderat per mantenir una correcta funcionalitat dels telòmers.[83] En particular, s'associa la dieta mediterrània amb una major longitud telomèrica leucocitària.[84] Sumàriament, es pot dir que aquells nutrients, aliments i patrons dietètics considerats beneficiosos o perjudicials per a la salut cardiovascular i la progressió d'altres malalties cròniques relacionades amb l'edat també tenen els mateixos efectes sobre la longitud dels telòmers.[85]
Quantificació[modifica]
A l'hora d'efectuar qualsevol tipus d'estudi relacionat amb els telòmers cal aplicar procediments de laboratori fiables que possibilitin quantificar la seva longitud.[86] Habitualment, s'empren mètodes biomoleculars per fer-ho. Entre els més comuns estan la Southern blot, la citometria de flux amb hibridació in situ per fluorescència i la PCR en temps real (qPCR).[87] L'ús de la qPCR és preferible quan es fan avaluacions en poblacions amb un gran nombre d'individus, però per assolir resultats òptims són necessaris uns protocols de treball homogenis i ben definits.[88]
Darreres investigacions[modifica]
Un estudi realitzat per especialistes de la Universitat Johns Hopkins indica que l'anàlisi de la longitud telomèrica en un àmbit hospitalari, emprant de forma combinada la citometria de flux i la hibridació in situ per fluorescència (flowFISH)[89] com a element diagnòstic, pot ser útil per millorar les decisions terapèutiques en diversos supòsits clínics.[90]
Investigadors xinesos consideren que la longitud dels telòmers és un potencial biomarcador per predir el risc i el pronòstic de l'ictus.[91]
Per compilar i oferir als investigadors una base de dades dels gens implicats en el manteniment telomèric d'humans i llevats, ha estat creada la pàgina web TelNet,[92] amb el suport del consorci interdisciplinari de recerca alemany CancerTelSys.
S'han creat procediments bioinformàtics per identificar les característiques detallades dels telòmers en l'estudi de genomes nous, els quals fan possible aconseguir resultats d'una forma més senzilla i ràpida que la aconseguida amb les tècniques emprades habitualment.[93] Un equip del Centre Alemany de Recerca Oncològica de Heidelberg ha desenvolupat un nou programari de disposició lliure sota la llicència GPL, anomenat TelomereHunter, que permet una caracterització in silico molt precisa dels mecanismes de manteniment dels telòmers en el genoma i amb la capacitat d'analitzar grans cohorts de genomes cancerosos, proporcionant així una àmplia varietat de dades amb valor diagnòstic.[94]
Avui dia, es segueixen múltiples línies de treball dirigides a controlar l'activitat de la telomerasa en les neoplàsies malignes, com ara l'ús d'inhibidors de la telomerasa com medicaments anticancerosos,[95] el desenvolupament de fàrmacs que actuïn sobre l'ADN telomèric, la cerca de vectors vírics capaços de transportar promotors de la telomerasa transcriptasa inversa o la creació de mètodes immunoteràpics que activin aquest enzim.[96] A hores d'ara, se sap que la telomerasa té moltes funcions extratelomèriques encara per determinar i que la seva inhibició total pot induir danys greus i imprevisibles en les mitocòndries de les cèl·lules sanes. Aquest és un fet importantíssim a tenir en compte quan es dissenyen noves estratègies terapèutiques contra el càncer relacionades amb els telòmers.[97]
Referències[modifica]
- ↑ UniProt «Telomerase reverse transcriptase» (en anglès). Protein knowledgebase. UniProt Consortium, 2019 Des 11; O14746 -TERT_HUMAN- (rev), pàgs: 19 [Consulta: 16 febrer 2020].
- ↑ Bryce LA, Morrison N, Hoare SF, Muir S, Keith WN «Mapping of the gene for the human telomerase reverse transcriptase, hTERT, to chromosome 5p15.33 by fluorescence in situ hybridization» (en anglès). Neoplasia, 2000 Maig-Jun; 2 (3), pp: 197-201. ISSN 1476-5586. PMC: 1507564. PMID: 10935505 [Consulta: 16 maig 2018].
- ↑ Carnegie Institution for Science «Joseph Gall» (en anglès). Faculty, Department of Embryology, 2019, pàgs: 6 [Consulta: 10 juliol 2019].
- ↑ Collins, K; Gorovsky, M «Tetrahymena thermophila» (en anglès). Curr Biol, 2005 Maig 10; 15 (9), pp: R317-R318. ISSN 0960-9822. DOI: 10.1016/j.cub.2005.04.039. PMID: 15886083 [Consulta: 11 febrer 2020].
- ↑ Blackburn EH, Gall JG «A tandemly repeated sequence at the termini of the extrachromosomal ribosomal RNA genes in Tetrahymena» (en anglès). J Mol Biol, 1978 Mar 25; 120 (1), pp: 33-53. ISSN 0022-2836. PMID: 642006 [Consulta: 11 setembre 2018].
- ↑ Nobel Media AB «The Nobel Prize in Physiology or Medicine 2009» (en anglès). Press release, NobelPrize.org, 2009; Oct 5, pàgs: 12 [Consulta: 14 juliol 2018].
- ↑ Londoño-Vallejo JA, Wellinger RJ «Telomeres and telomerase dance to the rhythm of the cell cycle» (en anglès). Trends Biochem Sci, 2012 Set; 37 (9), pp: 391-399. ISSN 0968-0004. DOI: 10.1016/j.tibs.2012.05.004. PMID: 22727244 [Consulta: 3 març 2020].
- ↑ López-Otín C, Blasco MA, Partridge L, Serrano M, Kroemer G «The hallmarks of aging» (en anglès). Cell, 2013 Jun 6; 153 (6), pp: 1194-1217. DOI: 10.1016/j.cell.2013.05.039. PMC: 3836174. PMID: 23746838 [Consulta: 11 setembre 2018].
- ↑ Blasco, MA «Telomere length, stem cells and aging» (en anglès). Nat Chem Biol, 2007 Oct; 3 (10), pp: 640-649. DOI: 10.1038/nchembio.2007.38. ISSN: 0092-8674. PMID: 17876321 [Consulta: 11 setembre 2018].
- ↑ Whittemore, K; Vera, E; Martínez-Nevado, E; Sanpera, C; Blasco, MA «Telomere shortening rate predicts species life span» (en anglès). PNAS, 2019 Jul 23; 116 (30), pp: 15122-15127. PMID: 31285335. DOI: 10.1073/pnas.1902452116. PMC: 6660761 [Consulta: 5 setembre 2020].
- ↑ Aviv A, Shay JW «Reflections on telomere dynamics and ageing-related diseases in humans» (en anglès). Philos Trans R Soc Lond B Biol Sci, 2018 Mar 5; 373 (1741), pii: 20160436. DOI: 10.1098/rstb.2016.0436. PMC: 5784057. PMID: 29335375 [Consulta: 19 juliol 2019].
- ↑ Ferrucci L, Gonzalez-Freire M, Fabbri E1, Simonsick E, et al «Measuring biological aging in humans: A quest» (en anglès). Aging Cell, 2020 Feb; 19 (2), pp: e13080. DOI: 10.1111/acel.13080. PMC: 6996955. PMID: 31833194 [Consulta: 18 abril 2020].
- ↑ Epel, ES «Telomeres in a Life-Span Perspective: A New Psychobiomarker?» (en anglès). Curr Dir Psychol Sci, 2009 Feb 1; 18 (1), pp: 6-10. ISSN 1467-8721. DOI: 10.1111/j.1467-8721.2009.01596.x [Consulta: 3 març 2020].
- ↑ Bateson M, Nettle D «Why are there associations between telomere length and behaviour?» (en anglès). Philos Trans R Soc Lond B Biol Sci, 2018 Mar 5; 373 (1741), pii: 20160438. DOI: 10.1098/rstb.2016.0438. PMC: 5784059. PMID: 29335363 [Consulta: 23 juliol 2019].
- ↑ Okamoto, K; Seimiya, H «Revisiting Telomere Shortening in Cancer» (en anglès). Cells, 2019 Feb; 8 (2), pp: 107. DOI: 10.3390/cells8020107. PMC: 6406355. PMID: 30709063 [Consulta: 23 maig 2020].
- ↑ Rachakonda S, Srinivas N, Mahmoudpour SH, Garcia-Casado Z, et al «Telomere length and survival in primary cutaneous melanoma patients» (en anglès). Sci Rep, 2018 Jul 19; 8 (1), pp: 10947. DOI: 10.1038/s41598-018-29322-9. PMC: 6053393. PMID: 30026606 [Consulta: 10 maig 2020].
- ↑ Yamada-Hishida H, Nobeyama Y, Nakagawa H «Correlation of telomere length to malignancy potential in non-melanoma skin cancers» (en anglès). Oncol Lett, 2018 Gen; 15 (1), pp: 393-399. DOI: 10.3892/ol.2017.7278. PMC: 5738687. PMID: 29285197 [Consulta: 10 maig 2020].
- ↑ Meeker, AK «Cancer telomeres and white crows» (en anglès). Am J Clin Exp Urol, 2018 Abr 1; 6 (2), pp: 93-100. ISSN 2330-1910. PMC: 5902727. PMID: 29666837 [Consulta: 16 maig 2018].
- ↑ Xu J, Chang WS, Tsai CW, Bau DT, et al «Leukocyte telomere length is associated with aggressive prostate cancer in localized prostate cancer patients» (en anglès). EBioMedicine, 2020 Feb; 52, pp: 102616. DOI: 10.1016/j.ebiom.2019.102616. PMC: 6992931. PMID: 31981976 [Consulta: 28 febrer 2020].
- ↑ Engelhardt M, Drullinsky P, Guillem J, Moore MA «Telomerase and telomere length in the development and progression of premalignant lesions to colorectal cancer» (en anglès). Clin Cancer Res, 1997 Nov; 3 (11), pp: 1931-1941. ISSN 1078-0432. PMID: 9815582 [Consulta: 10 març 2020].
- ↑ Doherty JA, Grieshober L, Houck JR, Barnett MJ, et al «Telomere Length and Lung Cancer Mortality among Heavy Smokers» (en anglès). Cancer Epidemiol Biomarkers Prev, 2018 Jul; 27 (7), pp: 829-837. DOI: 10.1158/1055-9965.EPI-17-1183. PMC: 6035074. PMID: 29743162 [Consulta: 10 març 2020].
- ↑ Boukamp P, Mirancea N «Telomeres rather than telomerase a key target for anti-cancer therapy?» (en anglès). Exp Dermatol, 2007 Gen; 16 (1), pp: 71-79. ISSN 1600-0625. DOI: 10.1111/j.1600-0625.2006.00517.x. PMID: 17181645 [Consulta: 16 maig 2018].
- ↑ Harrison's Principles of Internal Medicine, 16th Edition. Chap. 69: Cancer cell biology and angiogenesis, Robert G. Fenton i Dan L. Longo; 2005, pàg. 454. ISBN 9780071402354
- ↑ Bertuch, AA «The molecular genetics of the telomere biology disorders» (en anglès). RNA Biol, 2016 Aug 2; 13 (8), pp: 696-706. DOI: 10.1080/15476286.2015.1094596. PMC: 4993306. PMID: 26400640 [Consulta: 10 març 2020].
- ↑ Holohan B, Wright WE, Shay JW «Cell biology of disease: Telomeropathies: an emerging spectrum disorder» (en anglès). J Cell Biol, 2014 Maig 12; 205 (3), pp: 289-299. DOI: 10.1083/jcb.201401012. PMC: 4018777. PMID: 24821837 [Consulta: 16 febrer 2020].
- ↑ Savage, SA «Beginning at the ends: telomeres and human disease» (en anglès). F1000Res, 2018 Maig 1; 7, pii: F1000 Faculty Rev-524. DOI: 10.12688/f1000research.14068.1. PMC: 5931273. PMID: 29770205 [Consulta: 25 maig 2018].
- ↑ Barrett JH, Iles MM, Dunning AM, Pooley KA «Telomere length and common disease: study design and analytical challenges» (en anglès). Hum Genet, 2015 Jul; 134 (7), pp: 679-689. DOI: 10.1007/s00439-015-1563-4. PMC: 4460268. PMID: 25986438 [Consulta: 3 març 2020].
- ↑ Gaspar TB, Sá A, Lopes JM8, Sobrinho-Simões M, et al «Telomere Maintenance Mechanisms in Cancer» (en anglès). Genes (Basel), 2018 Maig 3; 9 (5), pii: E241. ISSN 2073-4425. DOI: 10.3390/genes9050241. PMID: 29751586 [Consulta: 19 maig 2018].
- ↑ Donati B, Ciarrocchi A «Telomerase and Telomeres Biology in Thyroid Cancer» (en anglès). Int J Mol Sci, 2019 Jun 13; 20 (12), pii: E2887. ISSN 1422-0067. DOI: 10.3390/ijms20122887. PMID: 31200515 [Consulta: 11 juliol 2019].
- ↑ Mercado-Irizarry A, Torres EA «Cryptogenic cirrhosis: Current knowledge and future directions» (en anglès). Clin Liver Dis (Hoboken), 2016 Abr 27; 7 (4), pp: 69-72. DOI: 10.1002/cld.539. PMC: 6490261. PMID: 31041033 [Consulta: 7 maig 2020].
- ↑ Laish I, Mari A, Mannasse B, Hadary R, et al «Telomere Length, Aggregates, and Capture in Cirrhosis» (en anglès). Isr Med Assoc J, 2018 Maig; 5 (20), pp: 295-299. ISSN 1565-1088. PMID: 29761675 [Consulta: 21 maig 2018].
- ↑ Ji Y, Dang X, Nguyen LNT, Nguyen LN, et al «Topological DNA damage, telomere attrition and T cell senescence during chronic viral infections» (en anglès). Immun Ageing, 2019 Jun 24; 16, pp: 12. DOI: 10.1186/s12979-019-0153-z. PMC: 6591813. PMID: 31285747 [Consulta: 13 juliol 2019].
- ↑ Everaerts S, Lammertyn EJ, Martens DS, De Sadeleer L, et al «The aging lung: tissue telomere shortening in health and disease» (en anglès). Respir Res, 2018 Maig 11; 19 (1), pp: 95. DOI: 10.1186/s12931-018-0794-z. PMC: 5948770. PMID: 29751799 [Consulta: 23 maig 2018].
- ↑ NTP/NIH «Lung-Regeneration» (en anglès). Nonneoplastic Lesion Atlas, 2015; Des 7 (rev), pàgs: 3 [Consulta: 23 maig 2018].
- ↑ Snetselaar R, van Batenburg AA, van Oosterhout MFM2 Kazemier KM, et al «Short telomere length in IPF lung associates with fibrotic lesions and predicts survival» (en anglès). PLoS One, 2017 Des 27; 12 (12), pp: e0189467. DOI: 10.1371/journal.pone.0189467. PMC: 5744955. PMID: 29281671 [Consulta: 23 maig 2018].
- ↑ Bilgili H, Białas AJ, Górski P, Piotrowski WJ «Telomere Abnormalities in the Pathobiology of Idiopathic Pulmonary Fibrosis» (en anglès). J Clin Med, 2019 Ag 16; 8 (8), pii: E1232. DOI: 10.3390/jcm8081232. PMC: 6723768. PMID: 31426295 [Consulta: 23 maig 2018].
- ↑ Genetics Home Reference «RTEL1 gene» (en anglès). NIH, US National Library of Medicine, 2018; Set 11, pàgs: 4 [Consulta: 16 setembre 2018].
- ↑ Genetics Home Reference «PARN gene» (en anglès). NIH, US National Library of Medicine, 2018; Set 11, pàgs: 4 [Consulta: 16 setembre 2018].
- ↑ McDonough JE, Martens DS, Tanabe N, Ahangari F, et al «A role for telomere length and chromosomal damage in idiopathic pulmonary fibrosis» (en anglès). Respir Res, 2018 Jul 9; 19 (1), pp: 132. DOI: 10.1186/s12931-018-0838-4. PMC: 6038197. PMID: 29986708 [Consulta: 16 setembre 2018].
- ↑ Chatterjee S, de Gonzalo-Calvo D, Derda AA, Schimmel K, et al «Leukocyte telomere length correlates with hypertrophic cardiomyopathy severity» (en anglès). Sci Rep, 2018 Jul 25; 8 (1), pp: 11227. DOI: 10.1038/s41598-018-29072-8. PMC: 6060137. PMID: 30046139 [Consulta: 14 setembre 2018].
- ↑ Mourkioti, F; Kustan, J; Kraft, P; Day, JW; et al «Role of Telomere Dysfunction in Cardiac Failure in Duchenne Muscular Dystrophy» (en anglès). Nat Cell Biol, 2013 Ag; 15 (8), pp: 895-904. PMID: 23831727. DOI: 10.1038/ncb2790. PMC: 3774175 [Consulta: 5 setembre 2020].
- ↑ Chang ACY, Chang ACH, Kirillova A, Sasagawa K, et al «Telomere shortening is a hallmark of genetic cardiomyopathies» (en anglès). Proc Natl Acad Sci USA, 2018 Set 11; 115 (37), pp: 9276-9281. ISSN 1091-6490. DOI: 10.1073/pnas.1714538115. PMID: 30150400 [Consulta: 19 setembre 2018].
- ↑ Anderson R, Lagnado A, Maggiorani D, Walaszczyk A, et al «Length-independent telomere damage drives post-mitotic cardiomyocyte senescence» (en anglès). EMBO J, 2019 Mar 1; 38 (5), pii: e100492. DOI: 10.15252/embj.2018100492. PMC: 6140486. PMID: 30150400 [Consulta: 12 juliol 2019].
- ↑ Marrs C, Chesmore K, Menon R, Williams S «Maternal human telomerase reverse transcriptase variants are associated with preterm labor and preterm premature rupture of membranes» (en anglès). PLoS One, 2018 Maig 17; 13 (5), pp: e0195963. ISSN 1932-6203. DOI: 10.1371/journal.pone.0195963. PMID: 29771920 [Consulta: 21 maig 2018].
- ↑ Song L, Zhang B, Liu B, Wu M, et al «Effects of maternal exposure to ambient air pollution on newborn telomere length» (en anglès). Environ Int, 2019 Jul; 128, pp: 254-260. ISSN 1873-6750. DOI: 10.1016/j.envint.2019.04.064. PMID: 31059920 [Consulta: 10 juliol 2019].
- ↑ Werlang ICR, Hahn MC, Bernardi JR, Nast M, et al «Exposure to different intrauterine environments: implications for telomere attrition in early life» (en anglès). J Matern Fetal Neonatal Med, 2019 Nov; 32 (21), pp: 3675-3684. DOI: 10.1080/14767058.2018.1468879. ISSN: 1476-7058. PMID: 29681194 [Consulta: 7 febrer 2020].
- ↑ Herlin M, Broberg K, Igra AM, Li H, et al «Exploring telomere length in mother-newborn pairs in relation to exposure to multiple toxic metals and potential modifying effects by nutritional factors» (en anglès). BMC Med, 2019 Abr 11; 17 (1), pp: 77. DOI: 10.1186/s12916-019-1309-6. PMC: 6458832. PMID: 30971237 [Consulta: 11 juliol 2019].
- ↑ Rajeevan MS, Murray J, Oakley L, Lin JS, Unger ER «Association of chronic fatigue syndrome with premature telomere attrition» (en anglès). J Transl Med, 2018 Feb 27; 16 (1), pp: 44. DOI: 10.1186/s12967-018-1414-x. PMC: 5830066. PMID: 29486769 [Consulta: 25 maig 2018].
- ↑ Ridout KK, Ridout SJ, Price LH, Sen S, Tyrka AR «Depression and Telomere Length: A Meta-Analysis» (en anglès). J Affect Disord, 2016 Feb; 191, pp: 237-247. DOI: 10.1016/j.jad.2015.11.052. PMC: 4760624. PMID: 26688493 [Consulta: 19 juliol 2018].
- ↑ Powell TR, Dima D, Frangou S, Breen G «Telomere Length and Bipolar Disorder» (en anglès). Neuropsychopharmacology, 2018 Gen; 43 (2), pp: 445-453. DOI: 10.1038/npp.2017.125. PMC: 5729555. PMID: 28621334 [Consulta: 21 febrer 2018].
- ↑ Mora Solano, Á «La longitud dels telòmers, un marcador de la qualitat de vida i de l'envelliment: implicació en els trastorns mentals». Treballs de la Societat Catalana de Biologia, 2019; 68, pp: 56-57. ISSN 2013-9802 [Consulta: 6 febrer 2020].
- ↑ Muneer, A; Minhas, FA «Telomere Biology in Mood Disorders: An Updated, Comprehensive Review of the Literature» (en anglès). Clin Psychopharmacol Neurosci, 2019 Ag 31; 17 (3), pp: 343-363. DOI: 10.9758/cpn.2019.17.3.343. PMC: 6705109. PMID: 31352701 [Consulta: 6 setembre 2020].
- ↑ Rodríguez-Carvajal, J «Neuroimagen funcional. Combinación de anatomía y fisiología» (en anglès). Gac Méd Méx, 2002 Maig-Jun; 138 (3), pp: 247-258. ISSN 0016-3813 [Consulta: 21 febrer 2018].
- ↑ Powell TR, De Jong S, Breen G, Lewis CM, Dima D «Telomere length as a predictor of emotional processing in the brain» (en anglès). Hum Brain Mapp, 2019 Abr 15; 40 (6), pp: 1750-1759. DOI: 10.1002/hbm.24487. PMC: 6492163. PMID: 30511786 [Consulta: 21 febrer 2020].
- ↑ Hisama, F; Martin, G; Oshima, J «Síndrome de Werner» (en anglès). Orphanet, 2012 Abr; ORPHA:902 (rev), pàgs: 5 [Consulta: 7 maig 2020].
- ↑ Genetics Home Reference «WRN gene» (en anglès). NIH, US National Library of Medicine, 2018; Maig 22 (rev), pàgs: 7 [Consulta: 25 maig 2018].
- ↑ UniProt «Werner syndrome ATP-dependent helicase» (en anglès). Protein knowledgebase. UniProt Consortium, 2019 Abr 22; Q14191 -WRN_HUMAN- (rev), pàgs: 21 [Consulta: 7 maig 2020].
- ↑ Crabbe L, Jauch A, Naeger CM, Holtgreve-Grez H, Karlseder J «Telomere dysfunction as a cause of genomic instability in Werner syndrome» (en anglès). Proc Natl Acad Sci USA, 2007 Feb 13; 104 (7), pp: 2205-2210. DOI: 10.1073/pnas.0609410104. PMC: 1794219. PMID: 17284601 [Consulta: 25 maig 2018].
- ↑ Oshima J, Sidorova JM, Monnat RJ Jr «Werner syndrome: Clinical features, pathogenesis and potential therapeutic interventions» (en anglès). Ageing Res Rev, 2017 Gen; 33, pp: 105-114. DOI: 10.1016/j.arr.2016.03.002. PMC: 5025328. PMID: 26993153 [Consulta: 25 maig 2018].
- ↑ Savage, SA; Agarwal, S; Tolar, J; Calado, RT; Bertuch, AA «Dyskeratosis Congenita and Telomere Biology Disorders: Diagnosis and Management Guidelines» (en anglès). Dyskeratosis Congenital Outreach, Inc. (Savage SA, Cook EF; Eds.), 2015 Gen; First Edition, pàgs: 446 [Consulta: 16 febrer 2020].
- ↑ Genetics Home Reference «DKC1 gene (dyskerin pseudouridine synthase 1)» (en anglès). NIH, US National Library of Medicine, 2020; Ag 17 (rev), pàgs: 6 [Consulta: 5 setembre 2020].
- ↑ UniProt «Dyskerin» (en anglès). Protein knowledgebase. UniProt Consortium, 2016 Jul 6; O95940 -O95940_HUMAN- (rev), pàgs: 2 [Consulta: 20 setembre 2018].
- ↑ Genetics Home Reference «TINF2 gene (TERF1 interacting nuclear factor 2)» (en anglès). NIH, US National Library of Medicine, 2020; Abr 15 (rev), pàgs: 5 [Consulta: 17 abril 2020].
- ↑ Genetics Home Reference «TERC gene (telomerase RNA component)» (en anglès). NIH, US National Library of Medicine, 2020; Abr 15 (rev), pàgs: 7 [Consulta: 17 abril 2020].
- ↑ LOVD «TERT gene homepage» (en anglès). Leiden University Medical Center, 2020; Mar 30 (rev), pàgs: 1 [Consulta: 17 abril 2020].
- ↑ Genetics Home Reference «USB1 / U6 snRNA biogenesis phosphodiesterase 1 -Homo sapiens (human)-» (en anglès). NIH, US National Library of Medicine, 2020; Mar 28 (rev), pàgs: 8 [Consulta: 2 maig 2020].
- ↑ Kniffin, CL; Converse, PJ «Nucleolar Protein Family A, member 2; NOLA2» (en anglès). OMIM, 2009 Jun 30; 606470 (rev), pàgs: 3 [Consulta: 2 maig 2020].
- ↑ Tiller, GE; Converse, PJ «Nucleolar Protein Family A, member 3; NOLA3» (en anglès). OMIM, 2008 Oct 14; 606471 (rev), pàgs: 3 [Consulta: 2 maig 2020].
- ↑ Gene «WRAP53» (en anglès). NCBI, US National Library of Medicine, 2020 Mar 15; ID55135 (rev), pàgs: 7 [Consulta: 2 maig 2020].
- ↑ Garofola C, Gross GP «Dyskeratosis Congenita» (en anglès). StatPearls [Internet]. StatPearls Publishing LLC, 2018 Jun 19; NBK507710 (rev), pàgs: 5. PMID: 29939532 [Consulta: 20 setembre 2018].
- ↑ Boltshauser, E «Síndrome de Hoyeraal-Hreidarsson» (en anglès). Orphanet, 2019 Ag; ORPHA:3322 (rev), pàgs: 4 [Consulta: 5 setembre 2020].
- ↑ Glousker G, Touzot F, Revy P, Tzfati Y, Savage SA «Unraveling the Pathogenesis of Hoyeraal-Hreidarsson Syndrome, a Complex Telomere Biology Disorder» (en anglès). Br J Haematol, 2015 Ag; 170 (4), pp: 457–471. DOI: 10.1111/bjh.13442. PMC: 4526362. PMID: 25940403 [Consulta: 30 setembre 2018].
- ↑ Genetics Home Reference «Coats plus syndrome» (en anglès). NIH, US National Library of Medicine, 2019; Jul 9 (rev), pàgs: 5 [Consulta: 12 juliol 2018].
- ↑ UniProt «CST complex subunit STN1» (en anglès). Protein knowledgebase. UniProt Consortium, 2020 Ag 12; Q9H668 -STN1_HUMAN- (rev), pàgs: 10 [Consulta: 6 setembre 2020].
- ↑ Simon AJ, Lev A, Zhang Y, Weiss B, et al «Mutations in STN1 cause Coats plus syndrome and are associated with genomic and telomere defects» (en anglès). Int J Mol Sci, 2019 Jun 19; 20 (12), pii: E2996. ISSN 1422-0067. DOI: 10.3390/ijms20122996. PMID: 31248154 [Consulta: 30 setembre 2018].
- ↑ Moore CA, Krishnan K «Aplastic Anemia» (en anglès). StatPearls [Internet]. StatPearls Publishing LLC, 2019 Maig 14; NBK534212 (rev), pàgs: 6. PMID: 30480951 [Consulta: 10 març 2020].
- ↑ Ball SE, Gibson FM, Rizzo S, Tooze JA, et al «Progressive Telomere Shortening in Aplastic Anemia» (en anglès). Blood, 1998 Maig 15; 91 (10), pp: 3582-3592. DOI: 10.1182/blood.V91.10.3582. ISSN: 0006-4971. PMID: 9572992 [Consulta: 11 setembre 2018].
- ↑ Bär C, Povedano JM, Serrano R, Benitez-Buelga C, et al «Telomerase gene therapy rescues telomere length, bone marrow aplasia, and survival in mice with aplastic anemia» (en anglès). Blood, 2016 Abr 7; 127 (14), pp: 1770-1779. ISSN 0006-4971. DOI: 10.1182/blood-2015-08-667485. PMID: 26903545 [Consulta: 11 setembre 2018].
- ↑ Wong, JW; Yun, CO «Telomere Gene Therapy: Polarizing Therapeutic Goals for Treatment of Various Diseases» (en anglès). Cells, 2019 Maig; 8 (5), pp: 392. PMID: 31035374. DOI: 10.3390/cells8050392. PMC: 6563133 [Consulta: 23 maig 2019].
- ↑ Sarkar J, Liu Y «Fanconi anemia proteins in telomere maintenance» (en anglès). DNA Repair (Amst), 2016 Jul; 43, pp: 107-112. DOI: 10.1016/j.dnarep.2016.02.007. ISSN: 4917397. PMID: 27118469 [Consulta: 28 setembre 2018].
- ↑ Stanley SE, Armanios M «The short and long telomere syndromes: paired paradigms for molecular medicine» (en anglès). Curr Opin Genet Dev, 2015 Ag 1; 33, pp: 1-9. DOI: 10.1016/j.gde.2015.06.004. PMC: 4741306. PMID: 26232116 [Consulta: 5 octubre 2018].
- ↑ Wei D, Xie J, Yin B, Hao H, et al «Significantly lengthened telomere in granulosa cells from women with polycystic ovarian syndrome (PCOS)» (en anglès). J Assist Reprod Genet, 2017 Jul; 34 (7), pp: 861-866. DOI: 10.1007/s10815-017-0945-z. PMC: 5476553. PMID: 28502062 [Consulta: 5 octubre 2018].
- ↑
- ↑ Crous-Bou M, Fung TT, Prescott J, Julin B, et al «Mediterranean diet and telomere length in Nurses' Health Study: population based cohort study» (en anglès). BMJ, 2014 Des 2; 349, pp: g6674. DOI: 10.1136/bmj.g6674. PMC: 4252824. PMID: 25467028 [Consulta: 5 juny 2018].
- ↑ Marti A, Echeverría R, Morell-Azanza L, Ojeda-Rodríguez A «Telómeros y calidad de la dieta» (en castellà). Nutr Hosp, 2017 Oct 24; 34 (5), pp: 1226-1245. DOI: 10.20960/nh.1181. ISSN: 1699-5198. PMID: 29130723 [Consulta: 14 juliol 2018].
- ↑ Aubert G, Hills M, Lansdorp PM «Telomere length measurement-caveats and a critical assessment of the available technologies and tools» (en anglès). Mutat Res, 2012 Feb 1; 730 (1-2), pp: 59-67. PMID: 21663926. DOI: 10.1016/j.mrfmmm.2011.04.003. PMC: 3460641 [Consulta: 10 maig 2020].
- ↑ Montpetit AJ, Alhareeri AA, Montpetit M, Starkweather AR, et al «Telomere length: a review of methods for measurement» (en anglès). Nurs Res, 2014 Jul-Ag; 63 (4), pp: 289-299. DOI: 10.1097/NNR.0000000000000037. PMC: 4292845. PMID: 24977726 [Consulta: 23 abril 2020].
- ↑ Joglekar MV, Satoor SN, Wong WKM, Cheng F, et al «An Optimised Step-by-Step Protocol for Measuring Relative Telomere Length» (en anglès). Methods Protoc, 2020 Abr 3; 3 (2), pii: E27. ISSN 2409-9279. DOI: 10.3390/mps3020027. PMID: 32260112 [Consulta: 23 abril 2020].
- ↑ Dejong, G «What is Flow FISH telomere testing?» (en anglès). RepeatDX, 2019; Ag 30, pàgs: 4 [Consulta: 11 febrer 2020].
- ↑ Alder JK, Hanumanthu VS, Strong MA, DeZern AE, et al «Diagnostic utility of telomere length testing in a hospital-based setting» (en anglès). Proc Natl Acad Sci USA, 2018 Mar 6; 115 (10), pp: E2358-E2365. DOI: 10.1073/pnas.1720427115. PMC: 5877993. PMID: 29463756 [Consulta: 28 setembre 2018].
- ↑ Tian Y, Wang S, Jiao F, Kong Q, et al «Telomere Length: A Potential Biomarker for the Risk and Prognosis of Stroke» (en anglès). Front Neurol, 2019 Jun 13; 10, pp: 624. DOI: 10.3389/fneur.2019.00624. PMC: 6585102. PMID: 31263449 [Consulta: 9 juliol 2019].
- ↑ Braun DM, Chung I, Kepper N, Deeg KI, Rippe K «TelNet - a database for human and yeast genes involved in telomere maintenance» (en anglès). BMC Genet, 2018 Maig 18; 19 (1), pp: 32. DOI: 10.1186/s12863-018-0617-8. ISSN: 1471-2156. PMID: 29776332 [Consulta: 21 maig 2018].
- ↑ Somanathan I, Baysdorfer C «A bioinformatics approach to identify telomere sequences» (en anglès). Biotechniques, 2018 Jul; 65 (1), pp: 20-25. ISSN 0736-6205. DOI: 10.2144/btn-2018-0057. PMID: 30014738 [Consulta: 11 setembre 2018].
- ↑ Feuerbach L, Sieverling L, Deeg KI, Ginsbach P, et al «TelomereHunter - in silico estimation of telomere content and composition from cancer genomes» (en anglès). BMC Bioinformàtics, 2019 Maig 28; 20 (1), pp: 272. DOI: 10.1186/s12859-019-2851-0. PMC: 6540518. PMID: 31138115 [Consulta: 10 juliol 2019].
- ↑ Cunningham AP, Love WK, Zhang RW, Andrews LG, Tollefsbol TO «Telomerase inhibition in cancer therapeutics: molecular-based approaches» (en anglès). Curr Med Chem, 2006; 13 (24), pp: 2875-2888. DOI: 10.2174/092986706778521887. PMC: 2423208. PMID: 17073634 [Consulta: 28 febrer 2020].
- ↑ Mizukoshi E, Kaneko S «Telomerase-Targeted Cancer Immunotherapy» (en anglès). Int J Mol Sci, 2019 Abr 12; 20 (8), pii: E1823. DOI: 10.3390/ijms20081823. PMC: 6515163. PMID: 31013796 [Consulta: 15 juliol 2019].
- ↑ Ségal-Bendirdjian E, Geli V «Non-canonical Roles of Telomerase: Unraveling the Imbroglio» (en anglès). Front Cell Dev Biol, 2019 Des 10; 7, pp: 332. DOI: 10.3389/fcell.2019.00332. PMC: 6914764. PMID: 31911897 [Consulta: 7 febrer 2020].
Bibliografia[modifica]
- Calado, Rodrigo T.; Young, Neal S. Telomere Diseases (en anglès). N Engl J Med, 2009 Des 10; 361 (24), pp: 2353–2365. DOI 10.1056/NEJMra0903373 [Consulta: 9 setembre 2018].
- Cascales Angosto, María; Álvarez Gómez, Juan Ángel. Telómeros, Telomerasa, sus implicaciones en el envejecimiento y el càncer (en castellà). Anales de la Real Academia de Doctores de España, 2010; 14 (1), pp: 49-70. ISSN 1138-2414 [Consulta: 14 juliol 2019].
- Martínez, Paula; Blasco, Maria A. Telomere-driven diseases and telomere-targeting therapies (en anglès). J Cell Biol, 2017 Abr 3; 216 (4), pp: 875-887. ISSN 1540-8140. DOI 10.1083/jcb.201610111 [Consulta: 16 juliol 2019].
- Lai, Tsung-Po; Wright, Woodring E.; Shay, Jerry W. Comparison of telomere length measurement methods (en anglès). Philos Trans R Soc Lond B Biol Sci, 2018 Mar 5; 373 (1741), pii: 20160451. PMID: 29335378. DOI 10.1098/rstb.2016.0451 [Consulta: 17 maig 2020].
- Bhala, Sonia; Best, Ana F.; Giri, Neelam; Alter, Blanche P.; et al. CNS manifestations in patients with telomere biology disorders (en anglès). Neurol Genet, 2019 Oct 29; 5 (6), pp: 370. PMID: 31872047. DOI 10.1212/NXG.0000000000000370 [Consulta: 16 febrer 2020].
- Arish, Nissim; Petukhov, Dmytro; Wallach-Dayan, Shulamit B. The Role of Telomerase and Telomeres in Interstitial Lung Diseases: From Molecules to Clinical Implications (en anglès). Int J Mol Sci, 2019 Jun 19; 20 (12), pii: E2996. DOI 10.3390/ijms20122996 [Consulta: 12 juliol 2019].
- Wang, Stephanie; Madu, Chikezie O.; Lu, Yi. Telomere and Its Role in Diseases (en anglès). Oncomedicine, 2019 Gen 23; 4, pp: 1-9. ISSN 2206-6349. DOI 10.7150/oncm.28210 [Consulta: 20 juliol 2019].
- Srinivas, Nalini; Rachakonda, Sivaramakrishna; Kumar, Rajiv. Telomeres and Telomere Length: A General Overview (en anglès). Cancers (Basel), 2020 Mar; 12 (3), pp: 558. PMID: 32121056. DOI 10.3390/cancers12030558 [Consulta: 17 abril 2020].
Enllaços externs[modifica]
| A Wikimedia Commons hi ha contingut multimèdia relatiu a: Telòmer |
- CancerTelSys e:Med Systems Medicine Program. 2018 Feb. (en anglès)
- Telomere Biology and Cancer Risk NIH IRP (Intramural Research Program at the National Institutes of Health). 2017 Gen. (en anglès)
- Telomeres and cell senescence Khan Academy, 2015 Mar. (en anglès)
- Replicación de ADN y telómeros Barjau Vallet, J. 2015 Abr. (en castellà)
- Telomeres and Telomerase Arxivat 2020-02-24 a Wayback Machine. Infoaging Guide, Afar.org; 2016 Set. (en anglès)
- La solución de los telómeros (extracto) Blackburn, E; Epel, E. 2017 Jul, Ed. Aguilar. (en castellà)
- Explaining Telomere Biology Disorders YourekaScience, 2019 Jul. (en anglès)
