Nucleòtid: diferència entre les revisions
m Bot elimina espais sobrants |
Secció nova: funcions dels nucleòtids |
||
| Línia 50: | Línia 50: | ||
Els [[àcids nucleics]] són [[macromolècules]], considerades [[polímers]], fets de nucleòtids, que són els [[monòmers]] d'aquestes estructures. En el DNA, les bases de la purina són l'[[adenina]] i la [[guanina]], mentre que les pirimidines són la [[timina]] i la [[citosina]]. El RNA fa servir l'[[uracil]] en comptes de la timina. L'adenina sempre forma parella amb la timina mitjançant dos [[Enllaç d'hidrogen|ponts d'hidrogen]], mentre que la guanina forma parella amb la citosina mitjançant tres ponts d'hidrogen, cadascun degut a les seves estructures úniques. |
Els [[àcids nucleics]] són [[macromolècules]], considerades [[polímers]], fets de nucleòtids, que són els [[monòmers]] d'aquestes estructures. En el DNA, les bases de la purina són l'[[adenina]] i la [[guanina]], mentre que les pirimidines són la [[timina]] i la [[citosina]]. El RNA fa servir l'[[uracil]] en comptes de la timina. L'adenina sempre forma parella amb la timina mitjançant dos [[Enllaç d'hidrogen|ponts d'hidrogen]], mentre que la guanina forma parella amb la citosina mitjançant tres ponts d'hidrogen, cadascun degut a les seves estructures úniques. |
||
== Funcions biològiques == |
|||
La funció principal dels nucleòtids a les cèl·lules és '''formar part dels àcids nucleics'''. L’ADN està format per desoxiribonucleòtids i l’ARN per ribonucleòtids. Mentre que la funció pràcticament exclusiva dels desoxiribonucleòtids és formar part de l’ADN, els ribonucleòtids juguen molts altres papers a banda de formar part de l’ARN. |
|||
'''Magatzem i transferència d’energia.''' Els ribonucleòtids trifosfat, especialment l’ATP i en menor mesura el GTP, són molt utilitzats en processos cel·lulars que requereixen energia. De fet s’ha denominat l’ATP “la moneda universal d’energia”<ref>{{Ref-publicació|article=Enzyme-catalyzed phosphoryl transfer reactions|url=https://pubmed.ncbi.nlm.nih.gov/6250450/|publicació=Annual Review of Biochemistry|data=1980|issn=0066-4154|pmid=6250450|pàgines=877–919|volum=49|doi=10.1146/annurev.bi.49.070180.004305|nom=J. R.|cognom=Knowles}}</ref>. El trencament de l’enllaç anhidre entre el 3er i el 2on grup fosfat dels ribonucleòtids trifosfat allibera una quantitat d’energia que és fàcilment aprofitada per enzims de síntesi de macromolècules, per transport de molècules contra gradient, en la contracció muscular, etc... |
|||
Els ribonucleòtids trifosfat '''poden actuar com a coenzims''' transferint grups en reaccions catalitzades per enzims. El més habitual és la transferència d’un grup fosfat en reaccions de [[fosforilació]], si bé poden transferir [[Difosfat|grups difosfat o pirofosfat]] (ref) o nucleòtids monofosfat com l’adenilat o AMP<ref>{{Ref-publicació|article=Adenylylation: renaissance of a forgotten post-translational modification|url=https://pubmed.ncbi.nlm.nih.gov/21256032/|publicació=Trends in Biochemical Sciences|data=2011-04|issn=0968-0004|pmid=21256032|pàgines=221–228|volum=36|exemplar=4|doi=10.1016/j.tibs.2010.12.004|nom=Aymelt|cognom=Itzen|nom2=Wulf|cognom2=Blankenfeldt|nom3=Roger S.|cognom3=Goody}}</ref>. |
|||
Un altre possible destí dels ribonucleòtids dins de la cèl·lula és '''formar part de coenzims'''. Alguns dels coenzims més habituals com el [[coenzim A]], el [[Dinucleòtid de flavina i adenina|FAD]], el [[Nicotinamida adenina dinucleòtid|NAD]] o el SAM tenen un component d’origen ribonucleotídic a la seva estructura. |
|||
Alguns ribonucleòtids juguen papers molt importants en '''transducció de senyals'''. Així trobem alguns nucleòtids que poden ser transformats en formes cíclades donant lloc a importants segons missatgers com l’[[Monofosfat d'adenosina cíclic|AMPc]] o el [[Fosfat de guanosina cíclic|GMPc]]. Algunes proteïnes molt importants en transducció de senyals com les [[Proteïna G|proteïnes G heterotrimèriques]] (acoblades a [[Receptor acoblat a proteïnes G|receptors 7TM]]) o les [[Proteïna G|proteïnes G monomèriques]] (Ras, Rho) es regulen en funció de si estan unides al ribonucleòtid GDP (estat inactiu) o GTP (estat actiu). |
|||
Mentre que la majoria de funcions biològiques dels ribonucleòtids es duen a terme a l’interior cel·lular, alguns nucleòtids són alliberats de forma regulada o accidental i participen en '''comunicació intercel·lular''' estimulant receptors en altres cèl·lules<ref>{{Ref-publicació|article=Extracellular ATP and other nucleotides-ubiquitous triggers of intercellular messenger release|url=https://pubmed.ncbi.nlm.nih.gov/26545760/|publicació=Purinergic Signalling|data=2016-03|issn=1573-9546|pmc=4749530|pmid=26545760|pàgines=25–57|volum=12|exemplar=1|doi=10.1007/s11302-015-9483-2|nom=Herbert|cognom=Zimmermann}}</ref>. Els receptors estimulats per aquests nucleòtids s’anomenen receptors purinèrgics<ref>{{Ref-publicació|article=Purine and purinergic receptors|url=https://pubmed.ncbi.nlm.nih.gov/32166165/|publicació=Brain and Neuroscience Advances|data=2018-01|issn=2398-2128|pmc=7058212|pmid=32166165|pàgines=2398212818817494|volum=2|doi=10.1177/2398212818817494|nom=Geoffrey|cognom=Burnstock}}</ref>, tot i que en alguns casos poden ser estimulats per nucleòtids de pirimidina . Els principals nucleòtids amb funció de paper de comunicació intercel·lular són l’ATP, l’ADP, l’UTP i nucleòsids con l’adenosina. Els nucleòtids i nucleòsids que estimulen receptors purinèrgics juguen papers importants en la resposta immune<ref>{{Ref-publicació|article=Characteristics and the role of purinergic receptors in pathophysiology with focus on immune response|url=https://pubmed.ncbi.nlm.nih.gov/32037918/|publicació=International Reviews of Immunology|data=2020|issn=1563-5244|pmid=32037918|pàgines=97–117|volum=39|exemplar=3|doi=10.1080/08830185.2020.1723582|nom=Marharyta|cognom=Zyma|nom2=Rafał|cognom2=Pawliczak}}</ref>, en agregació plaquetària<ref>{{Ref-publicació|article=Platelet Purinergic Receptors in Thrombosis and Inflammation|url=https://pubmed.ncbi.nlm.nih.gov/32464678/|publicació=Hamostaseologie|data=2020-05|issn=2567-5761|pmid=32464678|pàgines=145–152|volum=40|exemplar=2|doi=10.1055/a-1113-0711|nom=Christian|cognom=Gachet|nom2=Beatrice|cognom2=Hechler}}</ref>, en neurotransmissió<ref>{{Ref-publicació|article=Neuronal and glial purinergic receptors functions in neuron development and brain disease|url=https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3808753/|publicació=Frontiers in Cellular Neuroscience|data=2013-10-28|issn=1662-5102|pmc=3808753|pmid=24191147|volum=7|doi=10.3389/fncel.2013.00197|nom=Ana|cognom=del Puerto|nom2=Francisco|cognom2=Wandosell|nom3=Juan José|cognom3=Garrido}}</ref><ref>{{Ref-publicació|article=Role of purinergic receptors in CNS function and neuroprotection|url=https://pubmed.ncbi.nlm.nih.gov/21586368/|publicació=Advances in Pharmacology (San Diego, Calif.)|data=2011|issn=1557-8925|pmid=21586368|pàgines=495–528|volum=61|doi=10.1016/B978-0-12-385526-8.00015-1|nom=Hidetoshi|cognom=Tozaki-Saitoh|nom2=Makoto|cognom2=Tsuda|nom3=Kazuhide|cognom3=Inoue}}</ref>, vasoconstricció<ref>{{Ref-publicació|article=Purinergic Signaling in the Cardiovascular System|url=https://pubmed.ncbi.nlm.nih.gov/28057794/|publicació=Circulation Research|data=2017-01-06|issn=1524-4571|pmid=28057794|pàgines=207–228|volum=120|exemplar=1|doi=10.1161/CIRCRESAHA.116.309726|nom=Geoffrey|cognom=Burnstock}}</ref> així com en processos patològics com el càncer<ref>{{Ref-publicació|article=Extracellular purines, purinergic receptors and tumor growth|url=https://pubmed.ncbi.nlm.nih.gov/27321181/|publicació=Oncogene|data=2017-01-19|issn=1476-5594|pmc=5269532|pmid=27321181|pàgines=293–303|volum=36|exemplar=3|doi=10.1038/onc.2016.206|nom=F.|cognom=Di Virgilio|nom2=E.|cognom2=Adinolfi}}</ref> o la resposta a infeccions virals<ref>{{Ref-publicació|article=Multifaceted roles of purinergic receptors in viral infection|cognom=Paoletti|nom5=Juliana|cognom4=Law|nom4=Frédéric|cognom3=Voisin|nom3=Laurent|cognom2=Raza|nom2=Syed Qasim|nom=Audrey|url=https://pubmed.ncbi.nlm.nih.gov/22683717/|doi=10.1016/j.micinf.2012.05.010|exemplar=14|volum=14|pàgines=1278–1283|pmid=22683717|issn=1769-714X|data=2012-11|publicació=Microbes and Infection|cognom5=Pipoli da Fonseca}}</ref>. |
|||
== Síntesi == |
== Síntesi == |
||
Revisió del 13:10, 30 març 2021
 | |
| Substància química | classe estructural d'entitats químiques |
|---|---|
| Codi | Equivalència | Complement |
|---|---|---|
| A | A | T o U |
| C | C | G |
| G | G | C |
| T | T | A |
| U | U | A |
| M | A o C | K |
| R | A o G | Y |
| W | A o T | W |
| S | C o G | S |
| Y | C o T | R |
| K | G o T | M |
| V | A o C o G | B |
| H | A o C o T | D |
| D | A o G o T | H |
| B | C o G o T | V |
| X o N | A o C o G o T | X |
Els nucleòtids són les unitats estructurals bàsiques dels àcids nucleics, és a dir que els àcids nucleics estan formats per l'encadenament de nucleòtids. També es poden trobar lliures a totes les cèl·lules.
Estan compostos per molècules d'àcid fosfòric, un glúcid de cinc carbonis, és a dir, una pentosa, i bases nitrogenades. La pentosa pot ser una ribosa o el seu derivat, la 2-desoxiribosa. La ribosa apareix en els nucleòtids que constitueixen les molècules d'ARN,i la desoxiribosa forma part de les d'ADN.
A més, els nucleòtids participen en la senyalització cel·lular (guanosina monofosfat cíclica i adenosina monofosfat cíclica) i estan incorporats com a uns dels importants cofactors de les reaccions enzimàtiques (coenzim A, dinucleòtid de flavina i adenina, mononucleòtid de flavina, i nicotinamida adenina dinucleòtid fosfat). Els derivats dels nucleòtids com per exemple el nucleòsid trifosfat tenen un paper central en el metabolisme, on serveixen com a font d'energia química (adenosina trifosfat i guanosina trifosfat).[1]

Estructura dels nucleòtids

Un nucleòtid està compost per una base nitrogenada, un sucre de cinc carbonis (ribosa o 2- desoxiribosa) i un grup fosfat.[2] La base nitrogenada i el sucre junts formen un nucleòsid. El grup fosfat forma enllaços amb el carboni 2, 3, o 5 del sucre, sent el carboni 5 el més comú. Els nucleòtids cíclics es formen quan el grup fosfat és enllaçat amb dos dels grups hidroxils dels sucres.[1] Els ribonucleòtids són nucleòtids on el sucre és la ribosa, i els desoxiribonucleòtids contenen el sucre desoxiribosa. Els nucleòtids poden tenir tant la base purina com la base pirimidina.
Els àcids nucleics són macromolècules, considerades polímers, fets de nucleòtids, que són els monòmers d'aquestes estructures. En el DNA, les bases de la purina són l'adenina i la guanina, mentre que les pirimidines són la timina i la citosina. El RNA fa servir l'uracil en comptes de la timina. L'adenina sempre forma parella amb la timina mitjançant dos ponts d'hidrogen, mentre que la guanina forma parella amb la citosina mitjançant tres ponts d'hidrogen, cadascun degut a les seves estructures úniques.
Funcions biològiques
La funció principal dels nucleòtids a les cèl·lules és formar part dels àcids nucleics. L’ADN està format per desoxiribonucleòtids i l’ARN per ribonucleòtids. Mentre que la funció pràcticament exclusiva dels desoxiribonucleòtids és formar part de l’ADN, els ribonucleòtids juguen molts altres papers a banda de formar part de l’ARN.
Magatzem i transferència d’energia. Els ribonucleòtids trifosfat, especialment l’ATP i en menor mesura el GTP, són molt utilitzats en processos cel·lulars que requereixen energia. De fet s’ha denominat l’ATP “la moneda universal d’energia”[3]. El trencament de l’enllaç anhidre entre el 3er i el 2on grup fosfat dels ribonucleòtids trifosfat allibera una quantitat d’energia que és fàcilment aprofitada per enzims de síntesi de macromolècules, per transport de molècules contra gradient, en la contracció muscular, etc...
Els ribonucleòtids trifosfat poden actuar com a coenzims transferint grups en reaccions catalitzades per enzims. El més habitual és la transferència d’un grup fosfat en reaccions de fosforilació, si bé poden transferir grups difosfat o pirofosfat (ref) o nucleòtids monofosfat com l’adenilat o AMP[4].
Un altre possible destí dels ribonucleòtids dins de la cèl·lula és formar part de coenzims. Alguns dels coenzims més habituals com el coenzim A, el FAD, el NAD o el SAM tenen un component d’origen ribonucleotídic a la seva estructura.
Alguns ribonucleòtids juguen papers molt importants en transducció de senyals. Així trobem alguns nucleòtids que poden ser transformats en formes cíclades donant lloc a importants segons missatgers com l’AMPc o el GMPc. Algunes proteïnes molt importants en transducció de senyals com les proteïnes G heterotrimèriques (acoblades a receptors 7TM) o les proteïnes G monomèriques (Ras, Rho) es regulen en funció de si estan unides al ribonucleòtid GDP (estat inactiu) o GTP (estat actiu).
Mentre que la majoria de funcions biològiques dels ribonucleòtids es duen a terme a l’interior cel·lular, alguns nucleòtids són alliberats de forma regulada o accidental i participen en comunicació intercel·lular estimulant receptors en altres cèl·lules[5]. Els receptors estimulats per aquests nucleòtids s’anomenen receptors purinèrgics[6], tot i que en alguns casos poden ser estimulats per nucleòtids de pirimidina . Els principals nucleòtids amb funció de paper de comunicació intercel·lular són l’ATP, l’ADP, l’UTP i nucleòsids con l’adenosina. Els nucleòtids i nucleòsids que estimulen receptors purinèrgics juguen papers importants en la resposta immune[7], en agregació plaquetària[8], en neurotransmissió[9][10], vasoconstricció[11] així com en processos patològics com el càncer[12] o la resposta a infeccions virals[13].
Síntesi
Els nucleòtids poden ser sintetitzats per diverses maneres: in vitro i in vivo. In vivo, els nucleòtids poder ser sintetitzats de novo o reciclats mitjançant vies de recuperació.[14] Els components utilitzats en la síntesi dels novo nucleòtids són derivats dels precursors biosintétics del metabolisme de carbohidrats i d'aminoàcids, així com de l'amoníac i del diòxid de carboni. El fetge és el principal òrgan que realitza la novo síntesi dels quatre nucleòtids. La síntesi de novo de purines i la de pirimidines segueix dos vies diferents, les pirimidines són sintetitzades primer per aspartat i carbamoïl-fosfat en el citoplasma de la cèl·lula, i no dins d'un orgànul específic. Els nucleòtids passen a desglossar-se de tal manera que les parts útils poden ser reutilitzades en les reaccions de síntesi per crear nous nucleòtids. In vitro, els grups de protecció poden ser utilitzats durant la producció de nucleòtids en el laboratori. Un nucleòsid purificat està protegit per crear fosforamidita, que poden ser utilitzats per obtenir anàlegs que no han estat trobats a la natura i/o sintetitzar un oligonucleòtid.
Síntesi de ribonucleòtids tipus pirimidina

La síntesi de pirimidines CTP i UTP té lloc al citoplasma i comença amb la formació de carbamoïl-fosfat a partir de glutamina i CO₂. A continuació, l'aspartat experimenta una reacció de condensació amb el carbamoïl-fosfat per donar lloc a la formació d'àcid oròtic. Posteriorment es dóna una reacció de ciclació en la qual un enzim anomenat aspartat carbamoïltransferasa forma N-carbamoïl-aspartat el qual és convertit immediatament en àcid dihidrooròtic per l'acció de l'enzim dihidroorotasa. Finalment aquest àcid esdevé orotat gràcies a la dihidroorotat oxidasa. Així, la reacció neta és la següent:
(S)-Dihidroorotat + O2 = Orotat + H2O2.
L'orotat està unit per un enllaç covalent amb una unitat ribosil fosforilada. Aquest enllaç covalent entre la ribosa i la pirimidina és entre el Carboni 1 de la molècula de ribosa (la qual conté un pirofosfat) i el Nitrogen 1 de l'anell de pirimidina. L'orotat fosforibosiltransferasa (“PPRP transferasa”) catalitza la reacció global produint orotidina monofosfat: La reacció aquesta vegada és la següent:
Orotat + 5-fosfo-α-D-ribosa 1-difosfat (PRPP") = Orotidina 5'-fosfat + Pirofosfat
L'orotidina-5-fosfat és descarboxilat pel corresponent enzim (orotidina-5-fosfat descarboxilasa) per formar uridina monofosfat (UMP). La PRPP transferasa catalitza tant la reacció de ribosilació com la de descarboxilació, formant UMP a partir de l'àcid oròtic amb la presència de PRPP. És a partir d'aquest UMP d'on derivaran altres nucleòtids del grup pirimidina. L'UMP (monofosfat d'uridina) és fosforilat per dues quinases per mitjà de dues reaccions en cadena. Primer es duu a terme la primera fosforilació, aconseguint uridina difosfat i finalment s'arriba al producte uridina trifosfat (UTP) amb la segona fosforilació. Ambdós passos aconsegueixen l'energia a partir de la hidròlisi d'ATP:
2) UDP + ATP = UTP + ADP
La citidina trifosfat (CTP) es forma a continuació per una aminació del UTP gràcies a l'acció catalítica de la UTP sintetasa. L'NH3 prové de la Glutamina. Així tornem a tenir una reacció com la següent, amb la hidròlisi de l'ATP com a font d'energia: UTP + Glutamina + ATP + H2O = CTP + ADP + Pi La citidina monofosfat (CMP) deriva de la citidina trifosfat (CTP) quan es desfosforila dues vegades.[15] [16]
Síntesi de ribonucleòtids tipus purina
Els àtoms que són utilitzats per construir el nucleòtid de purina provenen de moltes fonts diferents.

 |
Orígens biosintetics dels àtoms amb anell de purina N1 sorgeix del grup amino de l'Asp C2 i C8 provenen del format. N3 i N9 estan sota la contribució del grup amida de Gln. C4, C5 i N7 deriven de la Gly mentre que el C6 té l'origen en HCO3- (CO2). |
El procés de novo síntesi dels nucleòtids de purina és on aquests precursors s'incorporen al procés de l'anell de purina mitjançant 10 passos fins al punt de ramificació intermedi IMP, el nucleòtid de base hipoxantina. L'AMP i el GMP són posteriorment sintetitzats a partir d'aquest intermediari per vies separades en dues etapes. Així, restes de purina són inicialment formades com a part dels ribonucleòtids, en lloc de com a bases lliures. Sis enzims participen en la síntesi de IMP. Tres d'ells són multifuncionals: GART (reaccions 2,3 i 5) PAICS (reaccions 6 i 7) ATIC (reaccions 9 i 10)
El procés comença amb la formació de PRPP. PRPS1 és l'enzim encarregat d'activar el R5P, que es forma principalment per la pentosa fosfat, a PRPP al reaccionar amb l'ATP. La reacció en què un grup pirofosfat és transferit directament de l'ATP fins al C1 del R5P on el producte té la configuració alfa sobre C1, considerat inusual. Aquesta reacció està també compartida per la síntesi de Trp, His i els nucleòtids de pirimidina i està altament regulada, ja que té lloc en un creuament metabòlic important i requereix molta energia.
En la primera reacció única per la biosíntesi del nucleòtid de purina, PPAT catalitza el desplaçament del grup pirofosfat PRPP (PPi) per un nitrogen de l'amida donat per qualsevol glutamina (N), glicina (N + C), aspartat (N), àcid fòlic (C1), o pel CO2. Aquest procés està realitzat durant la síntesi de purina. La reacció es produeix amb la inversió de la configuració de la ribosaC1, formant β-5-fosforibosilamina (5-PRA) i establint la forma anomèrica del futur nucleòtid. Més endavant una glicina s'incorpora, impulsada durant la hidròlisi d'ATP, i el grup carboxil forma un enllaç amida amb NH2 introduït prèviament. Una unitat d'un carboni de l'àcid fòlic coenzim N10-formil-THF s'afegeix al grup amino de la glicina substituïda seguit pel trencament de l'anell de imidazol. Seguidament, un segon grup NH2 es transfereix des de la glutamina fins al primer carboni de la unitat de glicina. Una carboxilació del segon carboni de la unitat de glicina es fa al mateix moment. Aquest nou carboni és modificat per l'addició d'una tercera unitat d'NH2, aquesta vegada transferit des d'un residu d'aspartat. Finalment, una segona unitat de carboni-formil-THF s'afegeix al grup de nitrogen i l'anell es tanca covalentment per formar el precursor comú purina inosina monofosfat (IMP).
El monofosfat d'inosina es converteix en adenosina monofosfat en dos passos. En primer lloc, la hidròlisi de GTP permet l'addició d'aspartat al IMP gràcies a la sintetasa adenilosuccinato, substituint l'oxigen carbonil per nitrogen i formant l'intermediari adenilosuccinato. El fumarat s'escindeix després per formar monofosfat d'adenosina. Aquesta etapa és catalitzada gràcies a l'adenilosuccinato liasa. La inosina monofosfat es converteix en guanosina monofosfat gràcies a l'oxidació de l'IMP que forma xantilat, seguida per la inserció d'un grup amina en el C2. El NAD+ és l'acceptor d'electrons en la reacció d'oxidació. La transferència del grup amida des de la glutamina és impulsat per la hidròlisi d'ATP.
Degradació de purines i pirimidines
En els éssers humans, els anells de pirimidina (C, T, U) poden ser degradats completament en CO2 i NH3 (excreció d'urea). Cal dir que els anells de purina (G, A) no poden. En comptes d'això, es degraden en l'àcid metabòlic úric inert que després s'excreta del cos. L'àcid úric es forma quan el GMP es divideix en la base guanina i en la ribosa. La guanina es desamina a xantina que al seu torn s'oxida a àcid úric, sent aquesta última reacció irreversible. De la mateixa manera, l'àcid úric es pot formar quan AMP és desaminat en IMP del qual s'extreu la unitat de ribosa per formar hipoxantina. La hipoxantina s'oxida formant xantina i finalment creant àcid úric. En lloc de la secreció d'àcid úric, la guanina i el IMP poden ser utilitzats pel procés de reciclatge i per la síntesi d'àcids nucleics en presència de PRPP i aspartat (NH3 donants).
Unitat de longitud
El nucleòtid és una unitat de longitud comuna per una sola cadena de RNA, similar a les bases nitrogenades com a unitat de longitud de la doble cadena de DNA.
Codis d'abreujament per bases degenerades
El IUPAC té designats símbols per als nucleòtids.[17] A part de les cinc bases nitrogenades (A, G, C, T/U), normalment les bases degenerades s'utilitzen per designar PCR primers. Posteriorment trobem la llista d'aquests codis dels nucleòtids.
| Codi de nucleòtids IUPAC | Bases |
|---|---|
| A | Adenina |
| C | Citosina |
| G | Guanina |
| T (o U) | Timina (o Uracil) |
| R | A o G |
| Y | C o T (U) |
| S | G o C |
| W | A o T (U) |
| K | G o T (U) |
| M | A o C |
| B | C o G o T (U) |
| D | A o G o T (U) |
| H | A o C o T (U) |
| V | A o C or G |
| N | qualsevol base |
| . o - | buit |
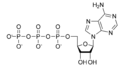
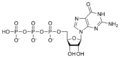
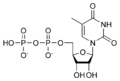
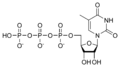
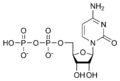
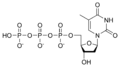
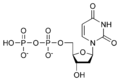
Estructures químiques
Nucleòtids
Desoxinucleòtids
Vegeu també
Referències
- ↑ 1,0 1,1 Alberts B, Johnson A, Lewis J, Raff M, Roberts K & Wlater P (2002). Molecular Biology of the Cell (4th ed.). Garland Science. ISBN 0-8153-3218-1. pp. 120-121.
- ↑ Coghill, Anne M.; Garson, Lorrin R.. The ACS style guide: effective communication of scientific information. 3a edició. Washington, D.C.: American Chemical Society, 2006, p. 244. ISBN 9780841239999.
- ↑ Knowles, J. R. «Enzyme-catalyzed phosphoryl transfer reactions». Annual Review of Biochemistry, 49, 1980, pàg. 877–919. DOI: 10.1146/annurev.bi.49.070180.004305. ISSN: 0066-4154. PMID: 6250450.
- ↑ Itzen, Aymelt; Blankenfeldt, Wulf; Goody, Roger S. «Adenylylation: renaissance of a forgotten post-translational modification». Trends in Biochemical Sciences, 36, 4, 2011-04, pàg. 221–228. DOI: 10.1016/j.tibs.2010.12.004. ISSN: 0968-0004. PMID: 21256032.
- ↑ Zimmermann, Herbert «Extracellular ATP and other nucleotides-ubiquitous triggers of intercellular messenger release». Purinergic Signalling, 12, 1, 2016-03, pàg. 25–57. DOI: 10.1007/s11302-015-9483-2. ISSN: 1573-9546. PMC: 4749530. PMID: 26545760.
- ↑ Burnstock, Geoffrey «Purine and purinergic receptors». Brain and Neuroscience Advances, 2, 2018-01, pàg. 2398212818817494. DOI: 10.1177/2398212818817494. ISSN: 2398-2128. PMC: 7058212. PMID: 32166165.
- ↑ Zyma, Marharyta; Pawliczak, Rafał «Characteristics and the role of purinergic receptors in pathophysiology with focus on immune response». International Reviews of Immunology, 39, 3, 2020, pàg. 97–117. DOI: 10.1080/08830185.2020.1723582. ISSN: 1563-5244. PMID: 32037918.
- ↑ Gachet, Christian; Hechler, Beatrice «Platelet Purinergic Receptors in Thrombosis and Inflammation». Hamostaseologie, 40, 2, 2020-05, pàg. 145–152. DOI: 10.1055/a-1113-0711. ISSN: 2567-5761. PMID: 32464678.
- ↑ del Puerto, Ana; Wandosell, Francisco; Garrido, Juan José «Neuronal and glial purinergic receptors functions in neuron development and brain disease». Frontiers in Cellular Neuroscience, 7, 28-10-2013. DOI: 10.3389/fncel.2013.00197. ISSN: 1662-5102. PMC: 3808753. PMID: 24191147.
- ↑ Tozaki-Saitoh, Hidetoshi; Tsuda, Makoto; Inoue, Kazuhide «Role of purinergic receptors in CNS function and neuroprotection». Advances in Pharmacology (San Diego, Calif.), 61, 2011, pàg. 495–528. DOI: 10.1016/B978-0-12-385526-8.00015-1. ISSN: 1557-8925. PMID: 21586368.
- ↑ Burnstock, Geoffrey «Purinergic Signaling in the Cardiovascular System». Circulation Research, 120, 1, 06-01-2017, pàg. 207–228. DOI: 10.1161/CIRCRESAHA.116.309726. ISSN: 1524-4571. PMID: 28057794.
- ↑ Di Virgilio, F.; Adinolfi, E. «Extracellular purines, purinergic receptors and tumor growth». Oncogene, 36, 3, 19-01-2017, pàg. 293–303. DOI: 10.1038/onc.2016.206. ISSN: 1476-5594. PMC: 5269532. PMID: 27321181.
- ↑ Paoletti, Audrey; Raza, Syed Qasim; Voisin, Laurent; Law, Frédéric; Pipoli da Fonseca, Juliana «Multifaceted roles of purinergic receptors in viral infection». Microbes and Infection, 14, 14, 2012-11, pàg. 1278–1283. DOI: 10.1016/j.micinf.2012.05.010. ISSN: 1769-714X. PMID: 22683717.
- ↑ Zaharevitz, DW; Anerson, LW; Manlinowski, NM; Hyman, R; Strong, JM; Cysyk, RL. «Contribution of de-novo and salvage synthesis to the uracil nucleotide pool in mouse tissues and tumors in vivo». .
- ↑ Jones, ME «Pyrimidine nucleotide biosynthesis in animals: Genes, enzymes, and regulation of UMP biosynthesis». Ann. Rev. Biochem, 49, 1, 1980, pàg. 253–79. DOI: 10.1146/annurev.bi.49.070180.001345. PMID: 6105839.
- ↑ McMurry, JE; Begley, TP. The organic chemistry of biological pathways. Roberts & Company, 2005. ISBN 9780974707716.
- ↑ IUPAC nucleotide code
Enllaços externs
| A Wikimedia Commons hi ha contingut multimèdia relatiu a: Nucleòtid |
- Abbreviations and Symbols for Nucleic Acids, Polynucleotides and their Constituents (IUPAC)
- Provisional Recommendations 2004 (IUPAC)
- Chemistry explanation of nucleotide structure
| Principals famíles bioquímiques | ||
| Àcids nucleics | Alcaloides | Aminoàcids | Carbohidrats | Carotenoides | Cofactors enzimàtics | Esteroides | Flavonoides | Glicòsids | Lípids | Pèptids | Policètids | Tetrapirrols | Terpens | ||
| Anàlegs d'àcids nucleics: | Tipus d'àcids nucleics | Anàlegs d'àcids nucleics : |
| Bases nitrogenades: | Adenina | Timina | Uracil | Guanina | Citosina | Purina | Pirimidina | |
|---|---|---|
| Nucleòsids: | Adenosina | Uridina | Guanosina | Citidina | Desoxiadenosina | Timidina | Desoxiguanosina | Desoxicitidina | |
| Nucleòtids: | AMP | UMP | GMP | CMP | ADP | UDP | GDP | CDP | ATP | UTP | GTP | CTP | AMPc | GMPc | ADPRc | |
| Desoxinucleòtids: | dAMP | TMP | dGMP | dCMP | dADP | TDP | dGDP | dCDP | dATP | TTP | dGTP | dCTP | |
| Àcids ribonucleics: | ARNm | ARNt | ARNr | ARNn | ARNnc | ARNmi | |
| Àcids desoxiribonucleics: | ADMmt | ADNc | |
| Anàlegs d'àcids nucleics: | AGN | APN | ATN | Morfolí | ARNin | |
| Seqüències: | Plasmidi | Còsmid | CAB | CAH | Cromosoma | Oligonucleòtid | |