Bioquímica
|
|
Aquest article o secció no cita les fonts o necessita més referències per a la seva verificabilitat. |

La bioquímica és la ciència que estudia les reaccions químiques i interaccions produïdes en organismes vius, incloent-hi l'estudi i l'estructura de proteïnes, glúcids, lípids, àcids nucleics i altres molècules presents en cèl·lules. L'etimologia de la paraula bioquímica prové del grec βίος, bios, 'vida' i de química. Aquesta del baix llatí chimia, de l'àrab kīmiyã´, 'pedra filosofal', i aquest, probablement del grec khimia 'mescla de sucs'.
La supervivència dels éssers vius depèn de la seva capacitat per portar a terme un seguit de reaccions químiques adreçades a l'intercanvi de matèria i energia amb el medi ambient i a la fabricació de les seves estructures vitals. La bioquímica estudia, per tant, totes aquelles reaccions que s'esdevenen tant a l'interior de la cèl·lula com al medi intern dels organismes pluricel·lulars. Aquestes bioreaccions no difereixen essencialment de les reaccions típiques de la química orgànica, bé que són caracteritzades específicament pel fet d'esdevenir-se totes a temperatures relativament baixes (en general, inferiors a 45 °C) gràcies a l'ajut dels biocatalitzadors, anomenats enzims, i pel fet de funcionar acoblades les unes a les altres en una complexíssima xarxa d'interrelacions, que constitueix el metabolisme. El metabolisme consta de reaccions degradadores (catabolisme), que aporten la matèria i l'energia necessàries per a l'organisme, i de reaccions biosintètiques (anabolisme), que utilitzen la matèria i l'energia per a la construcció de les macromolècules i d'altres estructures complexes de l'organisme. La bioquímica és una ciència nascuda de la convergència i l'encreuament de la química orgànica i la fisiologia, dues ciències molt desenvolupades al llarg del segle xix, que han experimentat un progrés molt important durant els darrers cinquanta anys.
Com que totes les formes de vida de l'actualitat descendeixen del mateix avantpassat comú, tenen una bioquímica generalment similar.[1][2] Es desconeix si les bioquímiques alternatives són possibles o pràctiques.
Història[modifica]



Antigament es considerava que els éssers vius no estaven subjectes a les lleis de la ciència igual que la matèria inerta. Era àmpliament acceptat que les molècules de la vida només podien ser produïdes per éssers vius (teoria de la força vital). Però el 1828, el químic alemany Friedrich Wöhler publicà el procés de síntesi de la urea (substància present en l'orina) a partir de cianat d'amoni, una substància inorgànica, provant que els compostos orgànics podien ser creats artificialment.[3][4]
Hom troba les arrels de la bioquímica moderna ja al segle xviii, en els clàssics estudis del químic suec Karl Wilhelm Scheele, que identificà l'àcid làctic en la llet, el cítric en la llimona, el màlic en les pomes i l'úric en l'orina, i en els del francès Antoine Laurent Lavoisier, que demostrà que els éssers vius empren oxigen de l'aire per a la combustió dels aliments, la qual produeix calor (energia).
Foren dos els principals eixos vertebradors dels estudis bioquímics del segle xix: La identificació de nous compostos naturals (foren descrits per primer cop les proteïnes, el glicogen, l'ADN i molts aminoàcids) i l'estudi funcional de la fermentació alcohòlica.
Els més grans avanços de la bioquímica durant el segle xix anaren lligats a l'estudi de la fermentació, que fixà les bases de l'enzimologia, de la bioenergètica i de l'estudi del metabolisme. Destaquen els treballs dels científics de les escoles francesa i alemanya, com ara Anselme Payen, que descobrí el 1833 el primer enzim, la diastasa (anomenada avui amilasa), Jean-François Persoz, Carl Justus von Liebig, Louis Pasteur o Eduard Buchner, que contribuí amb la primera demostració de complexos processos bioquímics fora de la cèl·lula el 1896: la fermentació alcohòlica en extractes de llevat.
La bioquímica assolí un impuls decisiu amb els treballs sobre l'hemoglobina d'Ernst Felix Immanuel von Hoppe-Seyler o la síntesi dels glúcids, els greixos i les proteïnes d'Emil Fischer. La nova ciència rebé definitivament el nom de bioquímica, proposat pel químic alemany Carl Neuberg, el 1903. Prèviament, aquesta àrea s'havia anomenat «química fisiològica».
La primera meitat del segle xx comportà un canvi qualitatiu en el desenvolupament de la bioquímica, ja que l'interès dels bioquímics es desplaçà cap a l'estudi de les funcions, dins l'organisme, dels composts identificats al segle precedent i el significat biològic dels processos en què intervenen. Així, l'estudi de la fermentació iniciat el segle xix conduí a l'elucidació, per part dels bioquímics alemanys Gustav Georg Embden, Otto Meyerhof i Jakob Parnass el 1933, de la primera ruta metabòlica identificada, la via glucolítica. Juntament amb la glicòlisi, es descrigueren els altres dos processos principals per a l'obtenció d'energia a la cèl·lula, el cicle dels àcids tricarboxílics, per part de Hans Adolf Krebs el 1937, i la cadena respiratòria, que permet la reducció de l'oxigen i la síntesi de l'ATP, estudi que va aplegar molts dels principals bioquímics de l'època com ara Otto Warburg o Albert Lehninger.
Durant la segona meitat del segle xx, la bioquímica experimentà un gran desenvolupament gràcies a noves i complexes tècniques analítiques com ara la cromatografia, la difracció de raigs X, la ressonància magnètica nuclear, el marcatge isotòpic, la microscòpia electrònica o l'espectroscòpia molecular. Aquestes tècniques permeteren la descoberta i l'anàlisi en detall de diverses molècules i vies metabòliques de la cèl·lula, com ara la glicòlisi i el cicle de Krebs.
També s'ha fet cada cop més palesa arreu del món la necessitat de dedicar més recursos humans i econòmics a la investigació en aquesta ciència. Això ha representat un nou canvi en l'objectiu de la bioquímica: durant aquest període, el principal interès ha estat l'estudi dels mecanismes moleculars que controlen els processos descrits els anys anteriors. Així, descobriments com ara el del monofosfat d'adenosina (AMP) cíclic per Earl Sutherland el 1957 o la fosforilació de les proteïnes per Edwin Krebs i Emil Fischer el 1959 han portat al naixement de disciplines noves com l'endocrinologia molecular, que ha permès l'estudi de la regulació i la integració del metabolisme. Malgrat els importants avenços científics assolits, encara es van descobrint nous composts bioquímics (com és el cas de l'important regulador metabòlic fructosa-2,6-difosfat), com també aspectes bàsics (com ara vies metabòliques secundàries) de l'entrellat de vies metabòliques que constitueixen el metabolisme. Avui en dia, les troballes de la bioquímica s'usen en diferents àrees, des de la genètica fins a la biologia molecular passant per l'agricultura i la medicina, entre altres camps.
Camps de recerca[modifica]

Actualment, la bioquímica té quatre línies principals d'estudi: la bioquímica estructural, la regulació del metabolisme, la bioquímica cel·lular i la bioquímica clínica.
La bioquímica estructural se centra en l'estructura de composts i agregats moleculars cada cop més complexos, per tal d'arribar a comprendre'n el mecanisme d'actuació i poder dissenyar fàrmacs específics per modificar-ne l'acció en casos de disfuncionalitat.
La regulació del metabolisme té com a objectiu l'estudi global i integrat del metabolisme, la seva regulació i la seva adaptació a diferents situacions fisiològiques, analitzant el control de l'activitat dels enzims (especialment pel que fa a la variació d'activitat amb relació al grau de fosforilació i l'expressió dels gens que codifiquen pels enzims) i el mecanisme d'acció de les hormones (endocrinologia molecular).
La bioquímica cel·lular estudia, a escala molecular, els diferents processos que permeten la supervivència de la cèl·lula, que abans s'havien limitat als mecanismes d'obtenció i aprofitament de matèria i energia i actualment s'estenen a tots els esdeveniments cel·lulars, com ara el cicle de divisió de la cèl·lula o la mort cel·lular.
La bioquímica clínica es planteja l'estudi de les bases moleculars que condueixen a situacions patològiques.
Monòmers i polímers[modifica]
Els monòmers i polímers són la base estructural sobre la qual es basen els quatre tipus de biomolècules principals de la bioquímica (glúcids, lípids, proteïnes i àcids nucleics). Els monòmers són les unitats bàsiques constituents dels polímers; són molècules relativament petites, i és de la unió de molts monòmers que es forma un polímer o macromolècula. Quan són sintetitzades, ambdues molècules experimenten un procés anomenat síntesi de deshidratació.
Glúcids[modifica]

Els monosacàrids són els monòmers dels glúcids. De la reacció de dos grups carboxil de dos monosacàrids, es forma un enllaç nou, alliberant-se així una molècula d'aigua. Aquesta molècula s'allibera perquè en formar-se l'enllaç O-glicosídic (l'enllaç que es forma entre els grups carboxil de dos monosacàrids) es perd un grup hidroxil (-OH) d'un dels dos grups carboxil i un àtom d'oxigen de l'altre (aquest procés s'anomena síntesi de deshidratació, car en alliberar-se una molècula d'aigua per sintetitzar la nova molècula, es «deshidrata»). El producte resultant d'aquesta unió s'anomena disacàrid. De la unió successiva de monosacàrids (amilosa) o disacàrids (àcid hialurònic) es formen unes macromolècules que reben el nom de polisacàrids. Tots els sucres són glúcids, però no tots els glúcids són sucres. Hi ha més glúcids a la Terra que qualsevol altre tipus de biomolècula coneguda; serveixen per emmagatzemar energia i informació genètica (la ribosa i el seu derivat, la desoxiribosa formen part dels nucleòtids de l'ARN i l'ADN, respectivament, i també tenen un paper important en la interacció i comunicació entre cèl·lules.
Monosacàrids[modifica]
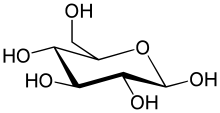
Com ja s'ha comentat, el tipus més simple de glúcids són els monosacàrids, formats essencialment per carboni, hidrogen i oxigen, majoritàriament en una ràtio d'1:2:1 (la fórmula general és CnH2nOn, on n com a mínim és 3). Exemples d'aquests monosacàrids són la glucosa (C₆H₁₂O₆), el glúcid més important; o la fructosa (C₆H₁₂O₆), el sucre que dona el gust dolç a les fruites. Aquesta fórmula general, però, només és vàlida en els monosacàrids, ja que després d'unir-se per sintetitzar disacàrids o polisacàrids, les proporcions d'hidrogen i oxigen canvien. Els monosacàrids es classifiquen en aldoses (amb un grup aldehid al final de la cadena, com per exemple la glucosa) i en cetoses (amb un grup ceto a la cadena, com per exemple la fructosa). Tant les aldoses com les cetoses es troben en un equilibri entre les formes de cadena oberta i (a partir d'una longitud de cadena de quatre carbonis) les formes cícliques. Les formes ciclitzades es generen per la formació d'un enllaç entre un dels grups hidroxils de la cadena del sucre amb el carboni del grup aldehid o ceto per formar un enllaç hemiacetàlic. Això forma anells saturats heterocíclics pentagonals o hexagonals (furanoses i piranoses, respectivament), que contenen un oxigen com a heteroàtom.
Disacàrids[modifica]

La molècula resultant de la unió de dos monosacàrids rep el nom de disacàrid. La reacció que ja s'ha explicat anteriorment també es pot dur a terme de forma inversa, utilitzant una molècula d'aigua per fragmentar un disacàrid i trencar l'enllaç O-glicosídic; és el procés d'hidròlisi. El disacàrid més conegut és la sacarosa, o sucre normal (també conegut com a "sucre de taula" o "sucre de canya" per diferenciar-lo de la resta de sucres). La sacarosa consisteix en una molècula de glucosa i una de fructosa unides. Un altre disacàrid important és la lactosa, que consisteix en una molècula de glucosa i una de galactosa. En la majoria d'humans, a mesura que s'envelleix, també sol disminuir la producció de lactasa, l'enzim que hidrolitza la lactosa en glucosa i galactosa. Això resulta en deficiència de lactasa, més coneguda com a intolerància a la lactosa.
Els polímers de sucres es caracteritzen per tenir extrems reductors o no reductors. L'extrem reductor d'un glúcid és un àtom de carboni que pot estar en equilibri amb la forma aldehid o ceto de cadena oberta. Si la unió dels monòmers es produeix en un d'aquests àtoms de carboni, el grup hidroxil lliure de la forma piranosa o furanosa s'intercanvia amb una cadena de costat OH d'un altre sucre, donant un acetal complet. Això evita que s'obri la cadena a la forma aldehid o ceto i fa que el residu modificat sigui no reductor. La lactosa té un extrem reductor al seu fragment de glucosa, mentre que el fragment de galactosa forma un acetal complet amb el grup C4-OH de la glucosa. La sacarosa manca d'extrem reductor, a causa de la formació d'un acetal complet entre el carboni aldehid de la glucosa (C1) i el carboni ceto de la fructosa (C2).
Oligosacàrids i polisacàrids[modifica]

Quan alguns (entre tres i sis) monosacàrids s'uneixen, el producte és un oligosacàrid (oligo significa "pocs"). Aquestes molècules tendeixen a ser utilitzades com a marcadors i senyals, entre altres funcions. Molts monosacàrids units formen un polisacàrid. Poden estar units en una sola cadena lineal, o es poden ramificar.
Hi ha dues classes principals de polisacàrids; els homopolisacàrids, formats per cadenes successives d'un mateix monòmer, com ara la cel·lulosa (fabricada per les plantes i component estructural important de la seva paret cel·lular); i els heteropolisacàrids, formats per diferents tipus de monòmers, com ara l'àcid hialurònic.
Ús dels glúcids com a font d'energia[modifica]
La glucosa és la font d'energia principal de la majoria de sistemes metabòlics. Per exemple, els polisacàrids són descompostos en monòmers (la glicogen fosforilasa recupera els residus de glucosa del glicogen). Els disacàrids com la lactosa o la sacarosa són fragmentats en els seus dos monosacàrids components.
Glicòlisi (anaeròbica)[modifica]
La glucosa és metabolitzada principalment per una ruta de deu passos molt important i antiga anomenada glicòlisi, el resultat net de la qual és trencar una molècula de glucosa en dues molècules de piruvat; també produeix dues molècules d'ATP, la moneda energètica de les cèl·lules, juntament amb dos equivalents reductors en convertir NAD+ en NADH. Aquest procés no requereix oxigen; si no hi ha oxigen disponible (o la cèl·lula no el pot utilitzar), el NAD és restaurat mitjançant la conversió del piruvat en lactat (per exemple, en els humans) o en etanol i diòxid de carboni (per exemple, en els llevats). Altres monosacàrids com la galactosa o la fructosa es poden convertir en intermedis de la ruta glucolítica.
Aeròbica[modifica]
En les cèl·lules aeròbiques amb prou oxigen, com la majoria de cèl·lules humanes, el piruvat és metabolitzat encara més. És convertit irreversiblement en acetil-CoA, alliberant un àtom de carboni com diòxid de carboni residual, i generant un altre equivalent reductor, NADH. Aleshores, les dues molècules d'acetil-CoA (d'una molècula de glucosa) entren al cicle de Krebs, produint dues molècules més d'ATP, sis molècules més de NADH i dues (ubi)quinones reduïdes (via FADH₂ com a cofactor unit a enzim), i alliberant els àtoms de carboni restants com a diòxid de carboni. Les molècules de NADH i de quinols així produïdes entren als complexos enzimàtics de la cadena respiratòria, un sistema de transport d'electrons que transfereix els electrons en última instància a l'oxigen i conserva l'energia alliberada en forma de gradient de protons en una membrana (en els eucariotes, la membrana mitocondrial interna). Per aquest procés, l'oxigen és reduït en aigua i es regeneren els acceptors d'electrons originals NAD+ i quinones. És per això que els humans inspiren oxigen i expiren diòxid de carboni. L'energia alliberada de la transferència dels electrons d'estats d'alta energia en NADH i quinol és conservada inicialment com a gradient de protons i convertida en ATP via ATP sintasa. Això genera 28 molècules addicionals d'ATP (24 dels 8 NADH + 4 dels 2 quinols), donant un total de 32 molècules d'ATP conservades per glucosa degradada (dues de la glicòlisi més dues del cicle de Krebs). Resulta evident que l'ús d'oxigen per oxidar completament la glucosa proporciona molta més energia als organismes que qualsevol ruta metabòlica oxigen-independent, i es creu que és el motiu pel qual la vida complexa només aparegué després que l'atmosfera de la Terra hagués acumulat grans quantitats d'oxigen.
Gluconeogènesi[modifica]
En els vertebrats, els músculs esquelètics que es contrauen vigorosament (com per exemple durant l'aixecament de pesos o els esprints) no reben prou oxigen per a respondre a les seves necessitats energètiques, de manera que passen al metabolisme anaeròbic, convertint glucosa en lactat. El fetge regenera la glucosa, mitjançant un procés anomenat gluconeogènesi. Aquest procés no és exactament l'invers de la glicòlisi, i de fet requereix tres vegades la quantitat d'energia obtinguda de la glicòlisi (s'utilitzen sis molècules d'ATP, en contrast amb les cinc que s'obtenen en la glicòlisi). De manera anàloga a les reaccions ja mencionades, la glucosa produïda pot sofrir glicòlisi en teixits que necessiten energia, ser emmagatzemada en forma de glicogen (o, en les plantes, midó), ser convertida en altres monosacàrids o unida en disacàrids o oligosacàrids. La combinació de les rutes de la glicòlisi durant l'exercici, el pas del lactat al flux sanguini a través del fetge, la posterior gluconeogènesi i l'alliberament de glucosa al flux sanguini rep el nom de cicle de Cori.
Lípids[modifica]
Els lípids són biomolècules insolubles en aigua i solubles en dissolvents orgànics, constituïdes essencialment per carboni, hidrogen i oxigen (en una proporció molt més baixa). Sovint també presenten nitrogen i fòsfor. Els lípids desenvolupen diverses funcions biològicament importants; actuen com a components estructurals de les membranes, com a coberta protectora sobre la superfície de molts organismes, com a components de la superfície cel·lular relacionats amb el reconeixement cel·lular, i com a formes de transport i "combustible" catabòlics. Malgrat que els lípids constitueixen una classe de biomolècules molt ben definida, constitueixen sovint molècules híbrides, com ara els glucolípids o les lipoproteïnes. Aquestes molècules requereixen la unió d'ambdues per exercir la seva funció biològica.
Classificació de lípids[modifica]
Existeixen diferents classificacions dels diferents tipus de lípids. La més usada, però, fa referència a l'estructura dels seus esquelets carbonats, i és la que serà tractada aquí. Així es distingeixen dos grans tipus de lípids, els lípids saponificables (o complexos) que contenen àcids grassos com a components, i els lípids no saponificables (o simples).
Lípids saponificables[modifica]
Àcids grassos[modifica]
Els àcids grassos són lípids constituïts per una cadena hidrocarbonada amb un grup carboxil en posició terminal. El nombre de carbonis és variable des de 4 fins a 30 carbonis. Habitualment, presenten un nombre parell de carbonis, sent els més freqüents els que tenen entre 16 i 18 carbonis. La majoria són lineals, però alguns poden ser ramificats o parcialment cíclics. Tot i que els àcids grassos es troben en quantitats molt grans com a components essencials dels lípids saponificables, en estat lliure només apareixen en traces. S'han aïllat aproximadament uns cent tipus diferents d'àcids grassos. Es distingeixen dos tipus d'àcids grassos; els àcids grassos saturats, en què tots els enllaços entre carbonis de la cadena són simples. L'altre tipus, els àcids grassos insaturats, presenten algun enllaç doble. Poden ser monoinsaturats si tenen un sol enllaç doble, o poliinsaturats si en presenten més d'un
Acilglicèrids[modifica]

Els acilglicèrids són un tipus de lípids constituïts per glicerina (un trialcohol de tres carbonis amb un grup hidroxil en cadascun) i àcids grassos. Segons el nombre d'àcids grassos (un, dos o tres) es distingeixen monoacilglicèrids, diacilglicèrids i triacilglicèrids. Aquests darrers són els més abundants i amb major importància biològica, representant aproximadament el 90% del catabolisme de lípids. Els triacilglicèrids en estat sòlid a temperatura ambient s'anomenen greixos, i els que són líquids, s'anomenen olis. La glicerina s'uneix a cada àcid gras mitjançant una reacció d'esterificació (reacció entre un alcohol i un àcid), reaccionant així els seus grups hidroxil amb l'OH del grup carboxil dels àcids grassos. Així doncs, per la formació d'un triacilglicèrid, es produeixen tres reaccions d'esterificació. L'enllaç nou que es forma s'anomena enllaç èster.
Fosfoglicèrids[modifica]
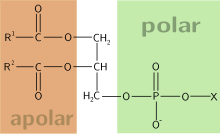
Els fosfoglicèrids estan constituïts per glicerina, dos àcids grassos, un grup fosfat, i, en el cas dels fosfoglicèrids complexos, un altre alcohol (habitualment un aminoalcohol). En la formació d'un fosfoglicèrid simple es duen a terme tres reaccions d'esterificació, en la unió dels carbonis 1 i 2 a àcids grassos i del 3 a un àcid fosfòric. En el cas dels fosfoglicèrids complexos, a més a més, un alcohol s'uneix al grup fosfat d'un fosfoglicèrid simple. Es designa amb vaguetat als fosfoglicèrids com a fosfolípids, però cal tenir en compte que no tots els lípids que presenten fòsfor són fosfoglicèrids, com es veurà en el següent apartat, les esfingomielines són fosfolípids perquè contenen fòsfor, però s'acostumen a classificar com a esfingolípids a causa de l'estructura del seu esquelet carbonat. Els fosfolípids (fosfoglicèrids i esfingomielines) són els principals lípids de membrana, i com a tal, també són el principal component de les membranes cel·lulars. Els lípids de membrana (i entre ells els fosfoglicèrids) són molècules amfipàtiques amb "cap" polar i una «cua» hidròfoba. Aquesta característica possibilita la formació de la bicapa lipídica, ja que els caps polars se situen a l'exterior i les cues hidròfobes a l'interior de la bicapa.
Esfingolípids[modifica]


Els esfingolípids estan formats per esfingosina, un àcid gras i un tercer component variable en els diferents tipus d'esfingolípids. N'hi ha dos tipus principals, segons quin és el tercer component. En les esfingomielines, el tercer component és un àcid fosfòric unit a colina o etanolamina; en els glicoesfingolípids és un glúcid (monosacàrid o oligosacàrid). Els glicoesfingolípids que tenen un monosacàrid s'anomenen cerebròsids, i els que tenen un oligosacàrid s'anomenen gangliòsids Les estructures dels esfingolípids i dels glicofosfolípids més corrents són molt similars. El prefix esfingo- fa referència a les enigmàtiques propietats dels esfingolípids, ja que, ara per ara, el paper dels esfingolípids és bastant desconegut. Tot i tenir estructures molt similars, la funció d'uns i altres resulta ser completament diferent. Se sap, però que els esfingolípids poden servir com a font de segons missatger en la transmissió de senyals cel·lulars.
Cèrids[modifica]

Els cèrids (o ceres) són el resultat de la unió d'un àcid gras amb un monoalcohol (alcohol amb un sol grup hidroxil) de cadena llarga mitjançant un enllaç èster. Els cèrids formen part de les cobertes protectores de pell, plomes, fulles i fruits i de l'exoesquelet dels insectes, entre d'altres. Són insolubles en aigua, durs en baixes temperatures i tous i mal·leables en temperatures relativament elevades (vora 40 - 50 °C).
Lípids no saponificables[modifica]
Esteroides[modifica]

Els esteroides són lípids derivats del ciclopentàperhidrofenantrè (un hidrocarbur saturat de disset carbonis amb estructura cíclica de quatre anells, tres dels quals hexagonals i un altre pentagonal). Els esteroides es diferencien entre ells per tres característiques:
- Els anells dels esteroides poden presentar dobles enllaços (la posició i el nombre de dobles enllaços és variable) o tenir tots els enllaços simples.
- Els anells dels esteroides tenen ramificacions (el nombre, la posició i la llargada és variable)
- Tenen grups funcionals que es troben als anells i/o a les ramificacions (el tipus, la posició i el nombre és variable).
Els punts de substitució més habituals són el carboni 11 (anell C), el carboni 3 (anell A) i el carboni 17 (anell D). Tots els esteroides s'originen a partir de l'escualè, un hidrocarbur lineal que se ciclitza amb molta facilitat. La majoria dels esteroides són hormones o bé sexuals o bé implicades en el metabolisme dels glúcids i de les proteïnes de molts teixits. Una excepció notable és el colesterol, que forma part de la membrana plasmàtica i resulta molt important pel manteniment de la seva fluïdesa.
Terpens[modifica]

Els terpens són lípids constituïts per molècules d'isoprè o derivats d'aquest. L'isoprè és un hidrocarbur poliinsaturat de cinc carbonis i amb doble enllaç entre els carbonis 1 i 2, i el carbonis 3 i 4. Aquests dobles enllaços acostumen a canviar en els seus derivats, i per tant l'única característica comuna és la seva estructura. Els isoprens i els seus derivats, per tant, són els monòmers dels terpens. Els isoprens s'uneixen entre ells mitjançant enllaços "cap amb cua" (C1 d'un amb C4 de l'altre) i "cua amb cua" (C4 d'un amb C4 de l'altre). Els terpens es classifiquen segons el nombre d'isoprens que presenten, així, un terpè de dues unitats d'isoprè s'anomena monoterpè, un de tres, sesquiterpè, un de quatre, diterpè...
La importància biològica dels terpens queda palesa en la gran varietat de terpens presents en els diferents processos biològica en els que participen. S'han identificat en els vegetals un nombre molt elevat de terpens, molts dels quals són components dels olis essencials d'aquestes plantes. El mentol i el geraniol (ambdós monoterpens), per exemple, són els components principals de l'oli de menta i del de gerani, respectivament. El fitol, un diterpè, és un alcohol lineal component de la clorofil·la. L'escualè és un triterpè precursor dels esteroides, com es comentarà més endavant. D'altra banda, també els carotenoides (pigments fotosintètics) i la ubiquinona (transportador d'hidrogen en la cadena respiratòria dels mitocondris) són membres d'aquesta família de compostos.
Biosíntesi dels lípids[modifica]
Catabolisme dels lípids[modifica]
El catabolisme dels lípids és, essencialment, el catabolisme dels triacilglicèrids, ja que és aquesta la forma més comuna en la que es troben els lípids en la naturalesa. Per aquesta raó, aquí només es farà referència al catabolisme dels àcids grassos i el de la glicerina (els dos components dels triacilglicèrids). Els triacilglicèrids són inicialment hidrolitzats per les lipases, donant com a productes àcids grassos i glicerina.
La glicerina és fosforilada per una cinasa i posteriorment deshidrogenada. La molècula resultant d'aquestes dues reaccions és la dihidroxiacetona fosfat, la qual, amb la intervenció d'una isomerasa, esdevé gliceraldehid 3-fosfat, anant llavors cap a la glicòlisi (que ja s'ha explicat abans).
Proteïnes[modifica]

Els aminoàcids[modifica]
Les proteïnes són molècules grans, els monòmers de les quals són aminoàcids. Hi ha vint aminoàcids considerats primaris. Els aminoàcids contenen tots un grup carboxil, un grup amino i l'anomenat grup "R", que és el que diferencia cada aminoàcid. Els aminoàcids s'uneixen entre ells amb un enllaç peptídic (enllaç que presenta unes característiques especials que el diferencien, com ara la rigidesa dels plans atòmics, característiques que es donen gràcies a un fenomen anomenat ressonància peptídica) que s'estableix entre el grup amino i el grup carboxil de dos aminoàcids. El producte resultant d'aquesta unió s'anomena pèptid. Els pèptids molt grans reben el nom de polipèptids o cadenes polipeptídiques. Una proteïna pot estar constituïda per una sola cadena polipeptídica (l'amilasa) o per més d'una (l'hemoglobina). En un medi neutre, els aminoàcids estan doblement ionitzats, ja que un protó pertanyent al grup carboxil és captat pel grup amino. La molècula, doncs, queda doblement ionitzada, però és globalment neutra (zwitterió).
Estructura de les proteïnes[modifica]

En les proteïnes es poden diferenciar fins a quatre nivells estructurals.
- Estructura primària és la seqüència d'aminoàcids de la cadena polipeptídica de la proteïna. És exclusiva de cada proteïna i és el nivell estructural més important de tots, ja que determina la resta de nivells.
- Estructura secundària descriu les diverses disposicions que adopten a l'espai els aminoàcids al llarg de les cadenes polipeptídiques de les proteïnes. Les tres disposicions més comunes d'estructura secundària són l'hèlix alfa, el full plegat beta i el gir beta.
- Estructura terciària és la disposició que adopten a l'espai cadascuna de les cadenes polipeptídiques que les formen. L'estructura terciària s'estabilitza mitjançant enllaços iònics, pont disulfur, interaccions hidrofòbiques, pont d'hidrogen i interaccions de Van der Waals.
- Estructura quaternària és la disposició que adopten a l'espai el conjunt de les cadenes polipeptídiques que les formen. Per aquesta raó, en les proteïnes amb una sola cadena polipeptídica no es diferencia estructura quaternària.
Classificació de les proteïnes[modifica]
Segons l'estructura[modifica]
Es diferencien dos tipus de proteïnes segons la seva estructura:
- Les proteïnes fibroses són proteïnes de forma filamentosa, insolubles en aigua. La seva funció és majoritàriament estructural. Poden ser rígides o més flexibles i laminars. En són exemples el col·lagen i la queratina.
- Les proteïnes globulars adopten formes més o menys esfèriques i compactes. La gran majoria són solubles en aigua. Les proteïnes globulars realitzen funcions molt diverses i són les més abundants. En són exemples la mioglobina i la concanavalina.
Segons la composició[modifica]
Segons la seva composició, les proteïnes es classifiquen en holoproteïnes, constituïdes únicament per aminoàcids, i heteroproteïnes, que contenen, a més d'aminoàcids, un altre component, anomenat grup prostètic, que és essencial per la seva funció.
Segons la funció[modifica]
Les funcions de les proteïnes són nombroses:
- Proteïnes estructurals: La seva funció és de protecció i manteniment. Habitualment es tracta de proteïnes fibroses.
- Proteïnes motores: S'encarreguen dels moviments de les cèl·lules de l'organisme. Per exemple, els moviments de les proteïnes actina i miosina són les responsables en última instància de la contracció dels músculs esquelètics.
- Proteïnes transportadores: S'uneixen fàcilment a certes molècules i s'encarreguen del seu transport en l'organisme. L'hemoglobina, que transporta l'oxigen, n'és un bon exemple.
- Proteïnes defensives: Formen part del sistema immunitari i són capaces d'unir-se als antígens dels agents infecciosos per tal de desactivar-los. Són els anticossos; un bon exemple de proteïnes que s'uneixen a un tipus específic de molècules. De fet, la prova ELISA, que utilitza anticossos, és actualment un dels tests més sensibles que utilitza la medicina actua per detectar diverses biomolècules.
- Proteïnes d'emmagatzematge: S'encarreguen de l'emmagatzematge de molècules o ions. L'albúmina de l'ou i la caseïna de la llet en són dos exemples.
- Proteïnes reguladores: Coordinen i controlen l'activitat metabòlica cel·lular. L'exemple més conegut és la insulina, que participa en la regulació de concentració de glucosa a la sang.
- Proteïnes enzimàtiques (enzims): Els enzims són probablement les proteïnes més importants. Aquestes molècules reconeixen molècules reactants específiques anomenades substrats; aleshores catalitzen la reacció entre aquestes molècules. Reduint-ne l'energia d'activació, l'enzim accelera la reacció de 10⁶ a 1012 vegades més; així, una reacció que normalment trigaria més de 3.000 anys en completar-se espontàniament pot trigar segons amb un enzim, en condicions de pH i temperatura tolerables per l'organisme (a diferència d'altres catalitzadors químics). A més a més, l'enzim es recupera intacte en finalitzar la reacció, de manera que pot tornar a intervenir en la mateixa reacció amb un nou conjunt de substrats. Utilitzant diversos modificadors es pot regular l'activitat de l'enzim, permetent controlar la bioquímica de la cèl·lula en general. L'anhidrasa carbònica que catalitza la síntesi de l'àcid carbònic, és un enzim.
Biosíntesi de les proteïnes[modifica]
Metabolisme de les proteïnes[modifica]
Àcids nucleics[modifica]

Els àcids nucleics són molt importants en la bioquímica, ja que emmagatzemen la informació genètica de l'organisme, a partir de la qual se sintetitzen les proteïnes necessàries per a aquest. Els àcids nucleics més comuns són l'àcid desoxiribonucleic (ADN) i l'àcid ribonucleic (ARN). Els monòmers reben el nom de nucleòtids. Els nucleòtids més comuns estan formats per una base nitrogenada (adenina, citosina, guanina, timina i uracil) unida a una molècula de ribosa (ARN) o desoxiribosa (ADN). L'adenina s'uneix amb la timina (en l'ADN) i l'uracil (en l'ARN), la timina només s'uneix amb l'adenina, i la citosina i la guanina només es poden unir l'una amb l'altra.
Aplicacions[modifica]
Gràcies al gran desenvolupament que han tingut les metodologies, especialment amb l'arribada de les tècniques de biologia molecular, la bioquímica s'ha constituït en la ciència biològica bàsica per excel·lència, ja que els coneixements derivats dels estudis bioquímics troben aplicació en totes les altres branques de la biologia, des de la fisiologia (bioquímica fisiològica i bioquímica de la nutrició) fins a la microbiologia (bioquímica de microorganismes), la genètica (biologia molecular), la citologia (biologia cel·lular), la taxonomia (bioquímica comparada) i, fins i tot, l'ecologia (bioquímica ecològica). A més, l'espectacular progrés de la bioquímica en anys recents ha permès la seva aplicació al cada vegada més extens camp de les ciències biomèdiques, com ara la farmacologia (bioquímica farmacològica i bioquímica toxicològica) o la medicina (bioquímica clínica), atès que la bioquímica proporciona les claus moleculars per a la comprensió de moltes malalties, incloses les tres de més gran incidència social, com són el càncer, la SIDA i les malalties cardiovasculars. Darrerament, ha anat guanyant importància la bioquímica industrial, que tracta de l'obtenció en grans quantitats de determinats composts (per exemple, d'insulina humana per cultiu de bacteris sotmesos a manipulació genètica), com també de l'aplicació a processos industrials dels resultats obtinguts en estudis bioquímics (com la utilització industrial d'enzims, com ara la cel·lulasa, enzim que degrada la cel·lulosa).
Vegeu també[modifica]
Referències[modifica]
- ↑ Smith E, Morowitz H «Universality in intermediary metabolism». Proc Natl Acad Sci USA, 101, 36, 2004, pàg. 13168–73. DOI: 10.1073/pnas.0404922101. PMID: 15340153.
- ↑ Romano A, Conway T «Evolution of carbohydrate metabolic pathways». Res Microbiol, 147, 6–7, 1996, pàg. 448–55. DOI: 10.1016/0923-2508(96)83998-2. PMID: 9084754.
- ↑ Wöhler, F. «Ueber künstliche Bildung des Harnstoffs.». Ann. Phys. Chem., 12, 1828, pàg. 253-256.
- ↑ Kauffman, G. B. and Chooljian, S.H. «Friedrich Wöhler (1800–1882), on the Bicentennial of His Birth». The Chemical Educator, 6, 2, 2001, pàg. 121-133. DOI: 10.1007/s00897010444a.
Bibliografia complementària[modifica]
- General
- Hunter, Graeme K. Vital Forces: The Discovery of the Molecular Basis of Life. San Diego: Academic Press, 2000. ISBN 0-12-361810-X. OCLC 162129355 191848148 44187710.
- Proceedings of National academy of Science of the United States of America, ISSN 1091-6490 (en línia)
- Llibres de text
- Handbuch der Experimentellen Chemie Sekundarbereich II, Band 11, Biochemie, Aulis Verlag Deubner GmbH & Co. KG * Köln
- Donald Voet et al.: Lehrbuch der Biochemie. Wiley-VCH, 2002, ISBN 3-527-30519-X
- Jeremy M. Berg, Lubert Stryer et al.: Biochemie. 5a edició. Spektrum Akademischer Verlag, 2003, ISBN 3-8274-1303-6, versió en línia en anglès
- David L. Nelson, Michael M. Cox: Lehninger Principles of Biochemistry. 4a edició. Palgrave Macmillan, 2004, ISBN 0-7167-4339-6
- Löffler, Petrides, Heinrich: Biochemie und Pathobiochemie. 8a edició. Springer-Lehrbuch, 2007, ISBN 978-3-540-32680-9
- Werner Müller-Esterl et al.: Biochemie, eine Einführung für Mediziner und Naturwissenschaftler. Spektrum Akademischer Verlag, 2004, ISBN 3-8274-0534-3
- Philipp Christen, Rolf Jaussi: Biochemie. Eine Einführung mit 40 Lerneinheiten. Springer-Verlag, 2005, ISBN 3-540-21164-0
- Andreas Held: Prüfungs-Trainer Biochemie und Zellbiologie. Spektrum Akademischer Verlag, 2005, ISBN 3-8274-1542-X
- Konrad Lechner: Schülerbuch Biochemie. 4a edició. Bayerischer Schulbuch-Verlag, 1998, ISBN 3-7627-4235-9
- Peter Karlson et al.: Kurzes Lehrbuch der Biochemie für Mediziner und Naturwissenschaftler. 14a edició. Thieme, Stuttgart 2005, ISBN 3-13-357814-6
- Graeme K. Hunter: Vital Forces. The discovery of the molecular basis of life. Academic Press, Londres 2000, ISBN 0-12-361811-8
- Joachim Rassow, Karin Hauser, Roland Netzker, Rainer Deutzmann: Biochemie. Georg Thieme Verlag, 2006, ISBN 3-13-125351-7
Enllaços externs[modifica]
| A Wikimedia Commons hi ha contingut multimèdia relatiu a: Bioquímica |
- La Llibreria virtual de bioquímica i biologia cel·lular (anglès)
- Biochemistry, 5a edició. Text complet de Berg, Tymoczko i Stryer, cortesia de l'NCBI (anglès)
- Biochemistry, 2a edició. Arxivat 2008-07-05 a Wayback Machine. Text complet de Garrett i Grisham (en anglès)
- Biochemistry Animation Arxivat 2012-06-24 a Wayback Machine. - (animacions Flash narrades) (en anglès)
