Cirrosi hepàtica
La cirrosi hepàtica, cirrosi de Laennec, o simplement cirrosi és una malaltia del fetge caracteritzada per la substitució de teixit del fetge per fibrosi, cicatrius i nòduls de regeneració (protuberàncies que es produeixen com a resultat d'un procés en el qual es regenera el teixit danyat). La paraula «cirrosi» deriva del grec κίρῥος, que significa 'marró' (el color taronja-groc del fetge malalt). Encara que l'entitat clínica es coneixia abans, va ser René Laennec qui li va donar el nom de «cirrosi» en el seu treball de 1819.[1][2]
La prevalença d'aquesta malaltia a Catalunya era -el desembre de 2012- de 460 casos per 100.000 habitants, amb una mortalitat anyal del 9,1%.[3]
Causes[modifica]
La cirrosi és més comunament causada per l'alcoholisme, l'hepatitis B i C, i l'esteatosi hepàtica, però té moltes altres causes possibles, com ara l'hepatitis autoimmunitària,[4] l'hemocromatosi, la malaltia de Wilson[5] o per la infecció del tremàtode Clonorchis sinensis. Alguns casos són idiopàtics, és a dir, de causa desconeguda.
Una forma particular de cirrosi hepàtica és la cirrosi familiar associada amb mutacions als gens KRT18 i KRT8, ubicats els dos al braç llarg del cromosoma 12 (12q13) i que codifiquen determinades queratines.[6]
Encara que algun tipus d'afectació hepàtica és habitual en les persones que pateixen una fibrosi quística, només en un 5–10% de elles apareix cirrosi i hipertensió portal. A hores d'ara no s'han identificat clarament els factors que condicionen el desenvolupament de la cirrosi en aquests malalts i no és freqüent detectar-la abans que siguin evidents els seus signes característics. En nens, la forma predominant és la cirrosi multilobular i acostuma a ser diagnosticada als 8-10 anys de vida, si bé ha estat descrit algun cas de cirrosi neonatal.[7] En adults, generalment, s'observa una colangitis biliar primària que poques vegades progressa cap a una cirrosi genuïna.[8]
Quasi un 50% dels nens amb síndrome d'Alagille desenvolupen una cirrosi dins de l'espectre d'alteracions del fetge propi de la malaltia.[9] D'ells, un ~15% evoluciona cap a un estat hepàtic terminal i necessiten trasplantament.[10]
Algunes persones que pateixen la malaltia de Rendu-Osler-Weber (telangièctasi hemorràgica hereditària), una forma d'angiodisplàsia autosòmica dominant, poden desenvolupar derivacions arteriovenoses causants d'una cirrosi congestiva.[11]
Un 37% dels adults afectats pel fenotip PiZZ de la deficiència d'alfa-1-antitripsina presenta una cirrosi en el moment de la seva mort. Aproximadament, en un 2–3% dels nens que pateixen aquesta malaltia apareix una fibrosi hepàtica que progressa cap a una cirrosi tributària de trasplantament.[12]
La colèstasi intrahepàtica progressiva familiar tipus 3,[13] una malaltia congènita rara derivada de mutacions en el gen ABCB4 (7q21), provoca cirrosis biliars en individus joves.[14] Una altra malaltia poc comuna és la cirrosi hereditària dels indis nord-americans,[15] fins ara una patologia autosòmica recessiva identificada només en els indígenes del nord-oest del Quebec.[16]
Diverses glicogenosis poden cursar amb una cirrosi (I, IIIa, IV).[17] D'entre elles cal destacar el tipus IV (Malaltia d'Andersen) i, per la seva especial gravetat, el subtipus hepàtic progressiu.[18] En algun cas ha sigut tractada amb èxit una cirrosi secundària a glicogenosi realitzant trasplantaments de cèl·lules de moll d'os autòlegs.[19]
Una etiologia rara de la cirrosi en adults és un hipopituïtarisme congènit no tractat.[20] Ocasionalment, la malaltia té el seu origen en un panhipopituïtarisme resultant de l'absència del tronc hipotàlam-hipofisari.[21]
La síndrome de Budd-Chiari (disminució del flux de sortida hepàtic, generalment a conseqüència de trombosi de les venes suprahepàtiques per coagulopatia o compressió/obstrucció de dits vasos per un tumor) és una causa infreqüent de cirrosi.[22] En la forma crònica de la síndrome l'afectació de la funció hepàtica és moderada i de progressió lenta, mentre que predominen els signes d'hipertensió portal.[23] Histològicament, es poden presentar dos patrons principals de cirrosi: veno-portal (amb fibrosi dels espais porta del fetge) o veno-cèntrica (congestiva).[24]
La insuficiència cardíaca dreta crònica ocasiona una congestió passiva hepàtica amb necrosi zonal i progressió cap a la fibrosi lobular central.[25] La cirrosi d'origen cardíac, però, és rara i avui dia els especialistes integren aquests canvis dins del terme 'fibrosi hepàtica congestiva de grau IV'.[26]
La fasciolosi, una zoonosi provocada pel trematode Fasciola hepatica, origina amb certa freqüència cirrosi en animals herbívors i, eventualment, en humans que beuen aigua contaminada pel paràsit o mengen vegetals crus que contenen els seus ous.[27]
S'ha observat l'associació d'un polimorfisme de nucleòtids simples en el gen RASGRF2 i la cirrosi alcohòlica, però no entre aquesta variant genètica i l'alcoholisme. La possessió de l'al·lel A de dit polimorfisme representa un risc major de desenvolupar l'esmentada forma de cirrosi que el que té la resta de la població.[28]
Es parla de cirrosi criptogènica quan no es poden identificar les causes de la malaltia. En alguns casos pot ser conseqüència de mutacions en factors protrombòtics (Factor V Leiden o l'inhibidor del activador del plasminogen, per exemple).[29] En altres, la causa oculta resulta ser una sitosterolèmia,[30] un trastorn metabòlic autosòmic recessiu.[31]
La pseudocirrosi és un conjunt de canvis morfològics al fetge molt similar al que presenta una cirrosi genuïna, però sense les alteracions histopatològiques característiques d'aquesta. Acostuma a presentar-se en malalts amb càncer metastàtic de mama, encara que ha estat descrita en altres tips de neoplàsies. Sovint s'acompanya d'hipertensió portal.[32] Altres processos que poden provocar-la són la sarcoïdosi, l'esquistosomiasi, la fibrosi congènita hepàtica, la síndrome de Rendu-Osler-Weber,[33] o la hiperplàsia nodular regenerativa del fetge.[34]
Signes i símptomes[modifica]

La cirrosi té moltes possibles manifestacions. Aquests signes i símptomes poden ser com a resultat directe del fracàs de les cèl·lules del fetge per lesió citopàtica o com a resultat de la hipertensió portal. També hi ha algunes manifestacions sense una causa específica però que poden ocórrer en la cirrosi.[36]
Disfunció del fetge[modifica]
- Aranyes vasculars. No sorgeixen exclusivament en la cirrosi.[37] Són lesions vasculars formades per una arteriola central envoltada de petits vasos que s'aprecien sobretot a la cara, el tronc i les extremitats superiors. Encara que la seva patogènia és dubtosa, es creu que són producte d'una alteració del metabolisme de les hormones sexuals. En els cirròtics, el seu nombre i la seva mida es relacionen amb la probabilitat de presentar una hemorràgia digestiva i/o una síndrome hepatopulmonar.
- Eritema palmar. S'acostuma a veure en les eminències tènars i hipotènars.[38] És un signe poc específic, ja que també apareix en altres malalties, com ara l'hipertiroïdisme o l'artritis reumatoide. En casos de cirrosi moltes vegades s'acompanya de canvis en les ungles. Especialment, de bandes o franges horitzontals blanquinoses separades per zones de color normal (ungles de Muehrcke) atribuïbles a un estat d'hipoalbuminèmia crònica.[39]
- Ginecomàstia. La seva causa és l'hiperestrogenisme derivat d'un catabolisme hormonal hepàtic incompetent.
- Hipogonadisme. Es considera que és principalment una conseqüència directa del consum d'alcohol, més que un resultat de la cirrosi per se. De fet, a banda de les cirrosis relacionades amb l'alcoholisme, s'observa en l'hemocromatosi (patologia que produeix un dipòsit de ferro en la hipòfisi i en els testicles) i no en cirrosis de qualsevol altre etiologia. En els homes, es produeix atròfia testicular, impotència i oligospèrmia (producció de semen disminuïda o de qualitat deficient). En les dones, és característica l'oligomenorrea acompanyada de baixos nivells d'estradiol i progesterona. Els dos sexes presenten alts índexs d'infertilitat, canvis en els caràcters sexuals secundaris i pèrdua de la libido.[40]
- Ascites. Alguns malalts cursen amb una ascites quilosa[41] que empitjora el pronòstic vital, acompanyada ocasionalment de quilotòrax.[42] L'ascites (retenció de líquid en la cavitat abdominal) és la complicació més freqüent de la cirrosi i que s'associa amb una pobra qualitat de vida, més risc d'infecció, i una evolució dolenta al llarg termini.[43] En cirròtics amb una ascites extrema es pot produir la ruptura d'una hèrnia abdominal o un hidrotòrax.[44] Els pacients ascítics són molt proclius a desenvolupar una peritonitis bacteriana espontània (PBE). És a dir, una infecció del líquid ascític (LA) sense una aparent font patogèna intraabdominal. Un 10-30% dels cirròtics hospitalitzats amb ascites tenen una PBE. Es una complicació greu i amb una recurrència elevada (el 70% de los malalts pateixen una recidiva en el decurs de l'any posterior al primer episodi i la seva taxa de mortalitat és alta, del 50-70%). Tots els pacients que es recuperen d'una PBE han de ser considerats possibles candidats a trasplantament. El mecanisme que inicia la PBE és la translocació bacteriana, procés pel qual les bactèries entèriques i els seus subproductes (endotoxines i ADN) creuen la barrera mucosa de l'intestí i infecten els ganglis limfàtics mesentèrics, arribant a la circulació sanguínia i després al LA. Els cirròtics que presenten una disminució de les proteïnes totals en el LA tenen un major risc de desenvolupar una PBE, ja que la capacitat d'opsonització d'aquest és escassa. El diagnòstic de PBE requereix una paracentesi, amb una presència en el LA de leucòcits polimorfonuclears ≥ 250/μl. La sospita de PBE fa necessari un tractament antibiòtic empíric, que pot modificar-se després segons els resultats de l'antibiograma. En els cirròtics amb criteris de risc de PBE és recomanable una profilaxi antibiòtica.[45]
- Fetor hepaticus. Mal alè característic provocat per la producció de tiols (en especial metanotiol), en el context d'una alteració del metabolisme de la metionina.[46]
- Icterícia. Originada per hiperbilirubinèmia directa.[47]
Hipertensió portal[modifica]
- Esplenomegàlia.[36] Clàssicament, l'esplenomegàlia en les cirrosis s'ha atribuït la congestió passiva crònica venosa subsegüent a l'hipertensió portal. Ara bé, no ha estat demostrada una correlació entre la mida de la melsa i el grau de pressió portal o l'existència de VEs. Diversos estudis anatomopatològics han evidenciat que -a més del segrest sanguini en la polpa vermella- es produeix un augment de la polpa blanca, increment del teixit reticuloendotelial, elevació del nombre de miofibroblasts subcapsulars i creixement progressiu de les artèries terminals. Per això, avui dia es considera que l'esplenomegàlia cirròtica és també de naturalesa hiperplàsica i està directament relacionada amb el procés de fibrogènesi hepàtica.[48]
- Varius esofàgiques (VE). És la complicació fatal més freqüent de la cirrosi. En el moment del diagnòstic, aproximadament un 30% dels cirròtics tenen aquesta patologia, arribant al 90% als 10 anys posteriors a la detecció de la cirrosi. El sagnat pot remetre espontàniament en alguns casos, però te té una taxa de mortalitat de -almenys- un 20% a las 6 setmanes de l'inici del quadre hemorràgic. Un diàmetre de la vena porta> 13 mm i la presència de trombocitopènia són elements predictius de la probabilitat de l'aparició de VEs en un cirròtic. La cirrosis descompensada (Child-Pugh B/C), la d'etiologia alcohòlica i la existència de marques vermelles semblants a fuetades en la endoscòpia basal són factors que afavoreixen la progressió de les VEs. Una mida de >5 mm amb senyals petequials, puntuacions CTP (Child-Turcotte-Pugh)[49] o MELD elevades, persistència en el consum d'alcohol, pressió alta de la vena porta (GPVH >16) i coagulopatia són indicadors que precedeixen a un episodi de sagnat varicós. L'esofagogastroduodenoscòpía és el mètode diagnòstic d'elecció. El diagnòstic diferencial de la hemorràgia per VEs inclou totes les etiologies d'un sagnat gastrointestinal alt. Les úlceres pèptiques són també freqüents en els individus cirròtics.[50]
- Caput medusae. Dilatació tortuosa de les venes periumbilicals, consegüent a una hipertensió portal greu, que té un aspecte molt particular.[51]
Complicacions[modifica]
Complicacions potencialment mortals són l'encefalopatia hepàtica (confusió i coma) i l'hemorràgia per varius esofàgiques.[52]
Els cirròtics tenen una marcada tendència a sofrir ictus hemorràgics a causa de les alteracions de la coagulació consegüents a la malaltia.[53]
La trombosi portal és una complicació freqüent de la cirrosi que s'acompanya d'un fenotip protrombòtic. Les seves conseqüències són greus, atès que comporta un deteriorament addicional d'estat clínic i s'associa a un increment de la morbiditat i mortalitat peritrasplantament hepàtic, arribant a constituir una contraindicació per efectuar dit tipus de cirurgia. A banda d'instaurar tractament anticoagulant precoç, la pràctica d'una derivació porto-sistèmica percutània intrahepàtica és tècnicament possible en les trombosis sense transformació cavernomatosa i s'aconsegueix una recanalització del vas en una proporció significativa de casos.[54]
Progressió de la malaltia[modifica]
En la cirrosi es distingeixen clarament dues etapes diferents. Per regla general, cursa amb un període inicial de duració variable (cirrosi compensada) asimptomàtic o amb símptomes molt inespecífics, com ara dispèpsia, astènia, pèrdua de la capacitat de concentració, hipotensió o hiperpirèxia. Als 10 anys, la supervivència dels pacients que es mantenen en aquesta fase s'acosta al 80%. L'aparició d'hipertensió portal en el període inicial és un signe de mal pronòstic.[55]
La cirrosi compensada pot evolucionar a cirrosi descompensada, apareixent llavors els signes clàssics de gravetat: icterícia, ascites, hemorràgia per VEs, síndrome hepatorenal i encefalopatia hepàtica. Sense el tractament oportú la supervivència dels malalts que arriben a aquesta etapa és del ~7%.[56] La cirrosi descompensada comporta una remodelació del col·lagen tipus III del fetge (abundant en els vasos i les cèl·lules estelades)[57] que accelera el seu dipòsit i indueix el desenvolupament d'un fracàs hepàtic irreversible.[58]
Diagnosi[modifica]
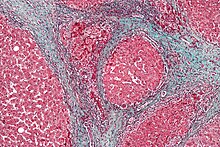
L'estàndard d'or per al diagnòstic de la cirrosi és una biòpsia hepàtica, generalment a través d'una punció percutània amb agulla fina. La biòpsia no és necessària si les dades clíniques, de laboratori i radiològiques suggereixen la cirrosi. A més, hi ha un petit però significatiu risc a l'hora de realitzar una biòpsia hepàtica (es produeix una hemorràgia en un 1,7% dels pacients, encara que només en un 0,3-0,5% d'ells és greu);[59] ja que la cirrosi predisposa, per ella mateixa, a determinades complicacions del procediment. Per això, cal seguir els criteris de contraindicació i mantenir les precaucions que indiquen els protocols vigents.[60] Els millors predictors de la cirrosi són l'ascites, el recompte de plaquetes <160.000/mm3, l'aparició d'aranyes vasculars i una puntuació superior a 7 en l'escala de cirrosi de Bonacini,[61] si la malaltia és conseqüència d'una hepatitis C. S'han creat diversos procediments per avaluar les probabilitats de progressió de dita hepatitis cap a la cirrosi.[62]
Proves de laboratori[modifica]
Els següents resultats són típics en la cirrosi:
- Transaminases o aminotrasferases - AST i ALT estan moderadament elevades, amb AST>ALT. No obstant això, els nivells normals de transaminases no s'oposen a la cirrosi.[36] Una marcada elevació de les transaminases en el context d'una cirrosi orienta cap a una agressió d'origen tòxic (fàrmacs o alcohol), una hepatitis vírica afegida o un dany isquèmic derivat de xoc o col·lapse cardiovascular.
- Fosfatases alcalines - una mica elevades, però menys de 2 a 3 vegades del límit superior de la normalitat. Elevacions més altes fan sospitar una cirrosi d'origen biliar (colangitis esclerosant primària o cirrosi biliar primària). També apareixen FAs altes en casos d'hepatocarcinoma.
- Gamma-glutamiltransferasa - (GGT o γ-glutamiltransferasa).[63] El valor d'aquest enzim s'ha de correlacionar amb els nivells de les fosfatases alcalines. En general està molt més elevat en la malaltia hepàtica crònica per alcohol.[64]
- Bilirubina - amb uns nivells normals quan la cirrosi està compensada, però pot elevar-se quan la cirrosi progressa. De fet, la bilirubina és un dels paràmetres utilitzats en la classificació de Child-Pugh per avaluar l'estat de la funció hepàtica. Una bilirubina aixecada constitueix un indicador de mal pronòstic i un dels criteris per indicar un trasplantament.
- Albúmina - els nivells baixen a mesura que la funció de síntesi del fetge amb cirrosi empitjora, ja que l'albúmina és sintetitzada exclusivament al fetge. El gradient albúmina sèrica–albúmina líquid ascític és un valor útil en el diagnòstic diferencial de l'ascites (gradient alt >1,1g/dl: cirrosi, hepatitis alcohòlica, insuficiència cardíaca congestiva; gradient baix <1,1g/dl: carcinomatosi peritoneal, tuberculosi peritoneal, pancreatitis) i també constitueix un indicador poc específic de la gravetat de la hipertensió portal.[65]
- Gammaglobulines - augmentades a causa de la derivació dels antígens bacterians (procedents dels intestins) des del fetge als teixits limfoides. Fonamentalment, aquest fenomen es deu al fet que les bactèries no fagocitades per les cèl·lules de Kupffer hepàtiques estimulen el sistema immune incrementant els nivells sèrics d'Igs. Un valor molt alt d'IgG suggereix una etiologia immune. L'IgM està aixecada en més del 90% dels malalts amb cirrosi biliar primària.
- Hiponatrèmia - o sodi baix en sèrum, a causa de la incapacitat per excretar aigua lliure resultant dels alts nivells de ADH i aldosterona. És una alteració que es veu sovint en els pacients amb ascites.[66]
- Hiperpotassèmia o hipopotassèmia - un potassi en sèrum aixecat s'acostuma a observar en cirròtics tractats amb diürètics d'acció distal (espironolactona, triamterè, amilorida). La hipopotassèmia pot ser conseqüència pèrdues relacionades amb vòmits, diarrea o l'administració de diürètics de nansa i és un dels factors que indueixen el desenvolupament d'encefalopatia.
- Leucopènia i neutropènia - a causa de l'esplenomegàlia amb segrest esplènic.
- Trombocitopènia - generalment multifactorial. A causa de la supressió de la medul·la per l'alcohol, sèpsia, manca d'àcid fòlic, segrest a la melsa (per l'esplenomegàlia), així com la disminució de trombopoetina.[64]
- Factors de coagulació - les coagulopaties són comunes en la cirrosi, ja que el fetge produeix la major part dels factors de coagulació. Per tant, les alteracions analítiques d'aquests es correlacionen amb l'empitjorament de la malaltia hepàtica.[67]
- Temps de protrombina - s'incrementa a causa dels trastorns de la coagulació, fet que afavoreix les hemorràgies.[68]
- Transferrina - la transferrina sèrica i la seva concentració de ferro es consideren elements amb valor predictiu de supervivència en la cirrosi descompensada. Independentment de l'etiologia d'aquesta, una transferrina ≥ 180 mg/dL s'associa amb un bon pronòstic de la malaltia.[69]
- Perfil lipídic - L'anàlisi de lípids en els pacients cirròtics d'etiologia alcohòlica o viral ajuda a identificar el grau de dany hepàtic. Una hipocolesterolèmia (nivell baix de colesterol en la sang) és signe de mal pronòstic i s'associa a la reducció de la síntesi del colesterol i de les seves fraccions en el context de la progressió de la cirrosi.[70]
Estadiatge[modifica]
La gravetat de la cirrosi es classifica comunament amb l'escala de Child-Pugh. Una altra escala d'avaluació adoptada a hores d'ara per xarxes de trasplantaments com Eurotransplant International Foundation o United Network for Organ Sharing és la MELD (acrònim anglès de Model for End-stage Liver Disease), que utilitza fonamentalment els valors sèrics de creatinina i bilirubina i el ràtio internacional normalitzat del temps de protrombina.[71][72] Han estat proposades diverses modificacions per millorar el valor predictiu d'aquesta escala, com ara l'anàlisi del líquid ascític o el nivell de sodi en sèrum.[73] En general, es considera que l'aplicació del sistema MELD redueix la taxa de mortalitat en els malalts que esperen un trasplantament hepàtic, però que no és per se una eina adequada per predir la supervivència del pacient després de realitzada la cirurgia, amb independència del procés causal d'aquest tipus de procediment.[74]
Tractament[modifica]
La cirrosi és generalment irreversible una vegada que es produeix, i el tractament generalment se centra en la prevenció de la progressió i les complicacions. En les fases avançades de la cirrosi l'única opció és un trasplantament de fetge. En les cirrosis hi ha poques proteïnes en sang, i això, juntament amb la dificultat que passi la sang a través del fetge, fa que es generi líquid ascític que s'acumula en la cavitat abdominal i que cada una o dues setmanes s'ha d'evacuar a través de puncions (peritoneocentesis o paracentesis abdominals)[75] quan la medicació (basada en diürètics) i les mesures dietètiques (restricció de la sal) no són efectives i es produeix l'anomenada ascites refractària.[76] L'any 2010, l'Hospital de Sant Pau de Barcelona fou el primer hospital a Espanya en introduir un avanç terapèutic constituent en la implantació d'una bomba automàtica subcutània controlada des d'un ordinador capaç de drenar aquest líquid abdominal. Aquesta innovació evita l'ingrés hospitalari i millora la qualitat de vida dels pacients.[77] Dit dispositiu ocasiona poques complicacions (la major part derivades de problemes amb el carregador o la programació de l'aparell) i les millores en el disseny dels catèters han disminuït el nombre d'obstruccions per cúmuls de fibrina o restes proteíniques.[78] Una altra forma de tractar aquesta ascites i altres complicacions de la hipertensió portal, és practicar una derivació porto-sistèmica percutània intrahepàtica (generalment anomenada TIPS, acrònim anglès de Transjugular Intrahepatic Portosystemic Shunt), procediment que consisteix en crear una comunicació d'un diàmetre prefixat entre la vena porta i la vena cava inferior a través del parènquima hepàtic cateteritzant les venes suprahepàtiques.[79]
A causa de les limitacions del trasplantament ortotòpic hepàtic,[80] durant els darrers anys s'han dissenyat teràpies cel·lulars amb cèl·lules hepatocitàries cultivades, cèl·lules de moll d'os, cèl·lules mare hematopoèsiques i cèl·lules mare mesenquimàtiques per tractar certs casos de cirrosi avançada.[81] El trasplantament d'hepatòcits es considera poc viable, ja que són difícils d'obtenir i el manteniment de la seva funcionalitat sota condicions de criopreservació o en cultius in vitro és gairebé impossible. En canvi, es coneix la capacitat de diferenciació en hepatòcits de les cèl·lules de la medul·la òssia i els estudis clínics amb cèl·lules mare i sense classificar pertanyents a aquesta línia han donat resultats prometedors.[82] A hores d'ara, les cèl·lules mare mesenquimatoses[83] són les que presenten millors perspectives d'aplicació eficaç en el tractament de la cirrosi, encara que els assajos amb elles no estan lliures de certs riscos (tumorigènesi per iatrogènia i embolismes cel·lulars, per exemple).[84]
Segons estudis experimentals en murins, les nanopartícules d'òxid de ceri i determinats antagonistes del receptor V1a de la vasopressina podrien ser elements terapèutics útils per reduir la hipertensió portal consegüent a la cirrosi.[85] Un compost no peptídic agonista de l'angiotensina (1-7), l'AVE0991,[86] aconsegueix in vivo disminuir la pressió portal sense alterar la pressió sistèmica i es considera una nova estratègia farmacològica en el tractament de la hipertensió portal.[87]
Referències[modifica]
- ↑ Laënnec, RTH «De l'auscultation médiate ou Traité du diagnostic des maladies des poumons et du coeur, fondé principalment sur ce nouveau moyen d'exploration» (en francès). Chez J.A. Brosson et J.S. Chaude, Libraires. (rep. Bibliothèque nationale de France), 1819, pp: 368-369 [Consulta: 21 agost 2020].
- ↑ Duffin, JM «Why does cirrhosis belong to Laennec?» (en anglès). CMAJ, 1987 Set 1; 137 (5), pp: 393-396. ISSN: 0820-3946. PMC: 1492806. PMID: 3304599 [Consulta: 21 març 2018].
- ↑ Miquel M, Clèries M, Vergara M, Vela E «Economic burden of cirrhosis in Catalonia: a population-based analysis» (en anglès). BMJ Open, 2018 Mar 3; 8 (3), pp: e018012. DOI: 10.1136/bmjopen-2017-018012. ISSN: 2044-6055. PMC: 5855312. PMID: 29502082 [Consulta: 19 abril 2018].
- ↑ Zubieta-Rodríguez, R; Gómez-Correa, J; Rodríguez-Amaya, R «Cirrosis hepática por hepatitis autoinmune: Serie de casos y revisión de la literatura» (en castellà). Revista Médicas UIS, 2016 Set 1; 29 (2), pp: 175-182. DOI: 10.18273/revmed.v29n2-2016015. ISSN: 1794-5240 [Consulta: 21 març 2018].
- ↑ Gómez Ayala, AE «Cirrosis hepática. Actualización» (en castellà). Farmacia Profesional, 2012 Jul-Ag; 26 (4), pp: 45-51. ISSN: 0213-9324 [Consulta: 21 març 2018].
- ↑ O'Neill, MJF «Cirrhosis, Familial» (en anglès). OMIM, 2005 Set 29; #215600, pp: 5 [Consulta: 4 abril 2018].
- ↑ Feigelson J, Anagnostopoulos C, Poquet M, Pecau Y, et al «Liver cirrhosis in cystic fibrosis--therapeutic implications and long term follow up» (en anglès). Arch Dis Child, 1993 Maig; 68 (5), pp: 653–657. ISSN: 0003-9888. PMC: 1029335. PMID: 8280210 [Consulta: 22 març 2018].
- ↑ Flass T, Narkewicz MR «Cirrhosis and other liver disease in cystic fibrosis» (en anglès). J Cyst Fibros, 2013 Mar; 12 (2), pp: 116-124. DOI: 10.1016/j.jcf.2012.11.010. PMC: 3883947. PMID: 23266093 [Consulta: 22 març 2018].
- ↑ Lykavieris P, Hadchouel M, Chardot C, Bernard O «Outcome of liver disease in children with Alagille syndrome: a study of 163 patients» (en anglès). Gut, 2001 Set; 49 (3), pp: 431-435. ISSN: 1468-3288. PMC: 1728437. PMID: 11511567 [Consulta: 22 març 2018].
- ↑ Spinner, NB; Leonard, LD, Krantz, ID «Alagille Syndrome» (en anglès). GeneReviews® [Internet]. University of Washington, 2013 Feb 28; NBK1273 (rev), pàgs: 24. PMID: 20301450 [Consulta: 22 març 2018].
- ↑ Leitão P, Carvalho A, Guerra C, Gonçalves J, Ramos I «Congestive cirrhosis in Osler-Weber-Rendu syndrome: A rare case report» (en anglès). Radiol Case Rep, 2017 Nov 6; 13 (1), pp: 51-54. DOI: 10.1016/j.radcr.2017.10.011. PMC: 5851303. PMID: 29552242 [Consulta: 4 abril 2018].
- ↑ Fairbanks KD, Tavill AS «Liver Disease in Alpha 1-Antitrypsin Deficiency: A Review» (en anglès). Am J Gastroenterol, 2008 Ag; 103 (8), pp: 2136-2141. Arxivat de l'original el 20 de setembre 2018. DOI: 10.1111/j.1572-0241.2008.01955.x. ISSN: 0002-9270. PMID: 18796107 [Consulta: 1r abril 2018].
- ↑ Orphanet «Progressive familial intrahepatic cholestasis type 3» (en anglès). Rare diseases, 2018 Abr 18; 79305 (rev), pàgs: 5 [Consulta: 19 abril 2018].
- ↑ Sun GR, Burns M «Progressive Familial Intrahepatic Cholestasis: A Rare Cause of Cirrhosis in Young Adult Patients» (en anglès). Case Rep Med, 2015 Jun; 2015, pp: 428638. DOI: 10.1155/2015/428638. PMC: 4468343. PMID: 26136783 [Consulta: 18 abril 2018].
- ↑ Orphanet «Hereditary North American Indian childhood cirrhosis» (en anglès). Rare diseases, 2018 Abr 18; 168583 (rev), pàgs: 3 [Consulta: 19 abril 2018].
- ↑ Richter A, Mitchell GA, Rasquin A «La cirrhose amérindienne infantile» (en francès). Med Sci (Paris), 2007 Nov; 23 (11), pp: 1002-1007. DOI: 10.1051/medsci/200723111002. ISSN: 1958-5381. PMID: 18021715 [Consulta: 19 abril 2018].
- ↑ Zobeiri, M «Liver Transplantation in a Myopathic Patient with Glycogen Storage Disease Type IIIa and Decompensated Cirrhosis» (en anglès). Int J Organ Transplant Med, 2017; 8 (4), pp: 217-220. ISSN: 2008-6490. PMC: 5756905. PMID: 29321839 [Consulta: 1r abril 2018].
- ↑ Magoulas, PL; El-Hattab, AW «Glycogen Storage Disease Type IV» (en anglès). GeneReviews® [Internet]. University of Washington, 2013 Gen 3; NBK115333, pàgs: 15. PMID: 23285490 [Consulta: 1r abril 2018].
- ↑ Wehbe TW, Abi Chahine NH, Annous AA3, Ferri MA, et al «A case report of congenital glycogen storage liver cirrhosis treated with bone marrow derived stem cells» (en anglès). Stem Cell Investig, 2017 Set 7; 4, pp: 73. DOI: 10.21037/sci.2017.07.04. PMC: 5638994. PMID: 29057245 [Consulta: 1r abril 2018].
- ↑ Nyunt A, Kochar N, Pilz DT, Kingham JG, Jones MK «Adult cirrhosis due to untreated congenital hypopituitarism» (en anglès). J R Soc Med, 2005 Jul; 98 (7), pp: 316–317. DOI: 10.1258/jrsm.98.7.316. PMC: 1168917. PMID: 15994594 [Consulta: 2 maig 2018].
- ↑ Gonzalez Rozas M, Hernanz Roman L, Gonzalez DG, Pérez-Castrillón JL «Panhypopituitarism due to Absence of the Pituitary Stalk: A Rare Aetiology of Liver Cirrhosis» (en anglès). Case Rep Endocrinol, 2016 Abr; 2016, pp: 9071097. DOI: 10.1155/2016/9071097. PMC: 4860241. PMID: 27213061 [Consulta: 3 maig 2018].
- ↑ Grus T, Lambert L, Grusová G, Banerjee R, Burgetová A «Budd-Chiari syndrome» (en anglès). Prague Med Rep, 2017; 118 (2-3), pp: 69-80. DOI: 10.14712/23362936.2017.6. ISSN: 1214-6994. PMID: 28922103 [Consulta: 4 abril 2018].
- ↑ Lin M, Zhang F, Wang Y, Zhang B, et al «Liver cirrhosis caused by chronic Budd-Chiari syndrome» (en anglès). Medicine (Baltimore), 2017 Ag; 96 (34), pp: e7425. DOI: 10.1097/MD.0000000000007425. PMC: 5571988. PMID: 28834866 [Consulta: 4 abril 2018].
- ↑ Tanaka M, Wanless IR «Pathology of the Liver in Budd-Chiari Syndrome: Portal Vein Thrombosis and the Histogenesis of Veno-Centric Cirrhosis, Veno-Portal Cirrhosis, and Large Regenerative Nodules» (en anglès). Hepatology, 1998 Feb; 27 (2), pp: 488-496. DOI: 10.1002/hep.510270224. ISSN: 0270-9139. PMID: 9462648 [Consulta: 4 abril 2018].
- ↑ Baialardo, AG «Síndrome cardio-hepático. ¿Qué debemos saber como cardiólogos?» (en castellà). Insuf Card, 2015; 10 (2), pp: 66-77. ISSN: 1852-3862 [Consulta: 4 abril 2018].
- ↑ Dai DF, Swanson PE, Krieger EV, Liou IW, et al «Congestive hepatic fibrosis score: a novel histologic assessment of clinical severity» (en anglès). Mod Pathol, 2014 Des; 27 (12), pp: 1552-1558. DOI: 10.1038/modpathol.2014.79. ISSN: 1530-0285. PMID: 24925051 [Consulta: 4 abril 2018].
- ↑ Machicado C, Machicado JD, Maco V, Terashima A, Marcos LA «Association of Fasciola hepatica Infection with Liver Fibrosis, Cirrhosis, and Cancer: A Systematic Review» (en anglès). PLoS Negl Trop Dis, 2016 Set; 10 (9), pp: e0004962. DOI: 10.1371/journal.pntd.0004962. PMC: 5040415. PMID: 27681524 [Consulta: 4 abril 2018].
- ↑ Novo-Veleiro I, Cieza-Borrella C, Pastor I, Chamorro AJ, et al «A Single Nucleotide Polymorphism in the RASGRF2 Gene Is Associated with Alcoholic Liver Cirrhosis in Men» (en anglès). PLoS One, 2016 Des 19; 11 (12), pp: e0168685. DOI: 10.1371/journal.pone.0168685. PMC: 5167392. PMID: 27992614 [Consulta: 15 abril 2018].
- ↑ Monereo Muñoz M, Aguilera García SG, de la Barreda Heusser R, González Arnay E, et al «Cirrosis hepática criptogenética y mutaciones de factores protrombóticos, ¿una mera asociación?» (en castellà). Rev Esp Enferm Dig, 2016 Set; 108 (9), pp: 588-591. DOI: 10.17235/reed.2015.3871/2015. ISSN: 1130-0108. PMID: 26785615 [Consulta: 4 abril 2018].
- ↑ Escolà-Gil, JC; Quesada, H; Julve, J; Martín-Campos, JM; et al «Sitosterolemia: diagnosis, investigation, and management» (en anglès). Curr Atheroscler Rep, 2014 Jul; 16 (7), pp: 424. DOI: 10.1007/s11883-014-0424-2. ISSN: 1523-3804. PMID: 24821603 [Consulta: 20 agost 2020].
- ↑ Bazerbachi F, Conboy EE, Mounajjed T, Watt KD, et al «Cryptogenic Cirrhosis and Sitosterolemia: A Treatable Disease If Identified but Fatal If Missed» (en anglès). Ann Hepatol, 2017 Nov-Des; 16 (6), pp: 970-978. DOI: 10.5604/01.3001.0010.5290. ISSN: 1665-2681. PMID: 29055934 [Consulta: 4 abril 2018].
- ↑ Adike A, Karlin N, Menias C, Carey EJ «Pseudocirrhosis: A Case Series and Literature Review» (en anglès). Case Rep Gastroenterol, 2016 Jul 29; 10 (2), pp: 381-391. DOI: 10.1159/000448066. PMC: 5043255. PMID: 27721722 [Consulta: 5 abril 2018].
- ↑ Garcia-Tsao, G «Liver involvement in hereditary hemorrhagic telangiectasia (HHT)» (en anglès). J Hepatol, 2007 Mar; 46 (3), pp: 499-507. DOI: 10.1016/j.jhep.2006.12.008. ISSN: 0168-8278. PMID: 17239481 [Consulta: 21 agost 2020].
- ↑ Jha P, Poder L, Wang ZJ, Westphalen AC, et al «Radiologic mimics of cirrhosis» (en anglès). AJR Am J Roentgenol, 2010 Abr; 194 (4), pp: 993-999. DOI: 10.2214/AJR.09.3409. ISSN: 1546-3141. PMID: 20308502 [Consulta: 5 abril 2018].
- ↑ Sinniah, R «A clinicopathological study of micronodular and macronodular cirrhosis in Belfast, Northern Ireland» (en anglès). Ulster Med J, 1972 Summer; 41 (2), pp: 121-134. ISSN 0041-6193. PMC: 2385380. PMID: 5084690 [Consulta: 14 desembre 2015].
- ↑ 36,0 36,1 36,2 Friedman, LS. Liver, Biliary Tract, & Pancreas Disorders. A: Current medical diagnosis and treatment 2014, Chap. 16 (Papadakis MA, McPhee SJ; Eds.) Mcgraw-Hill Education, 2014, pp: 641-697. ISBN 978-0-07-180634-3.[Enllaç no actiu]
- ↑ Samant, H; Kothadia, JP «Spider Angioma» (en anglès). StatPearls [Internet]. StatPearls Publishing LLC, 2020 Gen 29; NBK507818 (rev), págs: 4. PMID: 29939595 [Consulta: 20 agost 2020].
- ↑ Civan, JM «Cirrosis (eritema palmar)» (en castellà). A: Cirrosis, Manuales MSD (Versión para profesionales). Merck Sharp & Dohme Corp, 2018; Mar (rev), pàgs: 1 [Consulta: 21 agost 2020].
- ↑ Muehrcke, RC «The Finger-nails in Chronic Hypoalbuminaemia» (en anglès). Br Med J, 1956 Jun 9; 1 (4979), pp: 1327-1328. ISSN: 0007-1447. PMC: 1980060. PMID: 13316143 [Consulta: 31 maig 2018].
- ↑ Bernal, V; Bosch, J «Cirrosis hepàtica» (en castellà). A: Gastroenterología y Hepatología. Problemas comunes en la práctica clínica; Secc. 6, Cap. 60. Jarpyo Editores, SA, 2012, pp: 867-892. ISBN 978-84-92982-31-8 [Consulta: 30 maig 2018].
- ↑ Barlas S, Awad AH, Khan KA, Rashid Safdar MU «Chylous ascites: A rare complication of liver cirrhosis» (en anglès). Ann Saudi Med, 1993 Jul; 13 (4), pp: 372-374. DOI: 10.5144/0256-4947.1993.372. ISSN: 0975-4466. PMID: 17590704 [Consulta: 3 abril 2018].
- ↑ Caballería Rovira, R; Aragó López, JV; Sala Auvi, AM; Sanchís Closa, A «Ascitis quilosa y quilotórax en un caso de cirrosis hepática» (en castellà). Arch Bronconeumol, 1985 Set-Oct; 21 (5), pp: 251-252. DOI: 10.1016/S0300-2896(15)32118-9. ISSN: 0300-2896 [Consulta: 3 abril 2018].
- ↑ Ortega, R; Ginès, P «Ascitis en la cirrosis hepática» (en castellà). Med Integr, 2001 Jun; 38 (2), pp: 49-51. ISSN: 0210-9433 [Consulta: 21 març 2018].
- ↑ Lv Y, Han G, Fan D «Hepatic Hydrothorax» (en anglès). Ann Hepatol, 2018 Gen-Feb; 17 (1), pp: 33-46. DOI: 10.5604/01.3001.0010.7533. ISSN: 1665-2681. PMID: 29311408 [Consulta: 21 març 2018].
- ↑ Fernández, I «Peritonitis bacteriana espontánea» (en castellà). XIX Curso de Postgrado AGA-SEPD. Sesión IV: Enfermedades hepáticas, 2012 Jun, pags: 4. Arxivat de l'original el 2013-07-11 [Consulta: 30 març 2018]. Arxivat 2013-07-11 a Wayback Machine.
- ↑ Challenger F, Walshe JM «Methyl mercaptan in relation to foetor hepaticus» (en anglès). Biochem J, 1955 Mar; 9 (3), pp: 372-375. ISSN: 0264-6021. PMC: 1216252. PMID: 14363103 [Consulta: 21 març 2018].
- ↑ Krafts, K «Gastrointestinal pathology: Conjugated vs. unconjugated bilirubinèmia» (en anglès). Pathology Student. University of Minnesota, 2009; Oct 30, pàgs: 3 [Consulta: 31 maig 2018].
- ↑ Li L, Duan M, Chen W, Jiang A, et al «The spleen in liver cirrhosis: revisiting an old enemy with novel targets» (en anglès). J Transl Med, 2017 Maig 23; 15 (1), pp: 111. DOI: 10.1186/s12967-017-1214-8. PMC: 5442653. PMID: 28535799 [Consulta: 31 maig 2018].
- ↑ Hepatitis C Online. «Child-Turcotte-Pugh (CTP) Calculator» (en anglès). Tools&Calculators, 2020; Version 2.11.0. [Consulta: 18 agost 2020].
- ↑ LaBrecque, D; Khan, AG; Sarin, SK; Le Mair, AW «Varices esofágicas» (en castellà). Guías mundiales de la Organización Mundial de Gastroenterología- OMG, 2015 Gen, pàgs: 15 [Consulta: 15 abril 2018].
- ↑ Sharma, B; Raina, S «Caput Medusae» (en anglès). Indian J Med Res, 2015 Abr; 141 (4), pp: 494. DOI: 10.4103/0971-5916.159322. PMC: 4510739. PMID: 26112857 [Consulta: 21 març 2018].
- ↑ Ashkenazi E, Kovalev Y, Zuckerman E «Evaluation and treatment of esophageal varices in the cirrhotic patient» (en anglès). Isr Med Assoc J, 2013 Feb; 15 (2), pp: 109-115. ISSN: 1565-1088. PMID: 23516775 [Consulta: 21 març 2018].
- ↑
- ↑ Bañares, R; Catalina, MV «Tratamiento de la trombosis portal no tumoral en la cirrosis» (en castellà). Gastroenterol Hepatol, 2014 Jul; 37 (Supl 2), pp: 62-67. DOI: 10.1016/S0210-5705(14)70071-8. ISSN: 0210-5705. PMID: 25087714 [Consulta: 30 març 2018].
- ↑ Quiroga, J «Cuidados de la cirrosis compensada» (en castellà). Rev Esp Enferm Dig, 2008 Abr; 100 (4), pp: 243. ISSN: 1130-0108. PMID: 18567183 [Consulta: 19 abril 2018].
- ↑ Álvarez González, MA «Curso clínico de la cirrosis descompensada -Tesi doctoral-» (en castellà). Departament de Medicina. Universitat Autònoma de Barcelona, 2013 Oct, pp: 91. ISBN 9788449041969 [Consulta: 21 març 2018].
- ↑ Krishna, M «Anatomía microscópica del hígado» (en castellà). Clinical Liver Disease, 2013 Nov; 55 (2-Supl 2), pp: 109-112. DOI: 10.1002/cld.287. ISSN: 2046-2484 [Consulta: 21 abril 2018].
- ↑ Praktiknjo M, Lehmann J, Nielsen MJ, Schierwagen R, et al «Acute decompensation boosts hepatic collagen type III deposition and deteriorates experimental and human cirrhosis» (en anglès). Hepatol Commun, 2018 Gen 18; 2 (2), pp: 211-222. DOI: 10.1002/hep4.1135. PMC: 5796334. PMID: 29404528 [Consulta: 21 abril 2018].
- ↑ García González, M; Senosiaín Lalastra, C «Biopsia hepática percutània» (en castellà). Rev Esp Enferm Dig, 2013 Feb; 105 (2), pàgs: 2. DOI: 10.4321/S1130-01082013000200011. ISSN: 1130-0108 [Consulta: 26 juny 2018].
- ↑ Grant, A; Neuberger J «Guidelines on the use of liver biopsy in clinical practice» (en anglès). Gut, 45, Supl 4, 1999 Oct, pp: 1–11. DOI: 10.1136/gut.45.2008.iv1. ISSN: 0017-5749. PMC: 1766696. PMID: 10485854. «The main cause of mortality after percutaneous liver biopsy is intraperitoneal haemorrhage as shown in a retrospective Italian study of 68 000 percutaneous liver biopsies in which all six patients who died did so from intraperitoneal haemorrhage. Three of these patients had had a laparotomy, and all had either cirrhosis or malignant disease, both of which are risk factors for bleeding.»
- ↑ Udell, JA; Wang, CS, Tinmouth, J, FitzGerald, JM, Ayas, NT, Simel, DL, Schulzer, M, Mak, E, Yoshida, EM «Does this patient with liver disease have cirrhosis?» (en anglès). Journal of the American Medical Association, 307, 8, 22-02-2012, pp: 832–842. DOI: 10.1001/jama.2012.186. ISSN: 0098-7484. PMID: 22357834 [Consulta: 26 juny 2018].
- ↑ EBMcalc «Cirrhosis Probability in Hepatitis C MultiCalc» (en anglès). Foundation Internet Services, 2017; 254891 v17.4, pàgs: 3 [Consulta: 21 març 2018].
- ↑ International Union of Biochemistry and Molecular Biology «EC 2.3.2.2 (γ-glutamyltransferase)» (en anglès). Enzyme Nomenclature, 2011 (rev), pàgs: 2 [Consulta: 23 març 2018].
- ↑ 64,0 64,1 Maddrey, edited by Eugene R. Schiff, Michael F. Sorrell & Willis C.. Schiff's diseases of the liver.. 11th ed. / edited by Eugene R. Schiff, Willis C. Maddrey, Michael F. Sorrell.. Chichester, West Sussex, UK: John Wiley & Sons, 1999, p. Evaluation of the Liver A: Laboratory Test. ISBN 978-0-470-65468-2.
- ↑ Shahed FHM, Mamun-Al-Mahtab, Rahman S «The Evaluation of Serum Ascites Albumin Gradient and Portal Hypertensive changes in Cirrhotic Patients with Ascites» (en anglès). Euroasian J Hepatogastroenterol, 2016 Gen-Jun; 6 (1), pp: 8-9. DOI: 10.5005/jp-journals-10018-1157. PMC: 5578550. PMID: 29201716 [Consulta: 9 juny 2018].
- ↑ Ginés, P, Guevara, M «Hyponatremia in Cirrhosis: Pathogenesis, Clinical Significance, and Management» (en anglès). Hepatology, 2008 Set; 48 (3), pp: 1002-1010. DOI: 10.1002/hep.22418. ISSN: 1527-3350. PMID: 18671303 [Consulta: 21 agost 2020].
- ↑ Téllez-Ávila, F;, Chávez-Tapia, NC; Torre-Delgadillo, A «Trastornos de coagulación en el cirrótico» (en castellà). Rev Invest Clín, 2007 Mar-Abr; 59 (2), pp: 153-160. ISSN: 0034-8376. PMID: 17633804 [Consulta: 23 abril 2018].
- ↑ Tripodi A, Caldwell SH, Hoffman M, Trotter JF, Sanyal AJ «Review article: the prothrombin time test as a measure of bleeding risk and prognosis in liver disease» (en anglès). Aliment Pharmacol Ther, 2007 Jul 15; 26 (2), pp: 141-148. DOI: 10.1111/j.1365-2036.2007.03369.x. ISSN: 1365-2036. PMID: 17593061 [Consulta: 21 març 2018].
- ↑ Viveiros A, Finkenstedt A, Schaefer B, Mandorfer M, et al «Transferrin as a predictor of survival in cirrhosis» (en anglès). Liver Transpl, 2018 Mar; 24 (3), pp: 343-351. DOI: 10.1002/lt.24981. PMC: 5873434. PMID: 29149510 [Consulta: 21 abril 2018].
- ↑ Boemeke L, Bassani L, Marroni CA1, Gottschall CB «Lipid profile in cirrhotic patients and its relation to clinical outcome» (en anglès). Arq Bras Cir Dig, 2015 Abr-Jun; 28 (2), pp: 132-135. DOI: 10.1590/S0102-67202015000200012. PMC: 4737337. PMID: 26176252 [Consulta: 23 abril 2018].
- ↑ Botta F, Giannini E, Romagnoli P, Fasoli A, et al «MELD scoring system is useful for predicting prognosis in patients with liver cirrhosis and is correlated with residual liver function: a European study» (en anglès). Gut, 2003 Gen; 52 (1), pp: 134–139. ISSN: 1468-3288. PMC: 1773509. PMID: 12477775 [Consulta: 21 març 2018].
- ↑
- ↑ Prohic D, Mesihovic R, Vanis N, Puhalovic A «Prognostic Significance of Ascites and Serum Sodium in Patients with Low Meld Scores» (en anglès). Med Arch, 2016 Feb; 70 (1), pp: 48-52. DOI: 10.5455/medarh.2016.70.48-52. PMC: 4779358. PMID: 26980932 [Consulta: 21 març 2018].
- ↑ Moraes ACO, Oliveira PC, Fonseca-Neto OCLD «The Impact of the Meld Score on Liver Transplant Allocation and Results: an Integrative Review» (en anglès). Arq Bras Cir Dig, 2017 Gen-Mar; 30 (1), pp: 65-68. DOI: 10.1590/0102-6720201700010018. PMC: 5424692. PMID: 28489174 [Consulta: 21 març 2018].
- ↑ Moore KP, Aithal GP «Guidelines on the management of ascites in cirrhosis» (en anglès). Gut, 2006 Oct; 55 (Supl 6), pp: vi1–vi12. DOI: 10.1136/gut.2006.099580. PMC: 1860002. PMID: 16966752 [Consulta: 14 abril 2018].
- ↑ Fortune B, Cardenas A «Ascites, refractory ascites and hyponatremia in cirrhosis» (en anglès). Gastroenterol Rep (Oxf), 2017 Maig; 5 (2), pp: 104-112. DOI: 10.1093/gastro/gox010. PMC: 5421465. PMID: 28533908 [Consulta: 14 abril 2018].
- ↑ Una bomba subcutània ajudarà a drenar pacients amb cirrosi El Periódico, 30 de març de 2010
- ↑ Stirnimann G, Berg T, Spahr L, Zeuzem S, et al «Treatment of refractory ascites with an automated low-flow ascites pump in patients with cirrhosis» (en anglès). Aliment Pharmacol Ther, 2017 Nov; 46 (10), pp: 981-991. DOI: 10.1111/apt.14331. PMC: 5698811. PMID: 28940225 [Consulta: 14 abril 2018].
- ↑ Péron JM, Bureau C, Vinel JP «Place du TIPS dans le traitement de l'ascite réfractaire» (en francès). Gastroenterol Clin Biol, 2007 Mar; 31 (3), pp: 341-346. ISSN: 0399-8320. PMID: 17396099 [Consulta: 30 abril 2018].
- ↑ European Association for the Study of the Liver «Guías de práctica Clínica EASL: Trasplante hepático» (en castellà). J Hepatol, 2016 Feb; 64 (2), pp: 433-485. Arxivat de l'original el 23 d’abril 2018. DOI: 10.1016/j.jhep.2015.10.006. ISSN: 1600-0641. PMID: 26597456 [Consulta: 21 abril 2018]. Arxivat 23 April 2018[Date mismatch] a Wayback Machine.
- ↑ Nicolas CT, Wang Y, Nyberg SL «Cell therapy in chronic liver disease» (en anglès). Curr Opin Gastroenterol, 2016 Maig; 32 (3), pp: 189-194. DOI: 10.1097/MOG.0000000000000262. PMC: 5553907. PMID: 26950359 [Consulta: 21 abril 2018].
- ↑ Eom YW, Kim G, Baik SK «Mesenchymal stem cell therapy for cirrhosis: Present and future perspectives» (en anglès). World J Gastroenterol, 2015 Set 28; 21 (36), pp: 10253-61. DOI: 10.3748/wjg.v21.i36.10253. PMC: 4579873. PMID: 26420953 [Consulta: 21 abril 2018].
- ↑ Wei X, Yang X, Han ZP, Qu FF, et al «Mesenchymal stem cells: a new trend for cell therapy» (en anglès). Acta Pharmacol Sin, 2013 Jun; 34 (6), pp: 747-754. DOI: 10.1038/aps.2013.50. PMC: 4002895. PMID: 23736003 [Consulta: 21 abril 2018].
- ↑ Zhang Y, Li Y, Zhang L, Li J, Zhu C «Mesenchymal stem cells: potential application for the treatment of hepatic cirrhosis» (en anglès). Stem Cell Res Ther, 2018 Mar 9; 9 (1), pp: 59. DOI: 10.1186/s13287-018-0814-4. PMC: 5845383. PMID: 29523186 [Consulta: 21 abril 2018].
- ↑ Oró Bozzini, D «Nuevos tratamientos contra la hipertensión portal en la cirrosis hepática experimental: 1. Nanopartículas de óxido de cerio y 2. Agonismo parcial del receptor V1a de la vasopressina -Tesi doctoral-» (en castellà). Departament de Ciències Fisiològiques I. Universitat de Barcelona, 2016; Oct 21, pàgs: 165 [Consulta: 8 abril 2018].
- ↑ Santos RA, Ferreira AJ «Pharmacological effects of AVE 0991, a nonpeptide angiotensin-(1-7) receptor agonist» (en anglès). Cardiovasc Drug Rev, 2006; 24 (3-4), pp: 239-246. DOI: 10.1111/j.1527-3466.2006.00239.x. ISSN: 0897-5957. PMID: 17214600 [Consulta: 29 maig 2018].
- ↑ Klein S, Herath CB, Schierwagen R, Grace J, et al «Hemodynamic Effects of the Non-Peptidic Angiotensin-(1-7) Agonist AVE0991 in Liver Cirrhosis» (en anglès). PLoS One, 2015 Set 25; 10 (9), pp: e0138732. DOI: 10.1371/journal.pone.0138732. ISSN: 4583473. PMID: 26406236 [Consulta: 29 maig 2018].
Vegeu també[modifica]
Bibliografia[modifica]
- Bataller, Ramón; Ginès, Pere. La cirrosis hepàtica. A: Libro de la salud del Hospital Clínic de Barcelona y la Fundación BBVA; Cap. 39, pp: 385-392 (en castellà). Fundación BBVA (Eds: Rodés, J; Piqué, JM; Trilla, A), 2007. ISBN 9788496515338 [Consulta: 17 març 2018].
- Tsoulfas, Georgios (Ed.). Liver Cirrhosis - Update and Current Challenges (en anglès). InTech, 2017; Jul. DOI 10.5772/66244. ISBN 9789535133100 [Consulta: 17 març 2018].
- Sharma, Bashar; John, Savio. Hepatic Cirrhosis (en anglès). StatPearls [Internet]. StatPearls Publishing LLC, 2020 Ag 10; NBK482419 (rev), pàgs: 9. PMID: 29494026 [Consulta: 18 agost 2020].
Enllaços externs[modifica]
| A Wikimedia Commons hi ha contingut multimèdia relatiu a: Cirrosi hepàtica |
- Cirrhosis Pathology Discussion Forum. 2017, Jul (anglès)
- Fisiopatologia de la cirrosis hepàtica Vildózola Gonzáles, H; 2017, Mar (castellà)
- Cirrhosis Overview - Clinical Presentation Medscape. 2018, Oct (anglès)

