Fotosíntesi
| Aquest article tracta sobre la fixació d'energia lumínica amb alliberament d'oxigen. Si cerqueu la fixació d'energia lumínica sense alliberament d'oxigen, vegeu «fotosíntesi anoxigènica». |
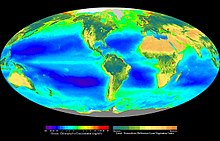
La fotosíntesi (del grec φώτο foto, 'llum', i σύνθεσις synthesis, 'composició') és un procés bioquímic que converteix el diòxid de carboni en compostos orgànics utilitzant l'energia de la llum solar.[1] La fotosíntesi es produeix en les plantes, les algues, i alguns grups de bacteris, però no en els arqueus.
Els organismes fotosintètics reben el nom de fotòtrofs; la majoria són fotoautòtrofs, és a dir, utilitzen el diòxid de carboni com a font de carboni; però no tots els organismes que utilitzen la llum són autòtrofs, car els fotoheteròtrofs (només certs bacteris) utilitzen compostos orgànics, i no diòxid de carboni, com a font de carboni.[2]
En les plantes, les algues i els cianobacteris, la fotosíntesi utilitza diòxid de carboni i aigua: allibera oxigen com a producte residual. La fotosíntesi té una importància crucial per a la vida a la Terra, car a més de mantenir el nivell normal d'oxigen a l'atmosfera, gairebé totes les formes de vida en depenen directament com a font d'energia, o indirectament com a font última de l'energia al seu aliment.[2] La quantitat d'energia capturada per la fotosíntesi és immensa, d'aproximadament 100 terawatts:[3] això és unes sis vegades l'energia consumida anualment per la civilització humana.[4] En total, els organismes fotosintètics converteixen uns 100.000 milions de tones de carboni en biomassa cada any.[5]
Tot i que la fotosíntesi es pot produir de diferents maneres en diferents espècies, alguns trets són sempre iguals. Per exemple, el procés sempre comença quan l'energia lumínica és absorbida per proteïnes anomenades centres de reacció fotosintètics, que contenen clorofil·les. En les plantes, aquestes proteïnes resideixen a l'interior d'orgànuls anomenats cloroplasts, mentre que en els bacteris es troben a la membrana plasmàtica. Una part de l'energia lumínica és recollida per les clorofil·les en forma de trifosfat d'adenosina (ATP). La resta de l'energia es fa servir per a treure electrons d'una substància com ara l'aigua. Aleshores, aquests electrons són utilitzats en les reaccions que transformen el diòxid de carboni en components orgànics. En les plantes, algues i cianobacteris, això es fa mitjançant una seqüència de reaccions anomenada cicle de Calvin, però en alguns bacteris es donen conjunts diferents de reaccions, com ara el cicle de Krebs invers en Chlorobium. Molts organismes fotosintètics tenen adaptacions que concentren o emmagatzemen el diòxid de carboni. Això permet reduir un procés malgastador anomenat fotorespiració que pot consumir part del sucre generat durant la fotosíntesi.

La fotosíntesi evolucionà d'hora en la història evolutiva de la vida, quan totes les formes de vida de la Terra eren microorganismes i l'atmosfera tenia molt més diòxid de carboni. Els primers organismes fotosintètics probablement evolucionaren fa uns 3.500 milions d'anys, i utilitzaven hidrogen o àcid sulfhídric com a font d'electrons, en lloc d'aigua.[6] Els cianobacteris aparegueren més endavant, fa uns 3.000 milions d'anys, i canviaren la Terra per sempre més quan començaren a oxigenar l'atmosfera a partir de fa uns 2.400 milions d'anys.[7] Aquesta nova atmosfera permeté l'evolució de vida complexa, com ara els protists. Finalment, fa uns 550 milions d'anys, un d'aquests protists establí una relació simbiòtica amb un cianobacteri: creà l'avantpassat de les plantes i les algues.[8] Els cloroplasts de les plantes actuals són els descendents d'aquests cianobacteris simbiòtics ancestrals.
Segons una investigació publicada el febrer de 2012 a la revista científica National Academy of Sciences sobre un tipus d'ameba anomenada Paulinella chromatophora, aquesta conté només dos compartiments fotosintètics anomenats cromatòfors, originats, com és comú, per cianobacteris endosimbiòtics, però en aquest cas representen un estadi primerenc en l'evolució d'aquest orgànul; aquesta ameba representa un model important per estudiar els processos evolutius pels quals es van desenvolupar aquests orgànuls.[9]
Visió de conjunt del procés fotosintètic
[modifica]L'energia de la fotosíntesi s'origina mitjançant l'absorció de fotons de la llum amb la participació d'un agent reductor, anomenat donador d'electrons, que en el cas de les plantes és l'aigua: allibera oxigen com a producte de rebuig. L'energia de la llum és convertida en energia química en forma d'ATP i de NADPH, que seran utilitzats en les reaccions de síntesi de molècules en els organismes fotoautòtrofs. Una característica excepcional dels organismes fotosintètics és que utilitzen aquesta energia per a fixar el diòxid de carboni en carbohidrats, principalment glucosa i altres compostos orgànics amb reaccions independents de la llum. De manera simplificada, la fotosíntesi podria ser definida com la conversió de l'energia solar en energia química, realitzada pels organismes vius.
En les plantes verdes, la reacció global de la fixació de carboni mitjançant la fotosíntesi (de vegades coneguda com a reducció del carboni) es pot representar per aquesta equació simplificada:
- n CO₂ + 2n H₂O + ATP + NADPH → (CH₂O)n + n O₂ + n H₂O,
en què n és definit de manera dependent de l'estructura del carbohidrat resultant. Els glúcids d'hexosa i de midó en són els productes principals, i per tant la reacció següent és la més utilitzada per a descriure el procés de reducció del carboni:
6 CO₂ + 12 H₂O + llum → C₆H₁₂O₆ + 6 O₂ + 6 H₂O
- Diòxid de carboni + aigua + llum → hexosa + oxigen + aigua
De manera simplificada, la fotosíntesi podria ser definida com la conversió de l'energia solar en energia química, realitzada pels organismes vius, i és la característica principal dels fotoautòtrofs, és a dir, que són capaços de sintetitzar glúcids a partir de compostos inorgànics utilitzant la llum com a font d'energia (com per exemple la llum del Sol), i no a partir de la ingestió d'altres organismes o dels seus nutrients derivats. Un fotoautòtrof, a més, utilitza CO₂ com a font de carboni. Els organismes quimioautòtrofs, en canvi, no depenen de l'energia de la llum, però sí de l'energia obtinguda d'altres compostos inorgànics.
La fotosíntesi té lloc en dues fases. En la primera fase, anomenada fase lluminosa, les reaccions dependents de la llum o reaccions fotosintètiques capturen l'energia lumínica i la utilitzen per a sintetitzar molècules altament energètiques. Més específicament, la clorofil·la, en absorbir l'energia de la llum, perd un electró que en passar per la cadena de transport electrònic produeix molècules riques en energia, com per exemple el NADPH i l'ATP. La molècula de clorofil·la recupera el seu electró a partir del trencament d'una molècula d'aigua, procés en el qual s'allibera oxigen dimolecular en forma de gas.
En la segona fase, fase fosca, les reaccions són independents de la llum i utilitzen aquestes molècules amb un alt contingut energètic per a capturar (fixar) el diòxid de carboni, CO₂, i produir els precursors de la glucosa. En la fase fosca l'enzim RuBisCO captura el CO₂ de l'atmosfera terrestre i el cicle de Calvin-Benson, el converteix en molècules orgàniques de 3 àtoms de carboni, que seran després convertides en glucosa. La fixació de carboni produeix un producte intermediari, que és convertit en els carbohidrats d'hexosa finals. Aquests carbohidrats són utilitzats per a formar altres productes orgànics, com la cel·lulosa, els precursors de la biosíntesi dels lípids i dels aminoàcids o combustible en la respiració cel·lular.
Aquests processos no sols es produeixen en les plantes, també en els animals quan l'energia de les plantes passa a la cadena alimentària. Els organismes que depenen dels organismes fotosintètics i quimiosintètics són anomenats heteròtrofs, entre els quals hi ha els humans. En general, la respiració és el procés contrari a la fotosíntesi: la glucosa i altres compostos són oxidats per produir diòxid de carboni, aigua i energia química. Tanmateix, aquests dos processos tenen lloc amb reaccions i compartiments cel·lulars diferents.
Orgànuls fotosintètics
[modifica]
1. membrana externa
2. espai intermembranal
3. membrana interna (1+2+3: embolcall)
4. estroma (fluid aquós)
5. lumen del tilacoide (interior del tilacoide)
6. membrana del tilacoide
7. granum (pila de tilacoides)
8. tilacoide (lamel·la)
9. midó
10. ribosoma
11. ADN plastídic
12. plastoglòbul (gota lipídica)
En els bacteris fotosintètics, les proteïnes que recullen llum per a la fotosíntesi es troben incloses en la membrana cel·lular que és la configuració més senzilla en què es poden disposar.[10] Tot i això, la membrana pot plegar-se formant capes cilíndriques anomenades tilacoides,[11] o agrupades en vesícules amb el nom de membranes intracitoplasmàtiques.[12] Aquestes estructures poden arribar a omplir la major part de l'interior de la cèl·lula, cosa que permet que l'àrea de la membrana cel·lular sigui molt més gran i per tant augmenti la capacitat d'absorció de llum per part del bacteri.[11]
En les plantes i les algues, la fotosíntesi es realitza en uns orgànuls anomenats cloroplasts. Una cèl·lula vegetal típica conté entre 10 i 100 cloroplastidis. El cloroplast està delimitat per una membrana doble, formada per una membrana fosfolipídica externa i una d'interna amb un espai intermembranal entre si. Dins d'aquesta membrana es troba un fluid aquós anomenat estroma. L'estroma conté piles de tilacoides anomenats grana (singular granum), que és on té lloc la fotosíntesi. Els tilacoides són discs plans formats per membranes que envolten un espai intern, el lumen. La fotosíntesi té lloc precisament a les membranes dels tilacoides, que contenen proteïnes integrals i perifèriques de membrana que componen els fotosistemes i que inclouen els pigments que absorbeixen la llum.
Les plantes usen la clorofil·la com a principal pigment per a absorbir la llum, el color de la qual dona la verdor a aquests éssers vius. A més de la clorofil·la, les plantes també utilitzen altres pigments com els carotens i les xantofil·les.[13] Les algues presenten més pigments que varien segons els tipus i que els donen la seva vària coloració: les algues verdes contenen clorofil·la, ficocianina, carotens i xantofil·les; les algues vermelles contenen ficoeritrina i les marrons i les diatomees fucoxantina. Aquests pigments no es troben lliures per la membrana sinó inclosos en unes proteïnes especials anomenades proteïnes antena o complexos captadors de llum.
Malgrat que totes les parts verdes de les plantes contenen cloroplasts és a les fulles on es recull la gran majoria de l'energia. Les cèl·lules de l'interior de les fulles formen el mesofil·le, un teixit que pot arribar a contenir entre 450.000 i 800.000 cloroplastidis per mil·límetre quadrat. La superfície de les fulles estan cobertes de cera resistent a l'aigua, i de la cutícula, que les protegeix d'una evaporació excessiva. Aquesta capa protectora impedeix l'entrada de la radiació ultraviolada i de la llum blava, cosa que impedeix un escalfament excessiu. D'altra banda, l'epidermis foliar és transparent a la resta de la llum visible i permet la fotosíntesi dins del mesofil·le.
Fase lluminosa
[modifica]
En les reaccions dependents de la llum, una molècula de clorofil·la absorbeix un fotó i perd un electró. Aquest electró és transferit a una forma modificada de la clorofil·la, la feofitina, que al seu torn el passa a una molècula de quinona. Aquest és l'inici del corrent d'electrons de la cadena de transport d'electrons, que duu finalment a la reducció de NADP en NADPH. A més a més, aquest flux crea un gradient de protons a través de la membrana del cloroplast; la dissipació d'aquest gradient és usada per l'ATP sintasa per a sintetitzar ATP. La molècula de clorofil·la recupera l'electró perdut mitjançant la fotòlisi d'una molècula d'aigua i allibera alhora una molècula de dioxigen (O₂). Així doncs, l'equació per a les reaccions de la fase lluminosa sota condicions de flux no cíclic en les plantes verdes és:[14]
- 2 H₂O + 2 NADP+ + 3 ADP + 3 Pi + llum → 2 NADPH + 2 H+ + 3 ATP + O₂
No totes les longituds d'ona de la llum poden ser emprades per a la fotosíntesi. L'espectre de llum que es pot usar depèn dels pigments accessoris presents. Per exemple, en les plantes verdes, l'espectre útil s'assembla a l'espectre d'absorció de la clorofil·la i els carotenoids amb pics en les longituds d'ona de llum violada-blava i roja. En les algues vermelles, l'espectre efectiu se sobreposa a l'espectre d'absorció de les ficobilines de la llum blau-verdosa, cosa que els permet viure en profunditats on la llum de major longitud d'ona, i que aprofiten les plantes verdes, no hi arriba. La part de l'espectre electromagnètic que no s'absorbeix és el que dona als organismes fotosintètics el seu color (per exemple, les plantes verdes, les algues vermelles, els bacteris porpra) i és la menys efectiva per a la fotosíntesi en els respectius organismes.
L'esquema Z
[modifica]En les plantes, la fase lluminosa té lloc a la membrana del tilacoide dels cloroplasts i usa l'energia lumínica per a sintetitzar ATP i NADPH. Aquesta reacció dependent de llum pot tenir dues formes: cíclica o acíclica. En la reacció acíclica, la clorofil·la i altres pigments accessoris del complex antena del fotosistema II capturen els fotons. Quan una molècula de clorofil·la dins del centre reactiu del fotosistema II obté suficient energia d'excitació dels pigments antena accessoris, transfereix un electró a la feofitina, la principal molècula acceptora d'electrons mitjançant el procés anomenat separació de càrrega fotoinduïda. Aquests electrons són després transportats a través de la cadena de transport d'electrons, el que s'anomena esquema Z i que es mostra en el diagrama. Aquest transport genera un potencial quimioosmòtic a través de la membrana. L'ATP sintasa utilitza aquest potencial per a produir ATP en la fotofosforilació, mentre que la reacció d'oxidoreducció final de l'esquema Z produeix NADPH. Perquè aquesta producció de NADPH s'esdevingui, l'electró ha d'entrar en la molècula de clorofil·la del fotosistema I. Allà, és excitat de nou per la llum que ha absorbit el fotosistema. Aleshores va passant per diferents acceptors d'electrons amb la consegüent disminució energètica; finalment aquest electró arriba a la NADP+ reductasa que l'utilitza per a reduir el coenzim NADP, que s'usarà en la fase fosca de la fotosíntesi. Aquest pas des del fotosistema II fins a la producció de NADPH s'anomena fase acíclica. Si la longitud d'ona és llarga també es pot produir la forma cíclica o fotofosforilació anoxigènica. En aquest cas, l'electró dins el fotosistema I s'excita amb l'energia recollida i passa la ferrodoxina, però aleshores entra en la cadena de transport d'electrons al nivell del complex de citocrom b₆f, i passant per la plastocianina, de nou al fotosistema I; en aquest cas només es crea potencial de membrana per acumulació de protons dins el lumen del tilacoide i per tant ATP, però no pas NADPH.

Fotòlisi de l'aigua
[modifica]L'NADPH és el principal agent reductor en els cloroplasts i proporciona electrons energètics a altres reaccions. En sintetitzar aquesta molècula, la clorofil·la s'oxida, és a dir, li manquen electrons que han de ser obtinguts d'algun altre agent reductor. En el cas del fotosistema I els electrons excitats que perd la clorofil·la són recuperats a partir de la cadena de transport d'electrons per la plastocianina. Però en el cas del fotosistema II que inclou el començament de l'esquema Z cal una font externa d'electrons per a reduir la clorofil·la a oxidada. Aquesta font d'electrons és l'aigua, en el cas de les plantes verdes i els cianobacteris. El fotosistema II oxida dues molècules d'aigua mitjançant quatre reaccions de separació de càrrega successives i produeix una molècula d'oxigen diatòmic i quatre ions d'hidrogen. L'electró obtingut en cada etapa es transfereix a un residu de tirosina que redueix la clorofil·la a oxidada (anomenada P680). Aquesta oxidació de l'aigua és catalitzada per una estructura activa d'oxidació-reducció que conté quatre ions de manganès i un ió de calci. Aquest complex uneix les dues molècules d'aigua i emmagatzema els quatre equivalents d'oxidació necessaris perquè es produeixi aquesta reacció d'oxidació de l'aigua. El fotosistema II és l'únic enzim conegut capaç de realitzar aquesta oxidació. Els ions d'hidrogen produïts contribueixen al potencial quimiosmòtic de membrana que s'utilitza per a la síntesi d'ATP. L'oxigen és l'altre producte, i en aquest cas de les reaccions de la fase lluminosa, de rebuig. Tot i això, l'oxigen diatòmic és vital per a la majoria d'organismes de la Terra, incloent-hi els organismes fotosintètics, ja que el necessiten per a la respiració cel·lular.[15][16]
Fase fosca
[modifica]Cicle de Calvin
[modifica]En les reaccions independents de llum o de la fase fosca, l'enzim RuBisCO captura CO₂ de l'atmosfera i utilitza l'NADPH format en la fase lluminosa i ATP per a sintetitzar sucres de tres carbonis, que més tard es combinaran per formar sacarosa i midó. Aquest procés s'anomena cicle de Calvin-Benson i la seva equació global en les plantes verdes és la següent:[14]:128
- 3 CO₂ + 9 ATP + 6 NADPH + 6 H+ → C₃H₆O₃-phosphate + 9 ADP + 8 Pi + 6 NADP+ + 3 H₂O
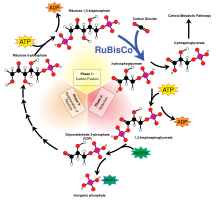
Així doncs, la fixació de carboni produeix productes intermediaris que després es transformaran en els carbohidrats finals. Els esquelets de carboni produïts per la fotosíntesi poden ser usats per a formar diversos compostos orgànics, de tipus estructural com ara la cel·lulosa, poden ser precursors de la síntesi de lípids i aminoàcid o també ser directament usats en la respiració cel·lular com a combustible, bé dins les mateixes plantes o bé en els animals quan hi arriben a través de la cadena alimentària.
En la fixació o reducció del diòxid de carboni, una molècula de CO₂ es combina amb un sucre de cinc carbonis, la ribulosa 1,5-bisfosfat (RuBP) per a produir dues molècules d'àcid 3-fosfoglicèric (3GP), de tres carbonis cadascuna, també anomenat 3-fosfoglicerat. El 3GP en presència d'ATP i NADPH que han estat sintetitzats durant la fase lluminosa, és reduït a gliceraldehid 3-fosfat (o 3-fosfogliceraldehid). La majoria d'aquestes molècules, 5 de 6 del gliceraldehid 3-fosfat produït són usades per tornar a formar la RuBP per tal que el procés pugui continuar. Les molècules de triosa (sucres de tres carbonis) que no s'han "reciclat" es condensen normalment per a formar una hexosa fosfat, les hexoses finalment s'empraran per sintetitzar sacarosa, midó i cel·lulosa. Com es mencionava més amunt, aquestes trioses poden ser usades per altres reaccions metabòliques de síntesi d'aminoàcids i lípids.
Mecanismes de concentració de diòxid de carboni
[modifica]A terra
[modifica]
En condicions ambientals caloroses i seques, les plantes tanquen els seus estromes per evitar la pèrdua d'aigua. Aleshores, la concentració de diòxid de carboni baixa mentre que la d'oxigen gas augmenta a les fulles (no a les tiges) provocant que augmenti la fotorespiració per part de l'activitat oxigenasa de la RuBisCo. A la vegada, la fixació de carboni disminueix. Algunes plantes han evolucionat per tal d'augmentar la concentració de diòxid de carboni a les fulles sota aquestes condicions.
La fixació de carboni per la via C₄ té lloc al mesofil·le i crea una molècula de 4 carbonis, l'àcid oxaloacètic a partir de fosfoenolpiruvat (PEP) que en té tres i una de diòxid de carboni gràcies a l'acció de l'enzim fosfoenolpiruvat carboxilasa. L'àcid oxaloacètic o el malat sintetitzat en aquest procés és transportat a unes cèl·lules especialitzades anomenades cèl·lules de la beina vascular on es troben l'enzim RuBisCO i els altres que formen part del cicle de Calvin. Allà el CO₂ s'allibera dels àcids de quatre carbonis per decarboxilació i es fixa a una molècula de 3-fosfoglicerat per la RuBisCO. La separació física de la RuBisCO del lloc on ocorren les reaccions de la fase lluminosa i per tant de la formació d'oxigen redueix la fotorespiració i augmenta la fixació de CO₂ i per tant la capacitat fotosintètica de la fulla.[17] Les plantes C₄ produeixen més sucres que les C₃ en condicions d'il·luminació i temperatura elevades. Molts cultius d'importància són plantes C₄ inclosos la dacsa, el sorgo, la canya de sucre i el mill. les plantes que no usen la fosfoenolpiruvat carboxilasa s'anomenen plantes C₃ perquè la reacció de carboxilació principal catalitzada per la RuBisCO produeix les molècules de tres carbonis 3-fosfoglicerat directament dins del Cicle de Calvin-Benson. La majoria, el 90%, de les plantes són C₃, mentre que només un 3% són C₄.[18]
Els xeròfits, com els cactus i la majoria de plantes suculentes, també utilitzen la PEP carboxilasa per a capturar diòxid de carboni en un procés anomenat metabolisme àcid de les crassulàcies (MAC). A diferència del metabolisme C4, en el qual se separa físicament la fixació del diòxid de carboni del cicle de Calvin, en el MAC aquests dos processos se separen de forma temporal. Les plantes amb MAC tenen una anatomia foliar diferent de les plantes C3 i fixen el CO₂ de nit, quan els seus estomes estan oberts. Aquestes plantes emmagatzemen el CO₂ principalment en forma d'àcid màlic mitjançant la carboxilació del fosfoenolpiruvat que produeix oxalacetat i que finalment és reduït a malat. Durant el dia, la descarboxilació del malat allibera CO₂ dins les fulles permetent la fixació del carboni en forma de 3-fosfoglicerat per part de la RuBisCO. Hi ha unes setze mil plantes que usen el metabolisme MAC.[19]
A l'aigua
[modifica]Els cianobacteris tenen carboxisomes, que augmenten la concentració de CO₂ al voltant de la RuBisCO per a aconseguir una velocitat de fotosíntesi superior. L'enzim anhidrasa carbònica i que es troba dins dels carboxisomes allibera CO₂ a partir dels ions hidrogencarbonat (HCO₃–) dissolts dins la cèl·lula. Abans que el CO₂ es difongui és absorbit ràpidament per la RuBisCO, que també es troba concentrada dins els carboxisomes. Els ions HCO₃– se sintetitzen a partir de CO₂ a l'exterior de la cèl·lula per una altra anhidrasa carbònica i són bombejats a l'interior per una proteïna de membrana. Com els ions tenen càrrega, no poden travessar la membrana i sense l'ajuda de l'anhidrasa carbònica la seva conversió en CO₂ és molt lenta. Així, els ions HCO₃– s'acumulen dins de la cèl·lula i, per difusió, entren als carboxisomes.[20] Els pirenoides en algues i antocerotòpsids també concentren CO₂ al voltant de la RuBisCO.[21]
Evolució
[modifica]
Es creu que els primers sistemes fotosintètics, com ara els dels bacteris verds i porpres del sofre, així com els bacteris verds i porpres no del sofre, eren anoxigènics, utilitzant diferents molècules com a donadors d'electrons. Es creu que els bacteris verds i porpres del sofre utilitzaven hidrogen i sofre com a donadors d'electrons. Els bacteris verds no del sofre utilitzaven diversos aminoàcids i altres àcids orgànics. Els bacteris porpres no del sofre utilitzaven una sèrie de molècules orgàniques no específiques. L'ús d'aquestes molècules és consistent amb les proves geològiques que l'atmosfera estava molt reduïda en aquell temps.
Els fòssils del que es creu que eren organismes fotosintètics filamentosos han estat datats a fa uns 3.400 milions d'anys.[22]
La font principal d'oxigen de l'atmosfera és la fotosíntesi de l'oxigen, i a vegades hom es refereix a la seva primera aparició amb el nom de catàstrofe de l'oxigen. Les proves geològiques suggereixen que la fotosíntesi oxigènica, com la dels cianobacteris, esdevingué important durant el Paleoproterozoic, fa uns 2.000 milions d'anys. La fotosíntesi moderna de les plantes i la majoria de procariotes fotosintètics és oxigènica. La fotosíntesi oxigènica utilitza l'aigua com a donador d'electrons que és oxidat en dioxigen molecular (O₂) al centre de reacció fotosintètic.
La simbiosi i l'origen dels cloroplasts
[modifica]Diversos grups d'animals han format relacions simbiòtiques amb algues fotosintètiques. Són especialment comunes en els coralls, les esponges i les anemones de mar, possiblement pel fet que aquests animals tenen un pla corporal particularment simple i una àrea de superfície gran en comparació amb el seu volum.[23] A més, alguns mol·luscs marins, com Elysia viridis i Elysia chlorotica, també tenen una relació simbiòtica amb cloroplasts que capturen de les algues de la seva dieta i que emmagatzemen dins el cos. Això permet als mol·luscs sobreviure només amb fotosíntesi durant mesos.[24][25] Alguns dels gens del nucli cel·lular vegetal fins i tot han estat transferits als llimacs, de manera que els cloroplasts puguin ser proveïts amb les proteïnes que necessiten per sobreviure.[26]
Una forma encara més estreta de simbiosi podria explicar l'origen dels cloroplasts. Els cloroplasts presenten moltes semblances amb els bacteris fotosintètics, incloent-hi un cromosoma circular, ribosomes de tipus procariota, i proteïnes similars al centre de reacció fotosintètic.[27][28] La teoria endosimbiòtica suggereix que els bacteris fotosintètics foren adquirits (mitjançant endocitosi) per cèl·lules eucariotes primitives per formar les primeres cèl·lules vegetals. Per consegüent, els cloroplasts podrien ser bacteris fotosintètics que s'adaptaren a la vida dins de cèl·lules vegetals. Com els mitocondris, els cloroplasts encara tenen el seu propi ADN, separat de l'ADN nuclear de les seves cèl·lules hoste vegetals, i els gens d'aquest ADN dels cloroplasts s'assemblen als dels cianobacteris.[29] L'ADN dels cloroplasts codifica proteïnes redox com ara centres de reacció fotosintètics. La hipòtesi CoRR proposa que aquesta Col·locació és necessària per a la Regulació Redox.
Els cianobacteris i l'evolució de la fotosíntesi
[modifica]La capacitat bioquímica d'utilitzar aigua com a font d'electrons en la fotosíntesi només ha sorgit un cop durant l'evolució, en l'antecessor comú de tots els cianobacteris actuals. El registre geològic indica que aquest esdeveniment tan important va ocórrer força aviat en la història terrestre, com a mínim fa 2450-2320 milions d'anys i s'especula que podria haver passat fins i tot abans.[30] Les proves geobiològiques disponibles de roques sedimentàries de l'Arqueà (>2500 Ma) indiquen que la vida ja existia fa 3500 Ma, però la pregunta sobre quan va aparèixer la fotosíntesi oxigènica encara es desconeix. Fa uns 2000 Ma, la paleontologia mostra que els cianobacteris ja formaven una biota diversa. Aquests organismes van continuar sent els productors primaris durant tot l'eó Proterozoic (2500–543 Ma), en part perquè l'estat redox dels oceans afavorien els fotoautòtrofs capaços de fixar nitrogen.[31] Les algues verdes van afegir-se als cianobacteris com a principals productors en les plataformes continentals cap a finals del Proterozoic, però no va ser fins al Mesozoic (251–65 Ma) que amb l'evolució dels dinoflagel·lats, els coccolitofòrids i les diatomees, que la producció primària en les aigües marines continentals va prendre la forma en què es troba avui dia. Els cianobacteris continuen sent crítics com a productors primaris de l'ecosistema marí en els girs oceànics com a fixadors de nitrogen, i en la seva forma endosimbiòntica com a plastidis de les algues marines.[32]
El 2010, un estudi de la Universitat de Tel-Aviv va descobrir que la vespa oriental (Vespa orientalis) transforma la llum del sol en corrent elèctric mitjançant el pigment xantopterina. Aquest treball és la primera prova científica que mostra un animal que aprofita l'energia del sol mitjançant captació amb pigments tot i que sembla que no fixa carboni ni produeix oxigen com la fotosíntesi oxigènica.[33]
Descobriment
[modifica]
Tot i que alguns dels passos de la fotosíntesi encara no estan compresos del tot, l'equació fotosintètica general ha estat coneguda des de la dècada del 1800.
Jan van Helmont començà a investigar el procés a mitjans de segle xvii, quan mesurà amb cura la massa del sòl utilitzat per una planta i la massa de la planta a mesura que creixia. En remarcar que la massa del sòl canviava molt poc, hipotetitzà que la massa de la planta en creixement devia venir de l'aigua, l'única substància que havia afegit dins el test de la planta. La seva hipòtesi era parcialment correcta—gran part de la massa afegida també ve del diòxid de carboni, a més de l'aigua. Tanmateix, això fou un indici vers la idea que gran part de la biomassa d'una planta ve dels productes de la fotosíntesi, no del sòl en si.
Joseph Priestley, químic i pastor religiós, descobrí que quan aïllava un volum d'aire a sota una gerra invertida, i hi cremava una espelma, l'espelma s'extingia molt ràpidament, molt abans que se li acabés la cera. Més tard descobrí que un ratolí també podia "danyar" l'aire. Més endavant demostrà que l'aire que havia estat "danyat" per l'espelma i el ratolí podia ser restaurat per una planta.
El 1778, Jan Ingenhousz, metge de la cort de l'emperadriu austríaca, repetí els experiments de Priestley. Descobrí que era la influència de la llum solar sobre la planta que li permetia rescatar un ratolí en qüestió d'hores.
El 1796, Jean Senebier, un pastor religiós, botànic i naturalista suís, demostrà que les plantes verdes consumeixen diòxid de carboni i alliberen oxigen sota la influència de la llum. Poc després, Nicolas-Théodore de Saussure demostrà que l'augment en massa de la planta a mesura que creix no podia ser únicament deguda a l'absorció de CO₂, sinó també a la incorporació d'aigua. D'aquesta manera es trobà la reacció bàsica per la qual la fotosíntesi produeix aliments (com ara la glucosa).
Cornelis Van Niel feu descobriments clau per explicar la química de la fotosíntesi. Estudiant bacteris porpres del sofre i bacteris verds, fou el primer científic a demostrar que la fotosíntesi és una reacció redox dependent de la llum, en què l'hidrogen redueix el diòxid de carboni.
Robert Emerson descobrí dues reaccions lumíniques quan estudiava la productivitat de les plantes amb diferents longituds d'ona de la llum. Amb només llum vermella, les reaccions lumíniques quedaven suprimides. Quan es combinava el blau amb el vermell, la producció era molt més substancial. Per tant, hi havia dos fotosistemes, un que absorbia longituds d'ona de fins a 600 nm, i l'altre fins a 700. El primer és conegut com a PSII, i l'últim com a PSI. El PSI només conté clorofil·la a, mentre que el PSII conté principalment clorofil·la a amb la majoria de la clorofil·la b disponible, entre altres pigments.[34]
El 1937 i el 1939, Robert Hill dugué a terme més experiments per demostrar que l'oxigen generat durant la fotosíntesi de les plantes verdes provenia de l'aigua. Demostrà que els cloroplasts aïllats alliberen oxigen en presència d'agents reductors no naturals com ara ferro, oxalat, ferricianur o benzoquinona després de ser exposats a la llum. La reacció de Hill és la següent:
- 2 H₂O + 2 A + (llum, cloroplasts) → 2 AH₂ + O₂
on A és l'acceptor d'electrons. Per tant, en presència de llum l'acceptor d'electrons és reduït i es produeix oxigen elemental. La cyt b₆, actualment coneguda com a plastoquinona, és un dels acceptors d'electrons.
Samuel Ruben i Martin Kamen utilitzaren isòtops radioactius per determinar que l'oxigen alliberat en la fotosíntesi provenia de l'aigua.
Melvin Calvin i Andrew Benson, juntament amb James Bassham, dilucidaren la ruta de l'assimilació del carboni (el cicle fotosintètic de reducció del carboni) en les plantes. El cicle de reducció del carboni és conegut com a cicle de Calvin, un nom que ignora inapropiadament la contribució de Bassham i Benson. Molts científics es refereixen al cicle com el cicle de Calvin-Benson, de Benson-Calvin, i alguns fins i tot l'anomenen cicle de Calvin-Benson-Bassham (CBB).
Un científic guardonat amb el Premi Nobel, Rudolph Arthur Marcus, aconseguí esbrinar la funció i la rellevància de la cadena de transport d'electrons.
Fotosíntesi artificial
[modifica]Investigadors de tot el món, incloent els Estats Units, el Japó i la Unió Europea han estat treballant des de la dècada de 1980 en refinar una forma artificial de fotosíntesi. Els resultats han estat variables però fins a l'any 2012 no es va aconseguir crear un sistema prou ràpid de catalitzador per oxidar l'aigua. La velocitat de la fotosíntesi natural ocorre a 100 a 400 cicles per segon. L'any 2012 els investigadors del Reial Institut de Tecnologia d'Estocolm (KTH), creadors d'aquest nou catalitzador, van aconseguir que la reacció de la fotosíntesi fos de 300 cicles per segon. Els científics d'aquest institut suec creuen que el termini d'uns 10 anys la fotosíntesi podria ser una font d'energia renovable molt important (a base de produir hidrogen en llocs molt assolellats com potser el Sàhara).[35]
Vegeu també
[modifica]Referències
[modifica]- ↑ Smith, A. L.. Oxford dictionary of biochemistry and biology. Oxford [Oxfor]: Oxford University Press, 1997, p. 508. ISBN 0-19-854768-4. «Photosynthesis - the synthesis by organisms of organic chemical esp. carbohydrates, from carbon dioxide using energy obtained from light rather than the oxidation of chemical compounds.»
- ↑ 2,0 2,1 D. A. Bryant & N.-U. Frigaard «Prokaryotic photosynthesis and phototrophy illuminated». Trends Microbiol, 14, 11, Novembre 2006, pàg. 488. DOI: 10.1016/j.tim.2006.09.001.
- ↑ Nealson K. H., Conrad P. G. «Life: past, present and future». Philos. Trans. R. Soc. Lond., B, Biol. Sci., 354, 1392, desembre 1999, pàg. 1923–39. DOI: 10.1098/rstb.1999.0532. PMC: 1692713. PMID: 10670014.
- ↑ «World Consumption of Primary Energy by Energy Type and Selected Country Groups, 1980-2004» (XLS). Energy Information Administration, 31-07-2006.
- ↑ Field C. B., Behrenfeld M. J., Randerson J. T., Falkowski P. «Primary production of the biosphere: integrating terrestrial and oceanic components». Science, 281, 5374, Juliol 1998, pàg. 237–40. DOI: 10.1126/science.281.5374.237. PMID: 9657713.
- ↑ Olson JM «Photosynthesis in the Archean era». Photosyn. Res., 88, 2, Maig 2006, pàg. 109–17. DOI: 10.1007/s11120-006-9040-5. PMID: 16453059.
- ↑ Buick R «When did oxygenic photosynthesis evolve?». Philos. Trans. R. Soc. Lond., B, Biol. Sci., 363, 1504, Agost 2008, pàg. 2731–43. DOI: 10.1098/rstb.2008.0041. PMID: 18468984.
- ↑ Gould SB, Waller RF, McFadden GI «Plastid evolution». Annu Rev Plant Biol, 59, 2008, pàg. 491–517. DOI: 10.1146/annurev.arplant.59.032607.092915. PMID: 18315522.
- ↑ Science Daily
- ↑ Tavano CL, Donohue TJ «Development of the bacterial photosynthetic apparatus». Curr. Opin. Microbiol., 9, 6, December 2006, pàg. 625–31. DOI: 10.1016/j.mib.2006.10.005. PMC: 2765710. PMID: 17055774.
- ↑ 11,0 11,1 Mullineaux CW «The thylakoid membranes of cyanobacteria: structure, dynamics and function». Australian Journal of Plant Physiology, 26, 7, 1999, pàg. 671–677. DOI: 10.1071/PP99027.
- ↑ Sener MK, Olsen JD, Hunter CN, Schulten K «Atomic-level structural and functional model of a bacterial photosynthetic membrane vesicle». Proc. Natl. Acad. Sci. U.S.A., 104, 40, October 2007, pàg. 15723–8. Bibcode: 2007PNAS..10415723S. DOI: 10.1073/pnas.0706861104. PMC: 2000399. PMID: 17895378.
- ↑ Campbell NA, Williamson B, Heyden RJ. Biology Exploring Life. Upper Saddle River, NJ: Pearson Prentice Hall, 2006. ISBN 0-13-250882-6.
- ↑ 14,0 14,1 Raven PH, Evert RF, Eichhorn SE. Biology of Plants,. 7a ed.. Nova York: W.H. Freeman and Company Publishers, 2005, p. 124–127. ISBN 0-7167-1007-2.
- ↑ «Yachandra Group Home page». Arxivat de l'original el 2008-10-25. [Consulta: 7 desembre 2012].
- ↑ Pushkar Y, Yano J, Sauer K, Boussac A, Yachandra VK «Structural changes in the Mn4Ca cluster and the mechanism of photosynthetic water splitting». Proc. Natl. Acad. Sci. U.S.A., 105, 6, February 2008, pàg. 1879–84. Bibcode: 2008PNAS..105.1879P. DOI: 10.1073/pnas.0707092105. PMC: 2542863. PMID: 18250316.
- ↑ L. Taiz, E. Zeiger. Plant Physiology. 4a ed.. Sinauer Associates, 2006. ISBN 978-0-87893-856-8.
- ↑ Monson RK, Sage RF. «16». A: C₄ plant biology. Boston: Academic Press, 1999, p. 551–580. ISBN 0-12-614440-0.
- ↑ Dodd AN, Borland AM, Haslam RP, Griffiths H, Maxwell K «Crassulacean acid metabolism: plastic, fantastic». J. Exp. Bot., 53, 369, April 2002, pàg. 569–80. DOI: 10.1093/jexbot/53.369.569. PMID: 11886877.
- ↑ Badger, M. R.; Price, GD «CO₂ concentrating mechanisms in cyanobacteria: molecular components, their diversity and evolution». Journal of Experimental Botany, 54, 383, 2003, pàg. 609–22. DOI: 10.1093/jxb/erg076. PMID: 12554704.
- ↑ Badger MR, Andrews JT, Whitney SM, Ludwig M, Yellowlees DC, Leggat W, Price GD «The diversity and coevolution of Rubisco, plastids, pyrenoids, and chloroplast-based CO₂-concentrating mechanisms in algae». Canadian Journal of Botany, 76, 6, 1998, pàg. 1052–1071. DOI: 10.1139/b98-074. ISSN: 1480-3305 0008-4026, 1480-3305.
- ↑ New Scientist, 19 d'agost del 2006
- ↑ Venn AA, Loram JE, Douglas AE «Photosynthetic symbioses in animals». J. Exp. Bot., 59, 5, 2008, pàg. 1069–80. DOI: 10.1093/jxb/erm328. PMID: 18267943.
- ↑ Rumpho ME, Summer EJ, Manhart JR «Solar-powered sea slugs. Mollusc/algal chloroplast symbiosis». Plant Physiol., 123, 1, maig 2000, pàg. 29–38. DOI: 10.1104/p.123.1.29. PMC: 1539252. PMID: 10806222.
- ↑ Muscatine L, Greene RW «Chloroplasts and algae as symbionts in molluscs». Int. Rev. Cytol., 36, 1973, pàg. 137–69. DOI: 10.1016/S0074-7696(08)60217-X. PMID: 4587388.
- ↑ Rumpho ME, Worful JM, Lee J, et al. «From the Cover: Horizontal gene transfer of the algal nuclear gene psbO to the photosynthetic sea slug Elysia chlorotica». Proc. Natl. Acad. Sci. U.S.A., 105, 46, Novembre 2008, pàg. 17867–17871. DOI: 10.1073/pnas.0804968105. PMID: 19004808.
- ↑ Douglas SE «Plastid evolution: origins, diversity, trends». Curr. Opin. Genet. Dev., 8, 6, Desembre 1998, pàg. 655–61. DOI: 10.1016/S0959-437X(98)80033-6. PMID: 9914199.
- ↑ Reyes-Prieto A, Weber AP, Bhattacharya D «The origin and establishment of the plastid in algae and plants». Annu. Rev. Genet., 41, 2007, pàg. 147–68. DOI: 10.1146/annurev.genet.41.110306.130134. PMID: 17600460.
- ↑ Raven JA, Allen JF «Genomics and chloroplast evolution: what did cyanobacteria do for plants?». Genome Biol., 4, 3, 2003, pàg. 209. DOI: 10.1186/gb-2003-4-3-209. PMC: 153454. PMID: 12620099.[Enllaç no actiu]
- ↑ «Cyanobacteria: Fossil Record». Ucmp.berkeley.edu. [Consulta: 26 agost 2010].
- ↑ Enrique Flores AH. The Cyanobacteria: Molecular Biology, Genomics and Evolution. Horizon, 2008, p. 3. ISBN 1904455158.
- ↑ Herrero A, Flores E. The Cyanobacteria: Molecular Biology, Genomics and Evolution. Caister Academic Press, 2008. ISBN 978-1-904455-15-8.
- ↑ Plotkin, M.; Hod, I.; Zaban, A.; Boden, S. A.; Bagnall, D. M.; Galushko, D.; Bergman, D. J. «Solar energy harvesting in the epicuticle of the oriental hornet (Vespa orientalis)» (en anglès). Naturwissenschaften, 97, 12, 2010, pàg. 1067–1076. DOI: 10.1007/s00114-010-0728-1. PMID: 21052618.
- ↑ ed. and technical staff: Mark D. Licker .... McGraw Hill Encyclopedia of Science & Technology (Mcgraw Hill Encyclopedia of Science and Technology). McGraw-Hill Professional, 2007, p. vol 13 p. 470. ISBN 0-07-144143-3.
- ↑ Science daily
Bibliografia
[modifica]- Isaac Asimov. Photosynthesis. Nova York, Londres: Basic Books, Inc., 1968. ISBN 0-465-05703-9.
- Bidlack JE; Stern KR, Jansky S. Introductory plant biology. Nova York: McGraw-Hill, 2003. ISBN 0-07-290941-2.
- Blankenship RE. Molecular Mechanisms of Photosynthesis. 2a ed.. John Wiley & Sons Inc, 2008. ISBN 0-470-71451-4.
- Govindjee. Bioenergetics of photosynthesis. Boston: Academic Press, 1975. ISBN 0-12-294350-3.
- Govindjee Beatty JT, Gest H, Allen JF. Discoveries in Photosynthesis. 20. Berlín: Springer, 2006 (Advances in Photosynthesis and Respiration). ISBN 1-4020-3323-0.
- Gregory R. L.. Biochemistry of photosynthesis. Nova York: Wiley-Interscience, 1971. ISBN 0-471-32675-5.
- Rabinowitch E, Govindjee. Photosynthesis. Londres: J. Wiley, 1969. ISBN 0-471-70424-5.
- Reece, J, Campbell, N. Biology. San Francisco: Pearson, Benjamin Cummings, 2005. ISBN 0-8053-7146-X.
Enllaços externs
[modifica]- Breu explicació del procés i algunes activitats de nivell Batxillerat en català (unitat didàctica allotjada a l'antiga Xtec.cat, ara recuperat al Wayback Machine)
- Col·lecció de pàgines sobre la fotosíntesi per a tots els nivells d'un expert conegut (Govindjee) (anglès)
- «The Photosynthetic Process» (en anglès). John Whitmarsh, 2010. [Consulta: 21 maig 2012].
- «Who Discovered Photosynthesis?. Famous Historic Experiments» (en anglès). Julian Rubin, 2011. [Consulta: 21 maig 2012].

