Metabolisme: diferència entre les revisions
| Línia 64: | Línia 64: | ||
Els abundants elements inorgànics actuen com a [[electrolit]]s [[ió|iònics]]. Els ions més importants són el [[sodi]], el [[potassi]], el [[calci]], el [[magnesi]], el [[clor]], el [[fòsfor]] i l'ió orgànic [[bicarbonat]]. El manteniment de [[gradient iònic|gradients]] precisos a través de les [[membrana cel·lular|membranes cel·lulars]] manté la [[pressió osmòtica]] i el [[pH]].<ref>{{cite journal |author=Sychrová H |title=Yeast as a model organism to study transport and homeostasis of alkali metal cations |url=http://www.biomed.cas.cz/physiolres/pdf/53%20Suppl%201/53_S91.pdf |journal=Physiol Res |volume=53 Suppl 1 |issue= |pages=S91–8 |year=2004 |pmid=15119939}}</ref> Els ions també són essencials pels [[nervi]]s i els [[múscul]]s, car els [[potencial d'acció|potencials d'acció]] en aquests teixits es produeixen per l'intercanvi d'electrolits entre el [[fluid extracel·lular]] i el [[citosol]].<ref>{{cite journal |author=Levitan i |title=Modulation of ion channels in neurons and other cells |journal=Annu Rev Neurosci |volume=11 |issue= |pages=119–36 |year=1988 |pmid=2452594 |doi=10.1146/annurev.ne.11.030188.001003}}</ref> Els ellectrolits entren i surten de les cèl·lules a través de proteïnes de la membrana cel·lular denominades [[canal iònic|canals iònics]]. Per exemple, la [[contracció muscular]] depèn del moviment de calci, sodi i potassi a través de canals iònics de la membrana cel·lular i [[túbul-T|túbuls-T]].<ref>{{cite journal |author=Dulhunty A |title=Excitation-contraction coupling from the 1950s into the new millennium |journal=Clin Exp Pharmacol Physiol |volume=33 |issue=9 |pages=763–72 |year=2006 |pmid=16922804 |doi=10.1111/j.1440-1681.2006.04441.x}}</ref> |
Els abundants elements inorgànics actuen com a [[electrolit]]s [[ió|iònics]]. Els ions més importants són el [[sodi]], el [[potassi]], el [[calci]], el [[magnesi]], el [[clor]], el [[fòsfor]] i l'ió orgànic [[bicarbonat]]. El manteniment de [[gradient iònic|gradients]] precisos a través de les [[membrana cel·lular|membranes cel·lulars]] manté la [[pressió osmòtica]] i el [[pH]].<ref>{{cite journal |author=Sychrová H |title=Yeast as a model organism to study transport and homeostasis of alkali metal cations |url=http://www.biomed.cas.cz/physiolres/pdf/53%20Suppl%201/53_S91.pdf |journal=Physiol Res |volume=53 Suppl 1 |issue= |pages=S91–8 |year=2004 |pmid=15119939}}</ref> Els ions també són essencials pels [[nervi]]s i els [[múscul]]s, car els [[potencial d'acció|potencials d'acció]] en aquests teixits es produeixen per l'intercanvi d'electrolits entre el [[fluid extracel·lular]] i el [[citosol]].<ref>{{cite journal |author=Levitan i |title=Modulation of ion channels in neurons and other cells |journal=Annu Rev Neurosci |volume=11 |issue= |pages=119–36 |year=1988 |pmid=2452594 |doi=10.1146/annurev.ne.11.030188.001003}}</ref> Els ellectrolits entren i surten de les cèl·lules a través de proteïnes de la membrana cel·lular denominades [[canal iònic|canals iònics]]. Per exemple, la [[contracció muscular]] depèn del moviment de calci, sodi i potassi a través de canals iònics de la membrana cel·lular i [[túbul-T|túbuls-T]].<ref>{{cite journal |author=Dulhunty A |title=Excitation-contraction coupling from the 1950s into the new millennium |journal=Clin Exp Pharmacol Physiol |volume=33 |issue=9 |pages=763–72 |year=2006 |pmid=16922804 |doi=10.1111/j.1440-1681.2006.04441.x}}</ref> |
||
Els [[metall de transició|metalls de transició]] solen estar presents com a [[element traça|elements traça]] en els organismes, I el [[zinc]] I el [[ferro]] són els més abundants.<ref>{{cite journal |author=Mahan D, Shields R |title=Macro- and micromineral composition of pigs from birth to 145 kilograms of body weight |url=http://jas.fass.org/cgi/reprint/76/2/506 |journal=J Anim Sci |volume=76 |issue=2 |pages=506–12 |year=1998 |pmid=9498359}}</ref><ref name=Husted>{{cite journal |author=Husted S, Mikkelsen B, Jensen J, Nielsen N |title=Elemental fingerprint analysis of barley (Hordeum vulgare) using inductively coupled plasma mass spectrometry, isotope-ratio mass spectrometry, and multivariate statistics |journal=Anal Bioanal Chem |volume=378 |issue=1 |pages=171–82 |year=2004 |pmid=14551660 |doi=10.1007/s00216-003-2219-0}}</ref> Aquests metalls són utilitzats en algunes proteïnes com a [[cofactor (bioquímica)|cofactors]] I són essencials per l’activitat d’enzims com ara la [[catalasa]] o proteïnes portadores d’oxigen com ara l’[[hemoglobina]].<ref>{{cite journal |author=Finney L, O'Halloran T |title=Transition metal speciation in the cell: insights from the chemistry of metal ion receptors |journal=Science |volume=300 |issue=5621 |pages=931–6 |year=2003 |pmid=12738850 |doi=10.1126/science.1085049}}</ref> Aquests cofactors estan units fermament a una proteïna específica; tot I que els cofactors enzimàtics poden ser modificats durant la catàlisi, els cofactors sempre tornen al seu estat original quan s’ha completat la catàlisi. Els micronutrients metàl•lics són portats als organismes per transportadors específics, I units a proteïnes d’emmagatzemament com ara la [[ferritina]] o la [[metal•lotioneïna]] quan no se les utilitza.<ref>{{cite journal |author=Cousins R, Liuzzi J, Lichten L |title=Mammalian zinc transport, trafficking, and signals |url=http://www.jbc.org/cgi/content/full/281/34/24085 |journal=J Biol Chem |volume=281 |issue=34 |pages=24085–9 |year=2006 |pmid=16793761 |doi=10.1074/jbc.R600011200}}</ref><ref>{{cite journal |author=Dunn L, Rahmanto Y, Richardson D |title=Iron uptake and metabolism in the new millennium |journal=Trends Cell Biol |volume=17 |issue=2 |pages=93–100 |year=2007 |pmid=17194590 |doi=10.1016/j.tcb.2006.12.003}}</ref> |
|||
==Catabolisme== |
|||
{{principal|Catabolisme}} |
|||
El catabolisme és el conjunt de processos metabòlics que descomponen molècules grans. Això inclou la descomposició I oxidació de molècules d’aliments. L’objectiu de les reaccions catabòliques és proveir l’energia I els components que necessiten les reaccions anabòliques. La naturalesa exacta d’aquestes reaccions catabòliques varia entre un organisme I l’altre; els [[organòtrof]]s utilitzen molècules orgàniques com a font d’energia, mentre que els [[litòtrof]]s utilitzen substrats inorgànics I els [[fotòtrof]]s capturen la [[llum solar]] com a energia química. Tanmateix, totes aquestes formes de metabolisme depenen de reaccions [[redox]] que impliquen la transferència de molècules donadores reduïdes (per exemple, [[molècula orgànica|molècules orgàniques]], [[aigua]], [[amoníac]], [[sulfur d’hidrogen]] o [[ferrós|ions ferrosos]]) a molècules acceptores com ara l’[[oxigen]], un [[nitrat]] o un [[sulfat]].<ref>{{cite journal |author=Nealson K, Conrad P |title=Life: past, present and future |url=http://www.pubmedcentral.nih.gov/articlerender.fcgi?tool=pubmed&pubmedid=10670014 |journal=Philos Trans R Soc Lond B Biol Sci |volume=354 |issue=1392 |pages=1923–39 |year=1999 |pmid=10670014 |doi=10.1098/rstb.1999.0532}}</ref> En els animals, aquestes reaccions impliquen la descomposició de complexes [[molècula orgànica|molècules orgàniques]] en molècules més senzilles, com ara el [[diòxid de carboni]] o l’aigua. En els organismes [[fotosíntesi|fotosintètics]] com ara les plantes I els [[cianobacteri]]s, aquestes reaccions de transferència d’electrons no alliberen energia, sinó que són utilitzades com un mode d’emmagatzemament de l’energia absorbida de la llum solar.<ref name=Nelson>{{cite journal |author=Nelson N, Ben-Shem A |title=The complex architecture of oxygenic photosynthesis |journal=Nat Rev Mol Cell Biol |volume=5 |issue=12 |pages=971–82 |year=2004 |pmid=15573135 |doi=10.1038/nrm1525}}</ref> |
|||
El conjunt més comú de reaccions catabòliques en els animals es pot separar en tres fases principals. En la primera, molècules orgàniques grans com ara les [[proteïnes]], els [[polisacàrid]]s o els [[lípid]]s són digerides en components més petits a l’exterior de les cèl•lules. Després, aquestes molècules més petites són absorbides per les cèl•lules encara més petites, sovint [[coenzim A|acetil coenzim A]] (CoA), que allibera una mica d’energia. Finalment, el grup acetil del CoA és oxidat en aigua I diòxid de carboni en el [[cicle de Krebs]] I la [[cadena de transport d’electrons]], alliberant l’energia que està emmagatzemada per mitjà de la reducció del coenzim [[nicotinamida adenina dinucleòtid]] (NAD<sup>+</sup>) en NADH. |
|||
===Digestioó=== |
|||
{{principal|Digestió|Aparell digestiu}} |
|||
Macromolècules com ara el midó, la cel•lulosa o les proteïnes no poden ser absorbides ràpidament per les cèl•lules I cal descompondre-les en unitats més petites abans que puguin ser utilitzades en el metabolisme cel•lular. Diversos tipus comuns d’enzims digereixen aquests polímers. Aquests enzims digestius inclouen [[proteasa|proteases]] que digereixen proteïnes en aminoàcids, així com [[glicòsid hidrolasa|glicòsid hidrolases]] que digereixen polisacàrids en monosacàrids. |
|||
Els microbis simplement secreten enzims digestius al medi que els envolta,<ref>{{cite journal |author=Häse C, Finkelstein R |title=Bacterial extracellular zinc-containing metalloproteases |url=http://www.pubmedcentral.nih.gov/articlerender.fcgi?tool=pubmed&pubmedid=8302217 |journal=Microbiol Rev |volume=57 |issue=4 |pages=823–37 |year=1993 |pmid=8302217}}</ref><ref>{{cite journal |author=Gupta R, Gupta N, Rathi P |title=Bacterial lipases: an overview of production, purification and biochemical properties |journal=Appl Microbiol Biotechnol |volume=64 |issue=6 |pages=763–81 |year=2004 |pmid=14966663 |doi=10.1007/s00253-004-1568-8}}</ref> mentre que els animals només secreten aquests enzims de cèl•lules especialitzades al seu [[intestí]].<ref>{{cite journal |author=Hoyle T |title=The digestive system: linking theory and practice |journal=Br J Nurs |volume=6 |issue=22 |pages=1285–91 |year=1997 |pmid=9470654}}</ref> Els aminoàcids o sucres alliberats per aquests enzims extracel•lulars són posteriorment bombejats dins les cèl•lules per proteïnes específiques del [[transport actiu]].<ref>{{cite journal |author=Souba W, Pacitti A |title=How amino acids get into cells: mechanisms, models, menus, and mediators |journal=JPEN J Parenter Enteral Nutr |volume=16 |issue=6 |pages=569–78 |year=1992 |pmid=1494216 |doi=10.1177/0148607192016006569}}</ref><ref>{{cite journal |author=Barrett M, Walmsley A, Gould G |title=Structure and function of facilitative sugar transporters |journal=Curr Opin Cell Biol |volume=11 |issue=4 |pages=496–502 |year=1999 |pmid=10449337 |doi=10.1016/S0955-0674(99)80072-6}}</ref> |
|||
[[Imatge:Catabolism schematic.svg|thumb|left|300px|Un esquema simplificat del catabolisme de [[proteïnes]], [[carbohidrat]]s I [[lípid]]s.]] |
|||
===Energia a partir de compostos orgànics=== |
|||
{{principal|Respiració cel•lular|Fermentació (bioquímica)|Catabolisme dels carbohidrats|Catabolisme dels lípids|Catabolisme de les proteïnes}} |
|||
El catabolisme dels carbohidrats és la descomposició de carbohidrats en unitats més petites. Els carbohidrats solen ser portats a les cèl•lules un cop han estat digerits en [[monosacàrid]]s.<ref>{{cite journal |author=Bell G, Burant C, Takeda J, Gould G |title=Structure and function of mammalian facilitative sugar transporters |journal=J Biol Chem |volume=268 |issue=26 |pages=19161–4 |year=1993 |pmid=8366068}}</ref> Un cop a dins, la ruta principal de descomposició és la[[glicòlisi]], en què sucres com ara la [[glucosa]] I la [[fructosa]] són transformats en [[àcid pirúvic|piruvat]] I es genera una mica d’ATP.<ref name=Bouche>{{cite journal |author=Bouché C, Serdy S, Kahn C, Goldfine A |title=The cellular fate of glucose and its relevance in type 2 diabetes |url=http://edrv.endojournals.org/cgi/content/full/25/5/807 |journal=Endocr Rev |volume=25 |issue=5 |pages=807–30 |year=2004 |pmid=15466941 |doi=10.1210/er.2003-0026}}</ref> El piruvat és un intermedi en diverses rutes metabòliques, però la majoria és convertit en [[acetil-CoA]] I injectat al [[cicle de Krebs]]. Tot I que es genera més ATP en el cicle de Krebs, el producte més important és el NADH, que es forma a partir del NAD<sup>+</sup> quan s’oxida l’acetil-CoA. Aquesta oxidació allibera [[diòxid de carboni]] com a residu. En condicions anaeròbiques, la glicòlisi produeix [[àcid làctic|lactat]] quan l’enzim [[lactat deshidrogenasa]] reoxida el NADH en NAD+ per a reutilitzar-lo en la glicòlisi. Una ruta alternativa per la descomposició de la glucosa és la [[ruta de la pentosa fosfat]], que redueix el coenzim [[NADPH]] I produeix sucres [[pentosa]] com ara la [[ribosa]], el component sucrós dels [[àcid nucleic|àcids nucleics]]. |
|||
La [[hidròlisi]] catabolitza els lípids en àcids grassos lliures I glicerol. El glicerol entra en glicòlisi I els àcids grassos són descomposts per mitjà de [[beta oxidació]] per a alliberar acetil-CoA, que és posteriorment injectat al cicle de Krebs. Els àcids grassos alliberen més energia en oxidar-se que els carbohidrats perquè aquests últims contenen més oxigen a la seva estructura. |
|||
Els [[aminoàcid]]s o bé es fan servir per a sintetitzar proteïnes I altres biomolècules, o bé són oxidats en [[urea]] I diòxid de carboni com a font d’energia.<ref>{{cite journal |author=Sakami W, Harrington H |title=Amino acid metabolism |journal=Annu Rev Biochem |volume=32 |issue= |pages=355–98 |year=1963 |pmid=14144484 |doi=10.1146/annurev.bi.32.070163.002035}}</ref> La ruta de l’oxidació comença amb la retirada del grup amino per una [[transaminasa]]. El grup amino és injectat al [[cicle de l’urea]], deixant un esquelet de carboni deaminat en format de [[cetoàcid]]. Alguns d’aquests cetoàcids son intermedis en el cicle de Krebs; per exemple, la deaminació del [[glutamat]] forma α-[[Àcid cetoglutàric|cetoglutarat]].<ref>{{cite journal |author=Brosnan J |title=Glutamate, at the interface between amino acid and carbohydrate metabolism |url=http://jn.nutrition.org/cgi/content/full/130/4/988S |journal=J Nutr |volume=130 |issue=4S Suppl |pages=988S–90S |year=2000 |pmid=10736367}}</ref> Els [[aminoàcid glucogènic|aminoàcids glucogènics]] també es poden transformar en glucosa per mitjà de la [[gluconeogènesi]] (explicada més avall).<ref>{{cite journal |author=Young V, Ajami A |title=Glutamine: the emperor or his clothes? |url=http://jn.nutrition.org/cgi/content/full/131/9/2449S |journal=J Nutr |volume=131 |issue=9 Suppl |pages=2449S–59S; discussion 2486S–7S |year=2001 |pmid=11533293}}</ref> |
|||
==Transformacions energètiques== |
|||
===Fosforilació oxidativa=== |
|||
[[Imatge:ATPsynthase labelled.png|right|thumb|280px|Estructura de l’[[ATP sintasa]]. El canal de protons I la tija rotant apareixen en blau, I les subunitats de la sintasa en vermell.]] |
|||
{{principal|Fosforilació oxidativa|Quimiosmosi|Mitocondri}} |
|||
En la fosforilació oxidativa, els electrons retirats de molècules d’aliment en rutes com ara el cicle de Krebs són transferits a l’oxigen I l’energia alliberada és utilitzada per a crear ATP. En els [[eucariotes]], això ho fan una sèrie de proteïnes de les membranes dels [[mitocondri]]s anomenades la [[cadena de transport d’electrons]]. En els [[procariotes]], aquestes proteïnes es troben a la [[estructura cel•lular bacteriana|membrana interior]] de la cèl•lula.<ref>{{cite journal |author=Hosler J, Ferguson-Miller S, Mills D |title=Energy transduction: proton transfer through the respiratory complexes |journal=Annu Rev Biochem |volume=75 |issue= |pages=165–87 |year=2006 |pmid=16756489 |doi=10.1146/annurev.biochem.75.062003.101730}}</ref> Aquestes proteïnes utilitzant l’energia alliberada pels electrons que passen de molècules [[agent reductor|reductores]] com el NADH en [[oxigen]] per a bombejar [[protó|protons]] a través d’una membrana.<ref>{{cite journal |author=Schultz B, Chan S |title=Structures and proton-pumping strategies of mitochondrial respiratory enzymes |journal=Annu Rev Biophys Biomol Struct |volume=30 |issue= |pages=23–65 |year=2001 |pmid=11340051 |doi=10.1146/annurev.biophys.30.1.23}}</ref> |
|||
El bombeig de protons a l’exterior dels mitocondris crea una [[difusió|diferència de concentració]] protònica a la membrana I genera un [[gradient electrquímic]].<ref>{{cite journal |author=Capaldi R, Aggeler R |title=Mechanism of the F(1)F(0)-type ATP synthase, a biological rotary motor |journal=Trends Biochem Sci |volume=27 |issue=3 |pages=154–60 |year=2002 |pmid=11893513 |doi=10.1016/S0968-0004(01)02051-5}}</ref> Això empeny els protons de nou dins els mitocondris a través de la base d’un enzim anomenat [[ATP sintasa]]. El flux de protons fa que la subunitat de la tija roti, fent que el [[lloc actiu]] del domini de la sintasa canviï de forma I fosforilitzi [[difosfat d’adenosina]] – convertint-lo en ATP.<ref name=Dimroth/> |
|||
===Energia a partir de compostos inorgànics=== |
|||
{{principal|Metabolisme microbià|Cicle del nitrogen}} |
|||
La [[quimiolitòtrof|quimiolitotròfia]] és un tipus de metabolisme, observat en els [[procariotes]], en què s’obté energia de l’oxidació de [[compost inorgànic|compostos inorgànics]]. Aquests organismes poden utilitzar [[hidrogen]],<ref>{{cite journal |author=Friedrich B, Schwartz E |title=Molecular biology of hydrogen utilization in aerobic chemolithotrophs |journal=Annu Rev Microbiol |volume=47 |issue= |pages=351–83 |year=1993 |pmid=8257102 |doi=10.1146/annurev.mi.47.100193.002031}}</ref> compostos reduïts de [[sofre]] (com ara [[sulfur]], [[sulfur d’hidrogen]] I [[tiosulfat]]),<ref name="Physiology1"/> [[Òxid de ferro (II)|ferro ferrós (FeII)]]<ref>{{cite journal |author=Weber K, Achenbach L, Coates J |title=Microorganisms pumping iron: anaerobic microbial iron oxidation and reduction |journal=Nat Rev Microbiol |volume=4 |issue=10 |pages=752–64 |year=2006 |pmid=16980937 |doi=10.1038/nrmicro1490}}</ref> o [[amoníac]]<ref>{{cite journal |author=Jetten M, Strous M, van de Pas-Schoonen K, Schalk J, van Dongen U, van de Graaf A, Logemann S, Muyzer G, van Loosdrecht M, Kuenen J |title=The anaerobic oxidation of ammonium |journal=FEMS Microbiol Rev |volume=22 |issue=5 |pages=421–37 |year=1998 |pmid=9990725 |doi=10.1111/j.1574-6976.1998.tb00379.x}}</ref> com a fonts de poder reductor, I obtenen energia de l’oxidació d’aquests compostos amb acceptors d’electrons com ara l’[[oxigen]] o el [[nitrit]].<ref>{{cite journal |author=Simon J |title=Enzymology and bioenergetics of respiratory nitrite ammonification |journal=FEMS Microbiol Rev |volume=26 |issue=3 |pages=285–309 |year=2002 |pmid=12165429 |doi=10.1111/j.1574-6976.2002.tb00616.x}}</ref> Aquests processos microbians són importants en [[cicle biogeoquímic|cicles biogeoquímics]] globals com ara l’[[acetogènesi]], la [[nitrificació]] I la [[desnitrificació]], I són essencials per la [[fertilitat del sòl]].<ref>{{cite journal |author=Conrad R |title=Soil microorganisms as controllers of atmospheric trace gases (H2, CO, CH4, OCS, N2O, and NO) |url=http://www.pubmedcentral.nih.gov/articlerender.fcgi?tool=pubmed&pubmedid=8987358 |journal=Microbiol Rev |volume=60 |issue=4 |pages=609–40 |year=1996 |pmid=8987358}}</ref><ref>{{cite journal |author=Barea J, Pozo M, Azcón R, Azcón-Aguilar C |title=Microbial co-operation in the rhizosphere |url=http://jxb.oxfordjournals.org/cgi/content/full/56/417/1761 |journal=J Exp Bot |volume=56 |issue=417 |pages=1761–78 |year=2005 |pmid=15911555 |doi=10.1093/jxb/eri197}}</ref> |
|||
===Energia a partir de la llum solar=== |
|||
{{principal|Fotòtrof|Fotofosforilació|Cloroplast}} |
|||
L’energia de la llum solar és utilitzada per les [[plantes]], els [[cianobacteri]]s, els [[bacteri púrpura|bacteris púrpura]], [[chlorobi|bacteris verds del sofre]] I alguns [[protist]]s. Aquest procés està unit sovint a la conversió de diòxid de carboni en compostos orgànics, com a part de la fotosíntesi, que és tractada més avall. Tanmateix, els sistemes de captura d’energia I de fixació de carboni poden funcionar per separat en els procariotes, car els bacteris púrpura I els bacteris verds del sofre poden utilitzar la llum solar com a font d’energia, tot alternant entre la fixació del carboni I la fermentació de compostos orgànics.<ref>{{cite journal |author=van der Meer M, Schouten S, Bateson M, Nübel U, Wieland A, Kühl M, de Leeuw J, Sinninghe Damsté J, Ward D |title=Diel variations in carbon metabolism by green nonsulfur-like bacteria in alkaline siliceous hot spring microbial mats from Yellowstone National Park |url=http://www.pubmedcentral.nih.gov/articlerender.fcgi?tool=pubmed&pubmedid=16000812 |journal=Appl Environ Microbiol |volume=71 |issue=7 |pages=3978–86 |year=2005 |pmid=16000812 |doi=10.1128/AEM.71.7.3978-3986.2005}}</ref><ref>{{cite journal |author=Tichi M, Tabita F |title=Interactive control of Rhodobacter capsulatus redox-balancing systems during phototrophic metabolism |url=http://www.pubmedcentral.nih.gov/articlerender.fcgi?tool=pubmed&pubmedid=11591679 |journal=J Bacteriol |volume=183 |issue=21 |pages=6344–54 |year=2001 |pmid=11591679 |doi=10.1128/JB.183.21.6344-6354.2001}}</ref> |
|||
La captura de l’energia solar és un procés que és similar en principi a la fosforilació oxidativa, car implica l’emmagatzemament d’energia en forma de gradient de concentració de protons, I l’ús d’aquesta força mecànica dels protons per a alimentar la síntesi d’ATP.<ref name=Dimroth/> Els electrons requerits per a fer funcionar aquesta cadena de transport d’electrons venen de proteïnes recol•lectores de llum anomenades [[centre de reacció fotosintètic|centres de reacció fotosintètics]]. Aquestes estructures es classifiquen en dos tipus segons el tipus de [[pigment fotosintètic]]; la majoria de bacteris fotosintètics només tenen un tipus de centre de reacció, mentre que les plantes I els cianobacteris en tenen dos.<ref>{{cite journal |author=Allen J, Williams J |title=Photosynthetic reaction centers |journal=FEBS Lett |volume=438 |issue=1–2 |pages=5–9 |year=1998 |pmid=9821949 |doi=10.1016/S0014-5793(98)01245-9}}</ref> |
|||
En les plantes, el [[fotosistema|fotosistema II]] utilitza l’energia lumínica per a treure electrons de l’aigua, alliberant oxigen com a residu. Aleshores, els electrons flueixen vers el [[complex del citocrom b6f]], que n’utilitza l’energia per a bombejar protons a través de la membrana de [[tilacoide]] del [[cloroplast].<ref>{{cite journal |author=Nelson N, Ben-Shem A |title=The complex architecture of oxygenic photosynthesis |journal=Nat Rev Mol Cell Biol |volume=5 |issue=12 |pages=971–82 |year=2004 |pmid=15573135 |doi=10.1038/nrm1525}}</ref> Aquests protons tornen a travessar la membrana, alimentant la síntesi d’ATP, com abans. Aleshores, els electrons flueixen a través del [[fotosistema|fotosistema I]], I poden servir o bé per a reduir el coenzim NADP<sup>+</sup>, per a usar-lo en el [[cicle de Calvin]] que és tractat més avall; o bé per a generar encara més ATP.<ref>{{cite journal |author=Munekage Y, Hashimoto M, Miyake C, Tomizawa K, Endo T, Tasaka M, Shikanai T |title=Cyclic electron flow around photosystem I is essential for photosynthesis |journal=Nature |volume=429 |issue=6991 |pages=579–82 |year=2004 |pmid=15175756 |doi=10.1038/nature02598}}</ref> |
|||
==Anabolisme== |
|||
{{principal|Anabolisme}} |
|||
L’’’’anabolisme’’’ és el conjunt de processos metabòlics constructius en què l’energia alliberada pel catabolisme s’utilitza per a sintetitzar molècules complexes. En general, les molècules complexes que formen les estructures cel•lular són produïdes pas a pas a partir de precursors petits I senzills. L’anabolisme inclou tres fases bàsiques. Primerament, la producció de precursors com ara [[aminoàcid]]s, [[monosacàrid]]s, [[terpenoide|isoprenoides]] I [[nucleòtid]]s. Segonament, la seva activació en formes reactives utilitzant energia de l’ATP. Tercerament I final, l’assemblatge d’aquests precursos en molècules complexes com ara [[proteïnes]], [[polisacàrid]]s, [[lípid]]s I [[àcid nucleic|àcids nucleics]]. |
|||
Els organismes presenten diferències en la quantitat de molècules de les cèl•lules poden produir ells mateixos. Els [[autòtrof]]s com ara les plantes poden produir les molècules orgàniques complexes com ara els polisacàrids I les proteïnes a partir de molècules senzilles com el [[diòxid de carboni]] I l’[[aigua]]. Els [[heteròtrof]]s, en canvi, requereixen una font de substàncies més complexes, com ara monosacàrids I aminoàcids, per a produir aquestes molècules complexes. Els organismes també es poden classificar segons la font última de l’energia; els fotoautòtrofs I els fotoheteròtrofs obtenen energia de la llum, mentre que els quimioautòtrofs I els quimioheteròtrofs obtenen energia de reaccions oxidatives inorgàniques. |
|||
===Fixació del carboni=== |
|||
{{principal|Fotosíntesi|Fixació del carboni|Quimiosíntesi}} |
|||
[[Imatge:Chloroplasten.jpg|frame|Cèl•lules vegetals (limitades per parets liles) plenes de cloroplasts (verd), que són el centre de la fotosíntesi.]] |
|||
La fotosíntesi és la síntesi de carbohidrats a partir de la llum solar, el [[diòxid de carboni]] (CO<sub>2</sub>) I l’aigua, produint oxigen com a residu. Aquest procés utilitza l’ATP I la NADPH produïts pels [[centre de reacció fotosintètic|centres de reacció fotosintètics]], com es descriu més amunt, per a transformar CO<sub>2</sub> en [[3-fosfoglicerat]], que després potser transformat en glucosa. Aquesta reacció de fixació del carboni és catalitzada per l’enzim [[RuBisCO]] com a part del [[cicle de Calvin|cicle de Calvin–Benson]].<ref>{{cite journal |author=Miziorko H, Lorimer G |title=Ribulose-1,5-bisphosphate carboxylase-oxygenase |journal=Annu Rev Biochem |volume=52 |issue= |pages=507–35 |year=1983 |pmid=6351728 |doi=10.1146/annurev.bi.52.070183.002451}}</ref> Existeixen tres tipus de fotosíntesi en les plantes: la [[fixació del carboni C3]], la [[fixació del carboni C4]] I la [[Metabolisme àcid de les crassulàcies|fotosíntesi MAC]]. Es diferencien en la ruta que prèn el diòxid de carboni per arribar al cicle de Calvin; les plantes C3 fixen el CO<sub>2</sub> directament, mentre que la C4 I la fotosíntesi MAC incorporen primer el CO<sub>2</sub> en altres compostos, com a adaptacions per a afrontar una intensa llum solar I condicions àrides.<ref>{{cite journal |author=Dodd A, Borland A, Haslam R, Griffiths H, Maxwell K |title=Crassulacean acid metabolism: plastic, fantastic |url=http://jxb.oxfordjournals.org/cgi/content/full/53/369/569 |journal=J Exp Bot |volume=53 |issue=369 |pages=569–80 |year=2002 |pmid=11886877 |doi=10.1093/jexbot/53.369.569}}</ref> |
|||
== Referències == |
== Referències == |
||
Revisió del 13:41, 1 nov 2008

El metabolisme és el conjunt de reaccions químiques que tenen lloc dins un organisme per a mantenir-lo en vida. Aquests processos permeten als organismes créixer i reproduir-se, mantenir les seves estructures, i respondre al seu medi. El metabolisme se sol subdividir en dues categories. El catabolisme descompon matèria orgànica, com per exemple per a extreure energia en la respiració cel·lular. L'anabolisme, d'altra banda, utilitza energia per a construir components de les cèl·lules com ara proteïnes i àcids nucleics.
Les reaccions químiques del metabolisme s'organitzen en rutes metabòliques, en què una substància química és transformada en una altra per una seqüència d'enzims. Els enzims són crucials pel metabolisme, car permeten que els organismes duguin a terme reaccions desitjables però termodinàmicament desfavorables acoblades a reaccions favorables. Els enzims també permeten la regulació de les rutes metabòliques en resposta a canvis en el medi de la cèl·lula o senyals d'altres cèl·lules.
El metabolisme d'un organisme determina quines substàncies li són nutritives i quines li són verinoses. Per exemple, alguns procariotes utilitzen sulfur d'hidrogen com a nutrient, però aquest gas és verinós pels animals.[1] La velocitat del metabolisme, el ritme metabòlic, també influencia la quantitat d'aliment que necessita un organisme.
Una característica sorprenent del metabolisme és la semblança de les rutes metabòliques bàsiques fins i tot entre espècies molt diferents. Per exemple, el conjunt d'àcid carboxílics que són coneguts com a intermedis del cicle de Krebs estan presents en tots els organismes, i existeixen en espècies tan diverses com l'eubacteri unicel·lular Escherichia coli i organismes multicel·lulars enormes com ara els elefants.[2] Aquestes semblances sorprenents en el metabolisme són probablement el resultat de la gran eficiència d'aquestes rutes, i de la seva aparició primerenca en la història evolutiva.[3][4]
Substàncies bioquímiques clau
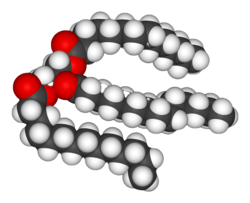
La majoria d'estructures que formen els animals, plantes i microbis es componen de tres tipus bàsics de molècula: els aminoàcids, els carbohidrats i els lípids (sovint anomenats greixos). Com que aquestes molècules són essencials per la vida, el metabolisme es concentra en la manufacturació d'aquestes molècules, en la construcció de cèl·lules i teixits, o descomponent-les per a utilitzar-les com a font d'energia, en la digestió i l'ús d'aliments. Moltes substàncies bioquímiques importants poden ser unides per a formar polímers com ara l'ADN i les proteïnes. Aquestes macromolècules són parts essencials de tots els éssers vius. La taula següent llista alguns dels polímers biològics més comuns.
| Tipus de molècula | Nom de les formes de monòmer | Nom de les formes de polímer | Exemples de formes de polímer |
|---|---|---|---|
| Aminoàcids | Aminoàcids | Proteïnes (anomenades també polipèptids) | Proteïnes fibroses i proteïnes globulars |
| Carbohidrats | Monosacàrids | Polisacàrids | Midó, glucogen i cel·lulosa |
| Àcids nucleics | Nucleòtids | Polinucleòtids | ADN i ARN |
Aminoàcids i proteïnes
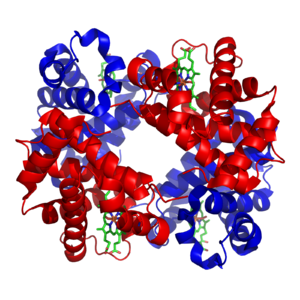
Les proteïnes es componen d'aminoàcids arranjats en una cadena lineal i units per enllaços peptídics. Moltes proteïnes són els enzims que catalitzen les reaccions químiques del metabolisme. Altres proteïnes tenen funcions estructurals o mecàniques, com ara les proteïnes que formen el citosquelet, una mena de carcassa que manté la forma de la cèl·lula.[5] Les proteïnes també són importants en la senyalització cel·lular, la resposta immunitària, l'adhesió cel·lular, el transport actiu a través de membranes i el cicle cel·lular[6]
Lípids
Els lípids són el grup de substàncies bioquímiques més divers. Els seus usos estructurals principals són com a part de membranes com ara la membrana cel·lular, o com a font d'energia.[6] Els lípids solen definir-se com a molècules hidròfobes o amfipàtiques que es dissolen en dissolvents orgànics, com ara el [[benzè] o el cloroform.[7] Els greixos són un gran grups de compostos que contenen àcids grassos i glicerol; una molecula de glicerol unida a tres èsters d'àcids grassos és un triacilglicèrid.[8] Existeixen diverses variacions d'aquesta estructura bàsica, incloent-hi nuclis alternatius com ara la esfingosina en els esfingolípids, i grups hidròfils com ara els fosfats en els fosfolípids. Els esteroides com ara el colesterol són un altre gran grup de lípids manufacturats dins les cèl·lules.[9]
Carbohidrats

Els carbohidrats són aldehids o cetones de cadena recta amb molts grups hidròxils que poden existir com a cadenes rectes o com a anells. Els carbohidrats són les molècules biològiques més abundants, i fan nombroses funcions, com ara l'emmagatzemament i transport d'energia (midó, glucogen) o formar components estructurals (la cel·lulosa en les plantes, la quitina en els animals).[6] Les unitats bàsiques de carbohidrats reben el nom de monosacàrids i inclouen la galactosa, la fructosa I, la més important, la glucosa. Els monosacàrids poden unir-se per a formar polisacàrids de manera gairebé il·limitada.[10]
Nucleòtids
Els polímers ADN i ARN són llargues cadenes de nucleòtids. Aquestes molècules són essencials per l'emmagatzemament i l'ús de la informació genètica, a través dels processos de transcripció i biosíntesi de proteïnes.[6] Aquesta informació és protegida per mecanismes de reparació de l'ADN i es propaga per mitjà de la replicació de l'ADN. Alguns virus tenen un genoma d'ARN, com ara el VIH, que utilitza la transcripció inversa per a crear una plantilla d'ADN a partir del seu genoma víric d'ARN.[11] L'ARN en ribozims com ara els spliceosomes i els ribosomes és similar als enzims, car pot catalitzar reaccions químiques. Es formen nucleòsids individuals per mitjà de la unió d'una base nitrogenada a un sucre ribosa. Aquestes bases són anells heterocíclics que contenen nitrogen, i es classifiquen com a purines o pirimidines. Els nucleòtids també actuen com a coenzims en reaccions metabòliques de transferència de grups.[12]
Coenzims

El metabolisme implica una immensa varietat de reaccions químiques, però la majoria cauen dins uns quants tipus bàsics de reaccions que impliquen la transferència de grups funcionals.[13] Aquesta química comuna permet a les cèl·lules utilitzar un conjunt reduït d'intermedis metabòlics per a transportar grups químics d'una reacció a l'altra.[12] Aquests intermedis de transferència de grups reben el nom de coenzims. Cada tipus de transferència de grups és realitzada per un coenzim determinat, que és el substrat d'un conjunt d'enzims que el produeixen i d'un conjunt d'enzims que el consumeixen. Per tant, aquests coenzims estan sent fabricats, consumits i reciclats contínuament.[14]
Un coenzim essencial és el trifosfat d'adenosina (ATP), la "moneda" universal d'energia de les cèl·lules. Aquest nucleòtid és utilitzat per a transferir energia química entre diferents reaccions químiques. Només hi ha una petita quantitat d'ATP dins les cèl·lules, però com que es regenera contínuament, el cos humà pot utilitzar el seu equivalent en pes en ATP cada dia.[14] L'ATP actua com a pont entre el catabolisme i l'anabolisme; les reaccions catabòliques generen ATP i les anabòliques en conseixen. També serveix com a portador de grups de fosfats en reaccions de fosforilació.
Una vitamina és un compost orgànic requerit en petites quantitats que no pot ser fabricat dins les cèl·lules. En nutrició humana, la majoria de vitamines funcionen com a coenzims després de la modificació; per exemple, totes les vitamines solubles en aigua són fosforilades o enllaçades a nucleòtids quan se les utilitza a les cèl·lules.[15] El nicotinamida adenina dinucleòtid (NADH), un derivat de la vitamina B3 (niacina), és un important coenzim que actua com a acceptor d'hidrogen. Centenars de tipus diferents de deshidrogenases retiren electrons del seu substrat i redueixen NAD+ en NADH. Aquesta forma reduïda del coenzim esdevé aleshores un substrat per qualsevol de les reductases de la cèl·lula que necessitin reduir els seus substrats.[16] El nicotinamida adenina dinucleòtid existeix en dues formes relacionades dins una cèl·lula, NADH i NADPH. La forma NAD+/NADH és més important en les reaccions catabòliques, mentre que la forma NADP+/NADPH és utilitzada en reaccions anabòliques.
Minerals i cofactors
Els elements inorgànics juguen papers crítics en el metabolisme; alguns són abundants (per exemple, el sodi i el potassi) mentre que d'altres funcionen a concentracions mínimes. Aproximadament el 99% de la massa d'un mamífer es compon dels elements carboni, nitrogen, calci, sodi, clor, potassi, hidrogen, fòsfor, oxigen i sofre.[17] Els compostos orgànics(proteïnes, lípids i carbohidrats) contenen la majoria del carboni i del nitrogen, i la majoria d'hidrogen i oxigen estan presents en forma d'aigua.[17]
Els abundants elements inorgànics actuen com a electrolits iònics. Els ions més importants són el sodi, el potassi, el calci, el magnesi, el clor, el fòsfor i l'ió orgànic bicarbonat. El manteniment de gradients precisos a través de les membranes cel·lulars manté la pressió osmòtica i el pH.[18] Els ions també són essencials pels nervis i els músculs, car els potencials d'acció en aquests teixits es produeixen per l'intercanvi d'electrolits entre el fluid extracel·lular i el citosol.[19] Els ellectrolits entren i surten de les cèl·lules a través de proteïnes de la membrana cel·lular denominades canals iònics. Per exemple, la contracció muscular depèn del moviment de calci, sodi i potassi a través de canals iònics de la membrana cel·lular i túbuls-T.[20]
Els metalls de transició solen estar presents com a elements traça en els organismes, I el zinc I el ferro són els més abundants.[21][22] Aquests metalls són utilitzats en algunes proteïnes com a cofactors I són essencials per l’activitat d’enzims com ara la catalasa o proteïnes portadores d’oxigen com ara l’hemoglobina.[23] Aquests cofactors estan units fermament a una proteïna específica; tot I que els cofactors enzimàtics poden ser modificats durant la catàlisi, els cofactors sempre tornen al seu estat original quan s’ha completat la catàlisi. Els micronutrients metàl•lics són portats als organismes per transportadors específics, I units a proteïnes d’emmagatzemament com ara la ferritina o la metal•lotioneïna quan no se les utilitza.[24][25]
Catabolisme
El catabolisme és el conjunt de processos metabòlics que descomponen molècules grans. Això inclou la descomposició I oxidació de molècules d’aliments. L’objectiu de les reaccions catabòliques és proveir l’energia I els components que necessiten les reaccions anabòliques. La naturalesa exacta d’aquestes reaccions catabòliques varia entre un organisme I l’altre; els organòtrofs utilitzen molècules orgàniques com a font d’energia, mentre que els litòtrofs utilitzen substrats inorgànics I els fotòtrofs capturen la llum solar com a energia química. Tanmateix, totes aquestes formes de metabolisme depenen de reaccions redox que impliquen la transferència de molècules donadores reduïdes (per exemple, molècules orgàniques, aigua, amoníac, sulfur d’hidrogen o ions ferrosos) a molècules acceptores com ara l’oxigen, un nitrat o un sulfat.[26] En els animals, aquestes reaccions impliquen la descomposició de complexes molècules orgàniques en molècules més senzilles, com ara el diòxid de carboni o l’aigua. En els organismes fotosintètics com ara les plantes I els cianobacteris, aquestes reaccions de transferència d’electrons no alliberen energia, sinó que són utilitzades com un mode d’emmagatzemament de l’energia absorbida de la llum solar.[6]
El conjunt més comú de reaccions catabòliques en els animals es pot separar en tres fases principals. En la primera, molècules orgàniques grans com ara les proteïnes, els polisacàrids o els lípids són digerides en components més petits a l’exterior de les cèl•lules. Després, aquestes molècules més petites són absorbides per les cèl•lules encara més petites, sovint acetil coenzim A (CoA), que allibera una mica d’energia. Finalment, el grup acetil del CoA és oxidat en aigua I diòxid de carboni en el cicle de Krebs I la cadena de transport d’electrons, alliberant l’energia que està emmagatzemada per mitjà de la reducció del coenzim nicotinamida adenina dinucleòtid (NAD+) en NADH.
Digestioó
Macromolècules com ara el midó, la cel•lulosa o les proteïnes no poden ser absorbides ràpidament per les cèl•lules I cal descompondre-les en unitats més petites abans que puguin ser utilitzades en el metabolisme cel•lular. Diversos tipus comuns d’enzims digereixen aquests polímers. Aquests enzims digestius inclouen proteases que digereixen proteïnes en aminoàcids, així com glicòsid hidrolases que digereixen polisacàrids en monosacàrids.
Els microbis simplement secreten enzims digestius al medi que els envolta,[27][28] mentre que els animals només secreten aquests enzims de cèl•lules especialitzades al seu intestí.[29] Els aminoàcids o sucres alliberats per aquests enzims extracel•lulars són posteriorment bombejats dins les cèl•lules per proteïnes específiques del transport actiu.[30][31]

Energia a partir de compostos orgànics
El catabolisme dels carbohidrats és la descomposició de carbohidrats en unitats més petites. Els carbohidrats solen ser portats a les cèl•lules un cop han estat digerits en monosacàrids.[32] Un cop a dins, la ruta principal de descomposició és laglicòlisi, en què sucres com ara la glucosa I la fructosa són transformats en piruvat I es genera una mica d’ATP.[33] El piruvat és un intermedi en diverses rutes metabòliques, però la majoria és convertit en acetil-CoA I injectat al cicle de Krebs. Tot I que es genera més ATP en el cicle de Krebs, el producte més important és el NADH, que es forma a partir del NAD+ quan s’oxida l’acetil-CoA. Aquesta oxidació allibera diòxid de carboni com a residu. En condicions anaeròbiques, la glicòlisi produeix lactat quan l’enzim lactat deshidrogenasa reoxida el NADH en NAD+ per a reutilitzar-lo en la glicòlisi. Una ruta alternativa per la descomposició de la glucosa és la ruta de la pentosa fosfat, que redueix el coenzim NADPH I produeix sucres pentosa com ara la ribosa, el component sucrós dels àcids nucleics.
La hidròlisi catabolitza els lípids en àcids grassos lliures I glicerol. El glicerol entra en glicòlisi I els àcids grassos són descomposts per mitjà de beta oxidació per a alliberar acetil-CoA, que és posteriorment injectat al cicle de Krebs. Els àcids grassos alliberen més energia en oxidar-se que els carbohidrats perquè aquests últims contenen més oxigen a la seva estructura.
Els aminoàcids o bé es fan servir per a sintetitzar proteïnes I altres biomolècules, o bé són oxidats en urea I diòxid de carboni com a font d’energia.[34] La ruta de l’oxidació comença amb la retirada del grup amino per una transaminasa. El grup amino és injectat al cicle de l’urea, deixant un esquelet de carboni deaminat en format de cetoàcid. Alguns d’aquests cetoàcids son intermedis en el cicle de Krebs; per exemple, la deaminació del glutamat forma α-cetoglutarat.[35] Els aminoàcids glucogènics també es poden transformar en glucosa per mitjà de la gluconeogènesi (explicada més avall).[36]
Transformacions energètiques
Fosforilació oxidativa
En la fosforilació oxidativa, els electrons retirats de molècules d’aliment en rutes com ara el cicle de Krebs són transferits a l’oxigen I l’energia alliberada és utilitzada per a crear ATP. En els eucariotes, això ho fan una sèrie de proteïnes de les membranes dels mitocondris anomenades la cadena de transport d’electrons. En els procariotes, aquestes proteïnes es troben a la membrana interior de la cèl•lula.[37] Aquestes proteïnes utilitzant l’energia alliberada pels electrons que passen de molècules reductores com el NADH en oxigen per a bombejar protons a través d’una membrana.[38]
El bombeig de protons a l’exterior dels mitocondris crea una diferència de concentració protònica a la membrana I genera un gradient electrquímic.[39] Això empeny els protons de nou dins els mitocondris a través de la base d’un enzim anomenat ATP sintasa. El flux de protons fa que la subunitat de la tija roti, fent que el lloc actiu del domini de la sintasa canviï de forma I fosforilitzi difosfat d’adenosina – convertint-lo en ATP.[14]
Energia a partir de compostos inorgànics
La quimiolitotròfia és un tipus de metabolisme, observat en els procariotes, en què s’obté energia de l’oxidació de compostos inorgànics. Aquests organismes poden utilitzar hidrogen,[40] compostos reduïts de sofre (com ara sulfur, sulfur d’hidrogen I tiosulfat),[1] ferro ferrós (FeII)[41] o amoníac[42] com a fonts de poder reductor, I obtenen energia de l’oxidació d’aquests compostos amb acceptors d’electrons com ara l’oxigen o el nitrit.[43] Aquests processos microbians són importants en cicles biogeoquímics globals com ara l’acetogènesi, la nitrificació I la desnitrificació, I són essencials per la fertilitat del sòl.[44][45]
Energia a partir de la llum solar
L’energia de la llum solar és utilitzada per les plantes, els cianobacteris, els bacteris púrpura, bacteris verds del sofre I alguns protists. Aquest procés està unit sovint a la conversió de diòxid de carboni en compostos orgànics, com a part de la fotosíntesi, que és tractada més avall. Tanmateix, els sistemes de captura d’energia I de fixació de carboni poden funcionar per separat en els procariotes, car els bacteris púrpura I els bacteris verds del sofre poden utilitzar la llum solar com a font d’energia, tot alternant entre la fixació del carboni I la fermentació de compostos orgànics.[46][47]
La captura de l’energia solar és un procés que és similar en principi a la fosforilació oxidativa, car implica l’emmagatzemament d’energia en forma de gradient de concentració de protons, I l’ús d’aquesta força mecànica dels protons per a alimentar la síntesi d’ATP.[14] Els electrons requerits per a fer funcionar aquesta cadena de transport d’electrons venen de proteïnes recol•lectores de llum anomenades centres de reacció fotosintètics. Aquestes estructures es classifiquen en dos tipus segons el tipus de pigment fotosintètic; la majoria de bacteris fotosintètics només tenen un tipus de centre de reacció, mentre que les plantes I els cianobacteris en tenen dos.[48]
En les plantes, el fotosistema II utilitza l’energia lumínica per a treure electrons de l’aigua, alliberant oxigen com a residu. Aleshores, els electrons flueixen vers el complex del citocrom b6f, que n’utilitza l’energia per a bombejar protons a través de la membrana de tilacoide del [[cloroplast].[49] Aquests protons tornen a travessar la membrana, alimentant la síntesi d’ATP, com abans. Aleshores, els electrons flueixen a través del fotosistema I, I poden servir o bé per a reduir el coenzim NADP+, per a usar-lo en el cicle de Calvin que és tractat més avall; o bé per a generar encara més ATP.[50]
Anabolisme
L’’’’anabolisme’’’ és el conjunt de processos metabòlics constructius en què l’energia alliberada pel catabolisme s’utilitza per a sintetitzar molècules complexes. En general, les molècules complexes que formen les estructures cel•lular són produïdes pas a pas a partir de precursors petits I senzills. L’anabolisme inclou tres fases bàsiques. Primerament, la producció de precursors com ara aminoàcids, monosacàrids, isoprenoides I nucleòtids. Segonament, la seva activació en formes reactives utilitzant energia de l’ATP. Tercerament I final, l’assemblatge d’aquests precursos en molècules complexes com ara proteïnes, polisacàrids, lípids I àcids nucleics.
Els organismes presenten diferències en la quantitat de molècules de les cèl•lules poden produir ells mateixos. Els autòtrofs com ara les plantes poden produir les molècules orgàniques complexes com ara els polisacàrids I les proteïnes a partir de molècules senzilles com el diòxid de carboni I l’aigua. Els heteròtrofs, en canvi, requereixen una font de substàncies més complexes, com ara monosacàrids I aminoàcids, per a produir aquestes molècules complexes. Els organismes també es poden classificar segons la font última de l’energia; els fotoautòtrofs I els fotoheteròtrofs obtenen energia de la llum, mentre que els quimioautòtrofs I els quimioheteròtrofs obtenen energia de reaccions oxidatives inorgàniques.
Fixació del carboni

La fotosíntesi és la síntesi de carbohidrats a partir de la llum solar, el diòxid de carboni (CO2) I l’aigua, produint oxigen com a residu. Aquest procés utilitza l’ATP I la NADPH produïts pels centres de reacció fotosintètics, com es descriu més amunt, per a transformar CO2 en 3-fosfoglicerat, que després potser transformat en glucosa. Aquesta reacció de fixació del carboni és catalitzada per l’enzim RuBisCO com a part del cicle de Calvin–Benson.[51] Existeixen tres tipus de fotosíntesi en les plantes: la fixació del carboni C3, la fixació del carboni C4 I la fotosíntesi MAC. Es diferencien en la ruta que prèn el diòxid de carboni per arribar al cicle de Calvin; les plantes C3 fixen el CO2 directament, mentre que la C4 I la fotosíntesi MAC incorporen primer el CO2 en altres compostos, com a adaptacions per a afrontar una intensa llum solar I condicions àrides.[52]
Referències
- ↑ 1,0 1,1 Friedrich C «Physiology and genetics of sulfur-oxidizing bacteria». Adv Microb Physiol, vol. 39, 1998, pàg. 235–89. DOI: 10.1016/S0065-2911(08)60018-1. PMID: 9328649.
- ↑ Smith E, Morowitz H «Universality in intermediary metabolism». Proc Natl Acad Sci USA, vol. 101, 36, 2004, pàg. 13168–73. DOI: 10.1073/pnas.0404922101. PMID: 15340153.
- ↑ Ebenhöh O, Heinrich R «Evolutionary optimization of metabolic pathways. Theoretical reconstruction of the stoichiometry of ATP and NADH producing systems». Bull Math Biol, vol. 63, 1, 2001, pàg. 21–55. DOI: 10.1006/bulm.2000.0197. PMID: 11146883.
- ↑ Meléndez-Hevia E, Waddell T, Cascante M «The puzzle of the Krebs citric acid cycle: assembling the pieces of chemically feasible reactions, and opportunism in the design of metabolic pathways during evolution». J Mol Evol, vol. 43, 3, 1996, pàg. 293–303. DOI: 10.1007/BF02338838. PMID: 8703096.
- ↑ Michie K, Löwe J «Dynamic filaments of the bacterial cytoskeleton». Annu Rev Biochem, vol. 75, 2006, pàg. 467–92. DOI: 10.1146/annurev.biochem.75.103004.142452. PMID: 16756499.
- ↑ 6,0 6,1 6,2 6,3 6,4 Nelson, David L.; Michael M. Cox. Lehninger Principles of Biochemistry. Nova York: W. H. Freeman and company, 2005, p. 841. ISBN 0-7167-4339-6. Error de citació: Etiqueta
<ref>no vàlida; el nom «Nelson» està definit diverses vegades amb contingut diferent. - ↑ Fahy E, Subramaniam S, Brown H, Glass C, Merrill A, Murphy R, Raetz C, Russell D, Seyama Y, Shaw W, Shimizu T, Spener F, van Meer G, VanNieuwenhze M, White S, Witztum J, Dennis E «A comprehensive classification system for lipids». J Lipid Res, vol. 46, 5, 2005, pàg. 839–61. DOI: 10.1194/jlr.E400004-JLR200. PMID: 15722563.
- ↑ «Nomenclature of Lipids». IUPAC-IUB Commission on Biochemical Nomenclature (CBN). [Consulta: 20 agost 2007].
- ↑ Hegardt F «Mitochondrial 3-hydroxy-3-methylglutaryl-CoA synthase: a control enzyme in ketogenesis». Biochem J, vol. 338 (Pt 3), 1999, pàg. 569–82. DOI: 10.1042/0264-6021:3380569. PMID: 10051425.
- ↑ Raman R, Raguram S, Venkataraman G, Paulson J, Sasisekharan R «Glycomics: an integrated systems approach to structure-function relationships of glycans». Nat Methods, vol. 2, 11, 2005, pàg. 817–24. DOI: 10.1038/nmeth807. PMID: 16278650.
- ↑ Sierra S, Kupfer B, Kaiser R «Basics of the virology of HIV-1 and its replication». J Clin Virol, vol. 34, 4, 2005, pàg. 233–44. DOI: 10.1016/j.jcv.2005.09.004. PMID: 16198625.
- ↑ 12,0 12,1 Wimmer M, Rose i «Mechanisms of enzyme-catalyzed group transfer reactions». Annu Rev Biochem, vol. 47, 1978, pàg. 1031–78. DOI: 10.1146/annurev.bi.47.070178.005123. PMID: 354490.
- ↑ Mitchell P «The Ninth Sir Hans Krebs Lecture. Compartmentation and communication in living systems. Ligand conduction: a general catalytic principle in chemical, osmotic and chemiosmotic reaction systems». Eur J Biochem, vol. 95, 1, 1979, pàg. 1–20. DOI: 10.1111/j.1432-1033.1979.tb12934.x. PMID: 378655.
- ↑ 14,0 14,1 14,2 14,3 Dimroth P, von Ballmoos C, Meier T «Catalytic and mechanical cycles in F-ATP synthases. Fourth in the Cycles Review Series». EMBO Rep, vol. 7, 3, 2006, pàg. 276–82. DOI: 10.1038/sj.embor.7400646. PMID: 16607397.
- ↑ Coulston, Ann; Kerner, John & Hattner, JoAnn et al. (2006), "Nutrition Principles and Clinical Nutrition", Stanford School of Medicine Nutrition Courses, SUMMIT
- ↑ Pollak N, Dölle C, Ziegler M «The power to reduce: pyridine nucleotides—small molecules with a multitude of functions». Biochem J, vol. 402, 2, 2007, pàg. 205–18. DOI: 10.1042/BJ20061638. PMID: 17295611.
- ↑ 17,0 17,1 Heymsfield S, Waki M, Kehayias J, Lichtman S, Dilmanian F, Kamen Y, Wang J, Pierson R «Chemical and elemental analysis of humans in vivo using improved body composition models». Am J Physiol, vol. 261, 2 Pt 1, 1991, pàg. E190–8. PMID: 1872381.
- ↑ Sychrová H «Yeast as a model organism to study transport and homeostasis of alkali metal cations». Physiol Res, vol. 53 Suppl 1, 2004, pàg. S91–8. PMID: 15119939.
- ↑ Levitan i «Modulation of ion channels in neurons and other cells». Annu Rev Neurosci, vol. 11, 1988, pàg. 119–36. DOI: 10.1146/annurev.ne.11.030188.001003. PMID: 2452594.
- ↑ Dulhunty A «Excitation-contraction coupling from the 1950s into the new millennium». Clin Exp Pharmacol Physiol, vol. 33, 9, 2006, pàg. 763–72. DOI: 10.1111/j.1440-1681.2006.04441.x. PMID: 16922804.
- ↑ Mahan D, Shields R «Macro- and micromineral composition of pigs from birth to 145 kilograms of body weight». J Anim Sci, vol. 76, 2, 1998, pàg. 506–12. PMID: 9498359.
- ↑ Husted S, Mikkelsen B, Jensen J, Nielsen N «Elemental fingerprint analysis of barley (Hordeum vulgare) using inductively coupled plasma mass spectrometry, isotope-ratio mass spectrometry, and multivariate statistics». Anal Bioanal Chem, vol. 378, 1, 2004, pàg. 171–82. DOI: 10.1007/s00216-003-2219-0. PMID: 14551660.
- ↑ Finney L, O'Halloran T «Transition metal speciation in the cell: insights from the chemistry of metal ion receptors». Science, vol. 300, 5621, 2003, pàg. 931–6. DOI: 10.1126/science.1085049. PMID: 12738850.
- ↑ Cousins R, Liuzzi J, Lichten L «Mammalian zinc transport, trafficking, and signals». J Biol Chem, vol. 281, 34, 2006, pàg. 24085–9. DOI: 10.1074/jbc.R600011200. PMID: 16793761.
- ↑ Dunn L, Rahmanto Y, Richardson D «Iron uptake and metabolism in the new millennium». Trends Cell Biol, vol. 17, 2, 2007, pàg. 93–100. DOI: 10.1016/j.tcb.2006.12.003. PMID: 17194590.
- ↑ Nealson K, Conrad P «Life: past, present and future». Philos Trans R Soc Lond B Biol Sci, vol. 354, 1392, 1999, pàg. 1923–39. DOI: 10.1098/rstb.1999.0532. PMID: 10670014.
- ↑ Häse C, Finkelstein R «Bacterial extracellular zinc-containing metalloproteases». Microbiol Rev, vol. 57, 4, 1993, pàg. 823–37. PMID: 8302217.
- ↑ Gupta R, Gupta N, Rathi P «Bacterial lipases: an overview of production, purification and biochemical properties». Appl Microbiol Biotechnol, vol. 64, 6, 2004, pàg. 763–81. DOI: 10.1007/s00253-004-1568-8. PMID: 14966663.
- ↑ Hoyle T «The digestive system: linking theory and practice». Br J Nurs, vol. 6, 22, 1997, pàg. 1285–91. PMID: 9470654.
- ↑ Souba W, Pacitti A «How amino acids get into cells: mechanisms, models, menus, and mediators». JPEN J Parenter Enteral Nutr, vol. 16, 6, 1992, pàg. 569–78. DOI: 10.1177/0148607192016006569. PMID: 1494216.
- ↑ Barrett M, Walmsley A, Gould G «Structure and function of facilitative sugar transporters». Curr Opin Cell Biol, vol. 11, 4, 1999, pàg. 496–502. DOI: 10.1016/S0955-0674(99)80072-6. PMID: 10449337.
- ↑ Bell G, Burant C, Takeda J, Gould G «Structure and function of mammalian facilitative sugar transporters». J Biol Chem, vol. 268, 26, 1993, pàg. 19161–4. PMID: 8366068.
- ↑ Bouché C, Serdy S, Kahn C, Goldfine A «The cellular fate of glucose and its relevance in type 2 diabetes». Endocr Rev, vol. 25, 5, 2004, pàg. 807–30. DOI: 10.1210/er.2003-0026. PMID: 15466941.
- ↑ Sakami W, Harrington H «Amino acid metabolism». Annu Rev Biochem, vol. 32, 1963, pàg. 355–98. DOI: 10.1146/annurev.bi.32.070163.002035. PMID: 14144484.
- ↑ Brosnan J «Glutamate, at the interface between amino acid and carbohydrate metabolism». J Nutr, vol. 130, 4S Suppl, 2000, pàg. 988S–90S. PMID: 10736367.
- ↑ Young V, Ajami A «Glutamine: the emperor or his clothes?». J Nutr, vol. 131, 9 Suppl, 2001, pàg. 2449S–59S; discussion 2486S–7S. PMID: 11533293.
- ↑ Hosler J, Ferguson-Miller S, Mills D «Energy transduction: proton transfer through the respiratory complexes». Annu Rev Biochem, vol. 75, 2006, pàg. 165–87. DOI: 10.1146/annurev.biochem.75.062003.101730. PMID: 16756489.
- ↑ Schultz B, Chan S «Structures and proton-pumping strategies of mitochondrial respiratory enzymes». Annu Rev Biophys Biomol Struct, vol. 30, 2001, pàg. 23–65. DOI: 10.1146/annurev.biophys.30.1.23. PMID: 11340051.
- ↑ Capaldi R, Aggeler R «Mechanism of the F(1)F(0)-type ATP synthase, a biological rotary motor». Trends Biochem Sci, vol. 27, 3, 2002, pàg. 154–60. DOI: 10.1016/S0968-0004(01)02051-5. PMID: 11893513.
- ↑ Friedrich B, Schwartz E «Molecular biology of hydrogen utilization in aerobic chemolithotrophs». Annu Rev Microbiol, vol. 47, 1993, pàg. 351–83. DOI: 10.1146/annurev.mi.47.100193.002031. PMID: 8257102.
- ↑ Weber K, Achenbach L, Coates J «Microorganisms pumping iron: anaerobic microbial iron oxidation and reduction». Nat Rev Microbiol, vol. 4, 10, 2006, pàg. 752–64. DOI: 10.1038/nrmicro1490. PMID: 16980937.
- ↑ Jetten M, Strous M, van de Pas-Schoonen K, Schalk J, van Dongen U, van de Graaf A, Logemann S, Muyzer G, van Loosdrecht M, Kuenen J «The anaerobic oxidation of ammonium». FEMS Microbiol Rev, vol. 22, 5, 1998, pàg. 421–37. DOI: 10.1111/j.1574-6976.1998.tb00379.x. PMID: 9990725.
- ↑ Simon J «Enzymology and bioenergetics of respiratory nitrite ammonification». FEMS Microbiol Rev, vol. 26, 3, 2002, pàg. 285–309. DOI: 10.1111/j.1574-6976.2002.tb00616.x. PMID: 12165429.
- ↑ Conrad R «Soil microorganisms as controllers of atmospheric trace gases (H2, CO, CH4, OCS, N2O, and NO)». Microbiol Rev, vol. 60, 4, 1996, pàg. 609–40. PMID: 8987358.
- ↑ Barea J, Pozo M, Azcón R, Azcón-Aguilar C «Microbial co-operation in the rhizosphere». J Exp Bot, vol. 56, 417, 2005, pàg. 1761–78. DOI: 10.1093/jxb/eri197. PMID: 15911555.
- ↑ van der Meer M, Schouten S, Bateson M, Nübel U, Wieland A, Kühl M, de Leeuw J, Sinninghe Damsté J, Ward D «Diel variations in carbon metabolism by green nonsulfur-like bacteria in alkaline siliceous hot spring microbial mats from Yellowstone National Park». Appl Environ Microbiol, vol. 71, 7, 2005, pàg. 3978–86. DOI: 10.1128/AEM.71.7.3978-3986.2005. PMID: 16000812.
- ↑ Tichi M, Tabita F «Interactive control of Rhodobacter capsulatus redox-balancing systems during phototrophic metabolism». J Bacteriol, vol. 183, 21, 2001, pàg. 6344–54. DOI: 10.1128/JB.183.21.6344-6354.2001. PMID: 11591679.
- ↑ Allen J, Williams J «Photosynthetic reaction centers». FEBS Lett, vol. 438, 1–2, 1998, pàg. 5–9. DOI: 10.1016/S0014-5793(98)01245-9. PMID: 9821949.
- ↑ Nelson N, Ben-Shem A «The complex architecture of oxygenic photosynthesis». Nat Rev Mol Cell Biol, vol. 5, 12, 2004, pàg. 971–82. DOI: 10.1038/nrm1525. PMID: 15573135.
- ↑ Munekage Y, Hashimoto M, Miyake C, Tomizawa K, Endo T, Tasaka M, Shikanai T «Cyclic electron flow around photosystem I is essential for photosynthesis». Nature, vol. 429, 6991, 2004, pàg. 579–82. DOI: 10.1038/nature02598. PMID: 15175756.
- ↑ Miziorko H, Lorimer G «Ribulose-1,5-bisphosphate carboxylase-oxygenase». Annu Rev Biochem, vol. 52, 1983, pàg. 507–35. DOI: 10.1146/annurev.bi.52.070183.002451. PMID: 6351728.
- ↑ Dodd A, Borland A, Haslam R, Griffiths H, Maxwell K «Crassulacean acid metabolism: plastic, fantastic». J Exp Bot, vol. 53, 369, 2002, pàg. 569–80. DOI: 10.1093/jexbot/53.369.569. PMID: 11886877.
Plantilla:Enllaç AD Plantilla:Enllaç AD Plantilla:Enllaç AD Plantilla:Enllaç AD
