Anticòs

Els anticossos (també coneguts com a immunoglobulines[1]) són glicoproteïnes del tipus gamma globulina. Existeixen en forma soluble a la sang o altres líquids corporals dels vertebrats, disposen d'una forma idèntica que actua com receptor dels limfòcits B i són utilitzats pel sistema immunitari per identificar i neutralitzar elements estranys al cos, com ara bacteris, virus o paràsits.[2]
L'anticòs típic està constituït per unitats estructurals bàsiques, cadascuna d'elles amb dues grans cadenes pesants i dues cadenes lleugeres de menor mida, que formen monòmers amb una unitat, dímers amb dues unitats, tetràmers amb quatre unitats o pentàmers amb cinc unitats. Els anticossos són sintetitzats per un tipus de leucòcits anomenats limfòcits B. N'existeixen diferents tipus, anomenats isotips, que es diferencien per la forma de les cadenes pesants que tenen. Es coneixen cinc tipus diferents d'isotipus en els mamífers, que desenvolupen funcions diferents, contribuint a dirigir la resposta immunitària adequada per cada tipus de cos estrany que troben.[3]
Tot i que l'estructura general de tots els anticossos és molt similar, una petita regió de l'àpex de la proteïna és extremadament variable, cosa que possibilita l'existència de milions d'anticossos diferents, cadascun amb un extrem lleugerament diferent. Aquesta part de la proteïna és coneguda com a regió hipervariable. Cadascuna d'aquestes variants es pot unir a una "diana" diferent, coneguda com a antigen.[4][5] Aquesta enorme diversitat d'anticossos permet al sistema immunitari reconèixer una diversitat igualment elevada d'antígens. L'única part de l'antigen recognoscible per l'anticòs es denomina epítop. Aquests epítops s'uneixen amb el seu anticòs corresponent en una interacció molt específica que es denomina acoblament induït, que permet als anticossos identificar i unir-se només al seu antigen entre tots els milions de molècules diferents que componen un organisme.
El reconeixement d'un antigen per part d'un anticòs el "marca" per ser atacat per altres parts del sistema immunitari. Els anticossos també poden neutralitzar directament els seus objectius, per exemple, mitjançant la unió a una part d'un patogen necessària perquè aquest provoqui una infecció.
L'extensa població d'anticossos i la seva diversitat és generada per combinacions aleatòries d'un conjunt de segments genètics que codifiquen diferents llocs de la unió de l'antigen (o paràtops), que posteriorment pateixen mutacions en aquesta zona del gen de l'anticòs, cosa que produeix una major diversitat.[3][6] Els gens dels anticossos també es reorganitzen en un procés conegut com a canvi de classe d'immunoglobulina, que canvia la base de la cadena pesant per una altra, creant un isotip d'anticossos diferents que manté la regió variable específica per l'antigen diana. Això permet que un mateix anticòs pugui ser utilitzat per les diferents parts del sistema immunitari. La producció d'anticossos és la funció principal del sistema immunitari humoral.[7]
Terminologia[modifica]

En general, com ja s'ha dit més amunt, es considera que "anticòs" i "immunoglobulina" són termes sinònims; el primer terme fa referència a la seva funció, mentre que el segon al·ludeix a la seva estructura. El terme "gammaglobulina" fa referència a les propietats electroforètiques de les immunoglobulines solubles en sèrum sanguini, si bé algunes immunoglobulina migren amb les fraccions alfa, beta i fins i tot amb l'albúmina.
Història[modifica]
El 1890 començà l'estudi dels anticossos quan Emil Adolf von Behring i Shibasaburo Kitasato van descriure l'activitat dels anticossos contra la diftèria i la toxina tetànica. Behring i Kitasato van proposar la teoria de la immunitat humoral, que establia l'existència d'un mediador en el sèrum sanguini que podia reaccionar amb un antigen estrany, donant-li el nom d'anticòs.[8][9] El 1897, la seva idea conduí Paul Ehrlich a proposar la teoria de la cadena lateral de la interacció entre l'antigen i l'anticòs, i postular la hipòtesi que existeixen receptors (descrits amb "cadenes laterals") a la superfície de les cèl·lules que es poden unir específicament a toxines en una interacció de tipus "pany i clau", i que aquesta reacció d'acoblament era el desencadenant de la producció d'anticossos.[10]
El 1904, seguint la idea d'altres investigadors que els anticossos es trobaven lliures a la sang, Almroth Wright va suggerir que els anticossos solubles revestien els bacteris per marcar-los per ser fagocitats i destruïts, mitjançant un procés denominat opsonització.[11]
En la dècada dels 1920, Michael Heidelberger i Oswald Avery van descobrir la naturalesa d'aquests anticossos en observar que els antígens podien ser precipitats per ells i demostrant que aquests eren un tipus de proteïnes.[12]

El 1938, John Marrack va publicar el resultat de les recerques sobre les propietats bioquímiques de les unions antigen-anticòs.[13] Després, a la dècada dels 1940 tingué lloc un gran avenç, quan Linus Pauling va confirmar la teoria de pany i clau proposada per Ehrlich en què es mostrava que les interaccions entre els anticossos i els antígens depenien més de la seva forma que de la seva composició química.[14] El 1948, Astrid Fagreaus va descobrir que els limfòcits B en la seva forma de plasmòcit eren els responsables de la producció d'anticossos.[15]
Els següents treballs d'investigació es van concentrar en la caracterització de l'estructura molecular dels anticossos:
- A principis de la dècada del 1960 es va produir el principal avenç en aquest sentit, amb el descobriment per part de Gerald M. Edelman i Joseph Gally de la cadena lleugera,[16] i el descobriment que era idèntica a la proteïna de Bence Jones, descrita el 1845 per Henry Bence Jones.[17] Edelman continuà amb el descobriment que els anticossos estaven composts de cadenes lleugeres i pesants unides per enllaços disulfurs.
- Per les mateixes dates, Rodney Porter va caracteritzar les regions d'unió de l'anticòs (Fab) i la cua de l'anticòs (Fc) del tipus IgG.[18] Conjuntament, aquests científics deduïren l'estructura i la seqüència completa del aminoàcids de la IgG, per la qual cosa reberen ex aequo el Premi Nobel de fisiologia i medicina el 1972.[18]
- Mentre la majoria d'aquests primers estudis es van fixar en les IgM i IgG, a la dècada del 1960 es van identificar altres isotips d'immunoglobulina: Thomas Tomasi va descobrir els anticossos secretats (IgA),[19] David Rowe i John Fahey van identificar la IgD[20] i la IgE fou identificada per Kikishige Ishizaka i Teruki Ishizaka com una classe d'anticossos implicats en reaccions al·lèrgiques.[21]
- El 1975, César Milstein i Georges J. F. Köhler van idear el mètode per la producció d'anticossos monoclonals.[22] El 1976, els estudis genètics van revelar la base de la immensa diversitat dels anticossos a ser identificada la recombinació dels gens d'immunoglobulina per Susumu Tonegawa.[23]
Formes d'anticossos[modifica]
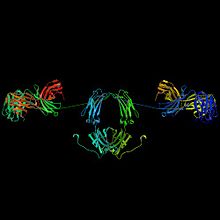
Els limfòcits B activats es diferencien o bé en plasmòcits, el paper dels quals és la producció d'anticossos solubles, o bé en limfòcits B de memòria, que sobreviuen a l'organisme durant els anys següents per possibilitar que el sistema immunitari reconegui l'antigen i respongui més ràpidament a futures infeccions amb un mateix patogen.[24]
Els anticossos són, per tant, uns productors essencials del sistema immunitari adaptatiu que aprenen i recorden les respostes davant de patògens invasors. Els anticossos es troben en dues formes: en forma soluble secretada a la sang i altres líquids del cos, i en forma unida a la membrana cel·lular, ancorada a la superfície d'un limfòcit B.
Forma soluble[modifica]
Els anticossos solubles són secretats per un limfòcit B actiu (en la seva forma de cèl·lula plasmàtica) per unir-se a substàncies estranyes i senyalitzar-les per la seva destrucció per la resta del sistema immunitari. També se'ls pot anomenar "anticossos lliures" (fins que s'uneixen a un antigen i acaben com una part d'un complex antigen-anticòs) o "anticossos secretats". En aquestes formes solubles s'uneixen a les immunoglobulines moleculars addicionals. A la IgM, per exemple, es troba una glicoproteïna unida a la fracció constant mitjançant ponts disulfurs d'uns 15 KDa anomenats cadenes J. A l'isotip IgA, a més, se li afegeix l'anomenada "peça de secreció", que és una glicoproteïna que es forma a les cèl·lules epitelials i les glàndules exocrines, i que posteriorment s'uneix a la immunoglobulina per facilitar-ne la secreció.
Forma ancorada a membrana[modifica]
La forma ancorada a membrana d'un anticòs es pot anomenar "immunoglobulina de superfície" (sIg) o "immunoglobulina de membrana" (mIg) i no és secretada; sempre està associada a la membrana cel·lular. Forma part del receptor del limfòcit B (BCR), que li permet detectar quan un antigen específic és present a l'organisme i provocar l'activació del limfòcit B.[25] El BCR es compon d'anticossos IgD o IgM units a la superfície de la membrana i els seus heterodímers associats a l'Ig-α i a l'Ig-β que tenen capacitat de produir la transducció de senyal del reconeixement de l'anticòs a la cèl·lula.[26] Un limfòcit B humà típic té entre 50.000 i 100.000 anticossos units a la superfície.[26] Després de l'acoblament de l'antigen, aquests anticossos s'agrupen en grans pedaços el diàmetre dels quals pot excedir 1μm en rais lipídics que aïllen els BCR de la majoria de receptors restants de senyalització cel·lular.[26] Aquests pedaços podrien millorar l'eficiència de la resposta immunitària cel·lular.[27] En els éssers humans, la superfície cel·lular està lliure d'altres proteïnes al voltant dels receptors dels limfòcits B en distàncies d'uns milers d'àngstroms,[26] cosa que redueix de tal manera les influències que competeixen amb la seva funció que fins i tot aïlla els BCRs.
Isotips, al·lotips i idiotips[modifica]
| Nombre | Classes | Descripció | Complexos d'anticossos |
| IgA | 2 | Es troba a les mucoses, com el tub digestiu, el tracte digestiu i el tracte urogenital. N'impedeix la colonització per part de patògens.[28] També es troba a la saliva, les llàgrimes i la llet. | 
|
| IgD | 1 | La seva funció consisteix principalment en servir de receptor d'antígens en limfòcits B que no han estat exposats als antígens.[29] La seva funció està menys definida que en altres isotips. | |
| IgE | 1 | S'uneix a un al·lergogen i desencadena l'alliberament d'histamina per part dels mastòcits i basòfils, i està implicada en l'al·lèrgia. També protegeix contra cucs paràsits.[7] | |
| IgG | 4 | Proporciona, en les seves quatre formes, la major part de la protecció immunitària basada en anticossos contra els patògens invasors.[7] És l'únic anticòs capaç de creuar la placenta per proporcionar al fetus una immunitat passiva. | |
| IgM | 1 | S'expressa a la superfície dels limfòcits B i en forma de secreció amb gran afinitat per la seva diana. Elimina els patògens als estadis immediats de la resposta immunitària mitjançada pels limfòcits B (humoral), fins que existeixen prou IgGs.[7][29] |
Els anticossos poden presentar-se en diferents varietats, conegudes com a isotips o classes. En els mamífers n'existeixen cinc isotips, coneguts com a IgA, IgD, IgE, IgG i IgM; en altres tipus d'animals existeixen diferents tipus d'immunoglobulines, com per exemple la IgY, un anticòs semblant a la IgG mamífera que es troba al rovell dels ous dels ocells. S'anomenen mitjançant el prefix "Ig", que significa "immunoglobulina", i difereixen en les seves propietats biològiques, localitzacions funcionals i capacitat de reconèixer diferents tipus d'antígens, tal com es mostra a la taula.[30]
Isotips[modifica]
Els isotips canvien durant el desenvolupament i l'activació dels limfòcits B. Abans de la seva maduració, quan encara no han estat exposats a l'antigen, es coneixen com a limfòcits B verges i només expressen els isotips IgM en la seva forma ancorada a la superfície cel·lular. Els limfòcits comencen a expressar tant IgM com IgD quan arriben a la maduresa, i en aquest moment ja estan preparats per respondre als seus antígens.[31] L'activació d'un limfòcit B segueix la seva trobada i unió amb el seu antigen, cosa que estimula la cèl·lula perquè es divideixi i es diferenciï en una cèl·lula productora d'anticossos denominada cèl·lula plasmàtica. En aquesta forma activada, els limfòcits B comencen a secretar anticossos en lloc d'ancorar-los a la membrana. Algunes cèl·lules filles dels limfòcits B activats pateixen un canvi isotòpic, un mecanisme que provoca que la producció d'anticossos en les formes IgM o IgD es transmuti als altres tipus, IgE, IgA o IgG, que juguen diferents papers al sistema immunitari.
Al·lotips[modifica]
S'entén per al·lotip les petites diferències en la seqüència d'aminoàcids a la regió constant de les cadenes lleugeres i pesants dels anticossos produïts pels diferents individus d'una espècie.
En els humans s'han descrit tres tipus de determinants al·lotípics:
- El 1956 Grubb i Laurell van descriure el sistema Gm en la classe d'immunoglobulines IgG. Aquest sistema va posar de manifest els diversos al·lotips de les cadenes pesants. També permet diferenciar quatre subclasses en aquestes molècules: IgG1, IgG2, IgG3 i IgG4. Els al·lotips són determinats genèticament.[32]
- El 1961, Claude Ropartz i col·laboradors van descobrir el sistema Km (anomenat inicialment Inv), situat a la cadena lleugera Kappa. Aquest al·lotip està present a totes les classes d'immunoglobulines.
- També existeix el sistema ISf, situat en la cadena pesant γ1 de la IgG1. L'expressió d'aquesta especificitat augmenta amb l'edat. En els individus caucàsics, és d'un 25% en els subjectes de menys de 20 anys i de fins a un 60% en els de més de 70 anys.
- Els al·lotips definits pel sistema Am se situen a les IgA, i més precisament a les cadenes α2. Existeixen dos isotips, α1 i α2, que caracteritzen les subclasses Am1 i Am2 de les IgA.
Idiotip[modifica]
L'idiotip és l'epítop propi d'una molècula pertanyent a un clon en particular. Aquest element forma part o està molt pròxim al lloc de reconeixement de l'antigen, i està situat a la porció variable Fab. En altres paraules, és el paràtop, o la regió propera d'una immunoglobulina que pot ser reconeguda com un epítop per determinats limfòcits. Segons la teoria de Jerne, la formació d'anticossos antiidiotips formaria una xarxa (xarxa de Jerne) la funció de la qual seria regular la síntesi de noves immunoglobulines.
Estructura[modifica]
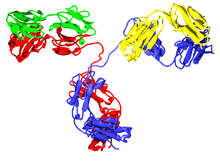
Els anticossos són proteïnes plasmàtiques globulars pesants (~150kDa). Tenen cadenes de sucres unides a alguns dels seus residus d'aminoàcids,[33] és a dir, els anticossos són glicoproteïnes. La unitat bàsica funcional de cada anticossos és el monòmer d'immunoglobulina, que conté una sola unitat d'Ig. Els anticossos secretats també poden ser dímers amb dues unitats d'Ig, en el cas de les IgA; tetràmers, amb quatre unitats d'Ig, en el cas de les IgM dels teleostis; o pentàmers, amb cinc unitats d'IgM, com en les IgM dels mamífers.[34]
Primers treballs[modifica]
Les primeres investigacions sobre l'estructura dels anticossos foren dutes a terme per Rodney Robert Porter i Gerald M. Edelman mitjançant senzilles digestions amb pepsina i papaïna seguides d'electroforesi. Ambdós reberen el Premi Nobel de medicina el 1972. També fou important la figura d'Alfred Nisonoff.
- A la dècada del 1950, Porter va procedir a fer una digestió suau amb papaïna, obtenint tres fragments, dos dels quals retenien l'especificitat de l'antigen (Fab), mentre que el tercer no mostrava activitat d'unió, tot i que es podia cristal·litzar (Fc).
- El 1959, Edelman, utilitzant 2-mercaptoetanol i urea, seguit d'electroforesi, va aconseguir aïllar les cadenes lleugeres i pesants, en dissociar-ne els enllaços disulfurs i no covalents.
- Aquell mateix any, Porter va identificar els components de les cadenes llegueres i pesants que es trobaven als seus fragments de papaïna i pepsina, i d'aquesta manera va determinar-ne el pes molecular.
- El 1960, Nisonoff demostrà que la digestió amb pepsina d'IgG produïa un fragment bivalent, que en realitat està format per dos altres fragments, i el denominà F (ab')₂ .[36]
Dominis de la immunoglobulina[modifica]
El monòmer d'Ig és una molècula en forma de Y que consta de dues cadenes de polipèptids; dues cadenes pesants idèntiques i dues cadenes lleugeres també idèntiques connectades per enllaços disulfurs.[30] Cada cadena es compon de dominis estructurals anomenats dominis Ig. Aquests dominis contenen entre 70 i 110 aminoàcids i es classifiquen en diferents categories, per exemple en variables (IgV) i constants (IgC), segons la seva mida i funció.[37] Tenen un "plec immunoglobulínic" característic en el qual dues làmines beta generen una forma d'"entrepà", romanent juntes per interaccions entre cisteïnes ben conservades al llarg de l'evolució, així com d'altres aminoàcids carregats.
Cadena pesant[modifica]
Hi ha cinc tipus d'Ig en els mamífers, que es denominen per lletres greges α, δ, ε, γ i μ.[4] El tipus de cadena pesant present defineix la classe de l'anticòs. Aquestes cadenes es troben als anticossos IgA, IgD, IgE, IgG i IgM respectivament. Les diferents cadenes pesants es diferencien en la mida i en la composició: α i γ contenen aproximadament 450 aminoàcids, mentre que μ i ε en tenen aproximadament 550.[4]
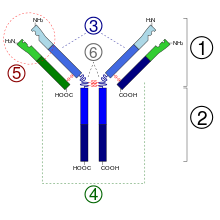
2. Regió Fc
3. Cadena pesant amb un domini constant (CH1), una regió frontissa, i dos més constants, els dominis (CH2 i CH3).
4. cadena lleugera amb un domini variable (VL) i una constant (CL)
5. Lloc d'unió a l'antigen (paràtop)
6. Regions frontissa.
Les cadenes pesants γ, α i δ tenen una regió constant composta de tres dominis estructurals Ig en tàndem i una regió frontissa per proporcionar-los flexibilitat.[30] Les cadenes pesants μ i ε tenen una regió constant composta de quatre dominis immunoglobulínics.[4] La regió variable de la cadena pesant difereix en els anticossos produïts per diferents limfòcits B, però és igual en tots els anticossos produïts pel mateix limfòcit B o per la seva línia clonal. La regió variable d'una cadena pesant és d'aproximadament 110 aminoàcids i està composta d'un únic domini Ig.
Recentment s'ha pogut determinar la topologia in vitro del gen de la cadena pesant, Igh, sent un dels primers estudis en aquest camp. El resultat és que la cromatina es disposa formant girs successius units per linkers, donant lloc a formes similars a la d'una flor. La posició relativa dels diferents segments varia dràsticament al llarg del desenvolupament del limfòcit B, permetent així una major varietat d'interaccions genòmiques.[38]
Cadena lleugera[modifica]
En els mamífers hi ha dos tipus de cadenes lleugeres, anomenades lambda (λ) i kappa (κ).[4] Una cadena lleugera conté dos dominis successius: un domini constant i un domini variable. La longitud aproximada de la cadena lleugera és d'entre 211 i 217 aminoàcids.[4] Cada anticòs conté dues cadenes lleugeres que sempre són idèntiques. Només un tipus de cadena lleugera, κ o λ, està present al mateix anticòs en els mamífers. Altres tipus de cadenes lleugeres com la cadena iota (ι), es troben en vertebrats inferiors com els peixos cartilaginosos i en els teleostis.
Regions Fab i Fc[modifica]
Algunes parts de l'anticòs tenen funcions úniques. Els extrems de l'Y, per exemple, contenen el lloc que s'uneix a l'antigen i, per tant, reconeixen elements estranys específics. Aquesta regió de l'anticòs es diu fragment d'unió a l'antigen, o regió Fab. Està compost d'un domini constant i un altre de variable de cadascuna de les cadenes (lleugera i pesant) de l'anticòs.[39] El paràtop està format pels dominis variables de la cadena pesant i lleugera a l'extrem amino terminal del monòmers de l'anticòs. El paper de la base de l'Y consisteix a modular l'activitat de la cèl·lula immunitària. Aquesta regió es diu fragment cristal·litzable o Fc i està composta de dos o tres dominis constants d'ambdues cadenes pesants, depenent de la classe de l'anticòs.[4] Mitjançant la unió a proteïnes específiques, la regió Fc s'assegura que cada anticòs generi una resposta immunitària apropiada per un antigen determinat.[40] La regió Fc també s'uneix a diversos receptors cel·lulars com el receptor del Fc i altres molècules del sistema immunitari com les proteïnes del complement. En fer-ho, es produeixen diferents efectes fisiològics com l'opsonització, la lisi cel·lular i la desgranulació dels mastòcits, basòfils i eosinòfils.[41]
IgG[modifica]

Propietats físiques:
- Massa molecular: 150.000 Da.
- Nombre d'aminoàcids: 450.
- Dominis de la cadena pesant: 3.
- Forma molecular: Sempre monòmer.
- Quatre subclasses (IgG1, IgG2, IgG3 i IgG4). Difereixen en el nombre i l'organització dels enllaços disulfur i en les seves activitats biològiques.
- Semivida: 23 dies.
- Concentració en sèrum: 10 mg /ml.
- Llocs d'unió per l'antigen: 2.
Propietats biològiques:
- Ig majoritària al sèrum (80%).
- Predominant en la resposta secundària.
- Pot travessar la barrera placentària.
- Activa el complement.
- S'uneix a receptors per Fc en els fagòcits.
IgM[modifica]

1: Unitat bàsica.
2: Cadenes pesants.
3: Cadenes lleugeres.
4: Cadena J.
5: Ponts disulfur intermoleculars.
Propietats físiques:
- Massa molecular: 900.000 Da (pentàmer).
- Forma molecular: pentàmer (o hexàmer) en sèrum; monòmer en membrana.
- Nombre d'aminoàcids (monòmer): 550.
- Dominis CH monòmer: 4.
- Semivida: 5 dies.
- Concentració al sèrum: 1,5 mg /ml.
- Cadenes polipeptídiques diferents: 3 (H,L,J).
- Llocs d'unió per l'antigen: 10 (pentàmer).
Propietats biològiques:
- 5-10% de les Ig del sèrum.
- Predominant en la resposta primària.
- Primer isotip produït en el nounat.
- Activa el complement.
- Actua com receptor antigènic durant el desenvolupament dels limfòcits B.
IgA[modifica]

1: Cadenes pesants.
2: Cadenes lleugeres.
3: Cadena J.
4: Peça secretora.
Propietats físiques:
- Massa molecular: 150.000-600.000 Da.
- Monòmer, dímer, trímer o tetràmer.
- Dues subclasses: IgA1 i IgA2.
- Nombre d'aminoàcids (monòmer): 470.
- Dominis cadena pesant (monòmer): 3
- Semivida: 6 dies.
- Concentració al sèrum: 3 mg /ml.
- Cadenes polipeptídiques diferents: 4 en la forma secretada (H,L,J i peça secretora)
- Llocs d'unió a l'Ag: 4 (dímer)
Propietats biològiques:
- 15-20% de les Ig del sèrum.
- Predominant en les secrecions mucoses.
- Present en la llet materna.
- La forma dimèrica conté la cadena J i el component secretor que li proporciona resistència a les proteases.
IgE[modifica]
Propietats físiques:
- Massa molecular: 188.000 Da.
- Forma molecular: monòmer.
- Nombre d'aminoàcids (monòmer): 550.
- Dominis cadena pesant monòmer: 4.
- Semivida: 1-5 dies.
- Concentració al sèrum: molt baixa.
- Cadenes polipeptídiques diferents: 2.
- Determinants antigènics: 2.
Propietats biològiques:
- Concentració en sèrum molt baixa.
- Nivells augmentats en pacients al·lèrgics.
- Important en la defensa contra paràsits (en especial cucs helmints).
Funció[modifica]
Com que els anticossos existeixen en forma lliure al corrent sanguini, es diu que formen part del sistema immunitari humoral. Els anticossos circulants són produïts per línies clonals de limfòcits B que responen específicament a un antigen, que pot ser un fragment de proteïna de la càpsida vírica, per exemple. Els anticossos contribueixen a la immunitat de tres maneres diferents: poden impedir que els agents patògens entrin a les cèl·lules o les danyin en unir-se a elles, poden promoure l'eliminació d'un patogen per part dels macròfags i altres cèl·lules mitjançant un revestiment del patogen, i poden desencadenar la destrucció directa del patogen (lisi) estimulant altres respostes immunitàries com la via del complement.[42]
Activació del complement[modifica]
Els anticossos que es poden unir a la superfície dels antígens atrauen els primers components de la cascada del complement mitjançant la seva regió Fc i iniciant l'activació de la ruta "clàssica" del complement.[42] Això acaba amb la mort del bacteri de dues maneres:[7] primer, la unió de les molècules del complement amb l'anticòs marca el microorganisme per la posterior ingestió per part dels fagòcits, en un procés anomenat opsonització. Aquests fagòcits són atrets per determinades molècules del complement. En segon lloc, alguns components del sistema del complement formen un complex d'atac a la membrana per ajudar els anticossos a matar el bacteri per lisi.[43]
Activació de cèl·lules efectores[modifica]
Per combatre els agents patògens que es repliquen a l'exterior de les cèl·lules, els anticossos s'uneixen als patògens per assemblar-los, provocant-ne l'aglutinació. Com que cada anticòs té almenys dos paràtops, es poden unir a més d'un antigen acoblant-se als epítops idèntics presentats a la superfície d'aquests antígens. Revestint el patogen, els anticossos estimulen les funcions efectores contra ell en les cèl·lules que reconeixen la regió Fc.[7]
Les cèl·lules que reconeixen els agents patògens revestits tenen receptors del Fc que, com ho indica el seu nom, interaccionen amb la regió Fc dels anticossos IgA, IgG i IgE. La unió d'un anticòs particular amb el receptor Fc d'una determinada cèl·lula desencadena en ella una funció efectora: els fagòcits duen a terme la fagocitosi, els mastòcits i els neutròfils produeixen la desgranulació, i les cèl·lules NK alliberen citocines i molècules citotòxiques que finalment destruiran el microbi invasor. Els receptor Fc són específics a l'isotip, cosa que dona una major flexibilitat al sistema immunitari, afectant només el mecanisme immunitari adequat per cada patogen diferent.[4]

Diversitat de les immunoglobulines[modifica]
Pràcticament tots els microorganismes poden desencadenar la resposta dels anticossos. El reconeixement i la destrucció reeixida de tipus molt diferents de patògens requereixen que els anticossos tinguin una enorme diversitat. La seva composició d'aminoàcids varia per permetre'ls interaccionar amb antígens molt diferents.[44] S'ha estimat que els éssers humans generen uns deu mil milions d'anticossos diferents, cadascun d'ells capaç d'unir-se a un epítop diferent.[45] Tot i que generen un enorme repertori de diferents anticossos en un mateix individu, el nombre de gens disponibles per fabricar aquestes proteïnes és limitat. En els vertebrats han evolucionat diferents mecanismes genètics complexos per permetre que els limfòcits B generin aquesta diversitat a partir d'un nombre relativament reduït de gens d'anticossos.[46]
Varietat de dominis[modifica]

La regió (locus) del cromosoma que codifica un anticòs és gran i conté diversos gens diferents per cada domini de l'anticòs - en els humans, el locus que conté els gens per les cadenes pesants (IGH@) es troba al cromosoma 14 i els locus que contenen els gens lambda i kappa de la cadena lleugera (IGL@) i IGK@) es troben als cromosomes 22 i 2. Un d'aquests dominis és conegut com a "domini variable" i està present a totes les cadenes lleugeres i pesants dels anticossos, però pot ser diferent entre els diferents anticossos generats pels diversos llinatges de limfòcits B. Les diferències entre els dominis variables es localitzen en tres bucles coneguts com a regions hipervariables (HV-1, HV-2 i HV-3) o regions determinants de la complementarietat (CDR1, CDR2 i CDR3). Les CDR es mantenen entre els dominis variables per regions de marc conservat. El locus de la cadena pesant conté uns 65 gens de domini variable diferents, que difereixen en la seva CDR. Combinant aquests gens amb diversos gens d'altres dominis es genera un gran contingent d'anticossos amb un alt grau de variabilitat. Aquesta combinació es denomina "recombinació V(D)J".[47]
Recombinació V(D)J[modifica]

La recombinació somàtica de les immunoglobulines, coneguda també com a recombinació V(D)J, consisteix en la generació d'una regió variable d'immunoglobulina exclusiva. La regió variable de cada immunoglobulina pesant està codificada per diverses parts, que es coneixen com segments. Aquests són coneguts com a segments variable (V), diversitat (D) i d'acoblament (J - joining en anglès).[46] Els segments V, D i J es troben a les cadenes pesants. A les lleugeres només s'hi troben els segments V i J. Hi ha múltiples còpies de tots aquests segments organitzats en tàndem al genoma dels mamífers. A la medul·la òssia, cada limfòcit B en desenvolupament acobla la regió variable de la seva immunoglobulina seleccionant i combinant a l'atzar un segment V amb un D i un altre J (o un V i un altre J, a les cadenes lleugeres). Com que existeixen múltiples còpies lleugerament diferents per cada seqüència genètica dels segments, es produeixen diferents combinacions que mitjançant aquest procés generen un elevat nombre de paràtops i també diferents especificitats de l'antigen.[3]
Després de la producció d'una immunoglobulina funcional per un limfòcit B durant la recombinació V(D)J, no es pot expressar cap regió variable diferent (un procés conegut com a exclusió al·lèlica). Així doncs, cada limfòcit B només pot produir anticossos que continguin un sol tipus de cadena variable.[4][48]
Hipermutació somàtica i maduració de l'afinitat[modifica]
Un altre mecanisme que genera diversitat en els anticossos té lloc als limfòcits B madurs. Després de l'activació per antígens, els limfòcits B comencen a proliferar ràpidament. En aquestes cèl·lules de ràpida divisió, els gens que codifiquen els dominis variables de les cadenes pesants i lleugeres pateixen una gran taxa de mutacions puntuals mitjançant un procés anomenat "hipermutació somàtica" (SHM). Aquesta produeix aproximadament el canvi d'un nucleòtid per gen variable i cèl·lula en cada divisió.[6] Per consegüent, qualsevol cèl·lula filla d'una línia de limfòcits B adquireix una lleugera diferència en la seqüència d'aminoàcids dels dominis variables de les seves cadenes d'anticossos.
La hipermutació somàtica serveix per incrementar la diversitat del reservori d'anticossos i influir en l'afinitat d'unió entre l'antigen i l'anticòs.[49] Algunes mutacions puntuals acaben per produir anticossos que tenen interaccions més dèbils (baixa afinitat) amb el seu antigen que l'anticòs original, mentre que d'altres generen anticossos amb una interacció més forta (alta afinitat).[50] Els limfòcits B que expressen anticossos d'elevada afinitat a la superfície reben un fort senyal perquè sobrevisquin durant les interaccions amb altres cèl·lules, mentre que els que expressen anticossos de baixa afinitat moriran per apoptosi.[50]
Així doncs, els limfòcits B que expressen anticossos amb una afinitat més elevada pel seu antigen competiran amb avantatge contra aquells de menor afinitat en la seva funció i supervivència. El procés de generació d'anticossos amb afinitat augmentada progressivament es diu "maduració de l'afinitat". La maduració de l'afinitat té lloc als limfòcits B madurs després de la recombinació V(D)J i és dependent del suport que rebrà dels limfòcits T col·laboradors.[51]

Canvi de classe[modifica]
El canvi de classe de la immunoglobulina és un procés biològic que té lloc després de l'activació dels limfòcits B, que permet la producció de diferents classes d'anticossos (IgA, IgE, o IgG).[3] Aquestes classes estan definides per les regions constants (C) de la cadena pesant de la immunoglobulina. Inicialment els limfòcits B verges expressen només IgM i IgD de superfície amb regions d'unió a l'anticòs idèntiques.
Cada isotip està adaptat per una funció diferent i per tant, després de l'activació, es necessita un anticòs amb un efector IgG, IgA o IgE per l'eliminació eficaç de l'antigen. El canvi de classe permet a la progènie d'un sol limfòcit B produir anticossos de diferents isotips. Només la regió constant de la cadena pesant de l'anticòs canvia durant el canvi de classe. Les regions variables, i per tant l'especificitat de l'antigen, romanen invariables. D'aquesta manera es produeixen efectors amb la funció adequada per cada amenaça de l'antigen. El canvi de classe és iniciat per les citocines. L'isotip generat depèn de les citocines presents a l'entorn del limfòcit B.[52]
El procés té lloc en un gen de la cadena pesant mitjançant un mecanisme conegut com a recombinació de canvi de classe (class switch recombination o CSR). Aquest mecanisme es basa en seqüències de nucleòtids conservats, anomenades regions de commutació (switch regions o S), que es troben en un punt de la seqüència de l'ADN anterior als gens de la regió constant (excepte a la cadena δ). El bri d'ADN s'escindeix per l'activitat de determinats enzims a dues regions S concretes.[53][54] L'exó del domini variable es torna a empalmar mitjançant un procés anomenat unió d'extrems no homòlegs (non-homologous end joining o NHEJ) a la regió constant elegida (γ, α o ε). Aquests procés conclou formant un gen d'immunoglobulina que codifica un anticòs d'un isotip diferent.[55]
Conversió gènica[modifica]
La conversió gènica és un intercanvi no recíproc en què la seqüència donant no és modificada, mentre que el gen acceptor adquireix un segment del donant per la recombinació homòloga. Tot i que aquest mecanisme de generació de diversitat en els anticossos ja era conegut, fins fa poc no se li havia donat prou rellevància. Se sap que és molt important en els ocells, que utilitzen a les cadenes lleugeres i pesants un gran nombre de pseudogens similars a les seqüències D, situades al principi de la seqüència del gen de les cadenes d'immunoglobulina. Posteriorment, aquests segments canvien somàticament l'única regió V, podent també estar sotmesos a hipermutació.[56] Aquest mecanisme també està present en alguns mamífers, com els conills.[57]
Fases finals de la síntesi d'immunoglobulines[modifica]
Una vegada reagrupats tots els segments, es produeix un sol ARNm, que es poliadenila. Aquest ARN abandona el nucli, dirigint-se als ribosomes del reticle endoplasmàtic rugós, on comença la seva traducció. Aleshores es produeix la glicosilació dels segments a la part luminal del RER i l'assemblatge; aquest procés és el següent: H+H → H2+L → H2L2. N'és una excepció la IgM, unint-se primer una cadena pesant amb una lleugera. El seu destí final, o bé com receptor o bé per ser secretada, depèn de si té o no un fragment afegit de dinou aminoàcids a la zona terminal N. Aquest pèptid s'incorpora a la síntesi mitjançant un procés de splicing. La seva presència determina una regió hidròfoba capaç d'ancorar-se a la membrana cel·lular.
Evolució de les immunoglobulines[modifica]
El desenvolupament d'organismes complexos, amb teixits i diversos llinatges cel·lulars, va requerir el desenvolupament de noves molècules per assegurar, d'una banda, que les cèl·lules s'adhereixin a altres de la mateixa colònia i, de l'altra, la defensa davant de possibles invasors patògens. Tres tipus de molècules, les lectines, les LLR i les immunoglobulines, han estat utilitzades al llarg de l'evolució en el desenvolupament de sistemes immunitaris. A vegades els seus patrons operatius es mesclen per combinar-ne les propietats, tot i que existeixen poques molècules que continguin els tres, com és el cas del gen de la malaltia poliquística renal (PKD1).[58]
Molts estudis aporten proves important que la superfamília de les immunoglobulines té representants en els bacteris i els arqueobacteris, o que almenys les immunoglobulines presents en aquests grups i les dels eucariotes podrien tenir un avantpassat comú a partir del qual evolucionaren de forma divergent. Així, s'han atribuït a aquest grup de proteïnes "similars a la immunoglobulina" bacteriana (BIG) el receptor de la Fc d'Ig de Streptococcus agalactiae, i l'endoglucanasa C de Cellumonas fimi.[59] També n'existeixen altres exemples com la invasina de Yersinia pseudotuberculosis o les Lig (Leptospiral Ig-like) de diverses espècies de Leptospira.[60][61] Després del seu descobriment en estreptococs es va descobrir una proteïna d'aquest tipus en el fag T4. En aquesta ocasió es va destacar que el seu paper estava relacionat amb l'adhesivitat cel·lular.[62]
Les proteïnes amb dominis Ig són comunes en eucariotes unicel·lulars, i fins a un cert punt la seva estructura és una característica conservada.[63] Un exemple d'això serien les alfa aglutinines de Saccharomyces cerevisiae. Es tracta de molècules que medien l'adhesió cel·lular i que tenen grans homologies amb els grups CD2-CD4 en els humans; el seu paper és en part similar, intervenint en aquest últim cas l'adhesió dels limfòcits T amb les cèl·lules presentadores d'antigen i les cèl·lules diana.[64]
Éssers pluricel·lulars[modifica]
És en els grups d'éssers pluricel·lulars més primitius, els parazous, que els científics intenten trobar indicis sobre l'origen del sistema immunitari adaptatiu.[66]
En aquest sentit, s'han dut a terme diversos treballs d'investigació sobre aquest grup, i en especial sobre les esponges considerades com fòssils vivents Geodia cydonium i Suberites domuncula. A G. cydonium s'hi troben molts dels tipus de proteïnes que també estan implicats en la immunitat dels mamífers. En especial, hi ha dos tipus de la superfamília de les immunoglobulines diferents: les unides a receptors tirosina-cinasa, i les molècules no enzimàtiques d'adhesió de les esponges. Els dominis corresponents ja mostren polimorfisme i, tot i complir funcions típiques de receptors i de molècules d'adherència cel·lular alhora, se sobreregulen en experiments de trasplantament.[67]
En definitiva, la superfamília de les immunoglobulines va intervenir en l'aparició de la pluricel·lularitat en mantenir la integritat estructural dels organismes distingint el propi de l'aliè. Això és a causa del fet que gràcies a les seves capacitats de generar mòduls, d'unir-se específicament a altres proteïnes i de formar bastons, així com d'oligomeritzar-se i de generar diversitat per splicing alternatiu a partir d'un material genètic limitat, es converteixen en ideals per mitjançar l'adherència cel·lular i com receptors de superfície de membrana.[68][69]
En la recerca de precedents del sistema immunitari adaptatiu, en els protòstoms es troben diversos exemples de proteïnes de la superfamília de les Ig que compleixen un paper en la defensa immunitària, com l'hemolina dels cucs de seda o la proteïna DSCAM de Drosophila melanogaster, així com proteïnes relacionades amb el fibrinogen amb dominis Ig (FREPs) dels gastròpodes. Algunes d'aquestes proteïnes, que representen una barrera de tipus innat, poden tenir isoformes solubles i ancorades a la membrana i generen diversitat per splicing alternatiu en zones de la molècula diferents a les cadenes variables dels vertebrats.[70]
Deuteròstoms[modifica]
Molts dels elements del sistema immunitari adaptatiu, incloent-hi les cèl·lules especialitzades, ja estan preconfigurades en els deuteròstoms més basals. S'han realitzat treballs sobre l'eriçó de mar (Strongylocentrotus purpuratus), trobant-hi un sistema immunitari ric amb homòlegs d'importants reguladors immunitaris i hematopoètics dels vertebrats, alguns d'ells crítics. Per això es teoritza que la pressió evolutiva clau pel desenvolupament del complex sistema immunològic en deuteròstoms no fou tant l'amenaça dels patògens com l'existència d'una rica varietat d'organismes simbiòtics, circumstància que és evident en els mateixos éssers humans amb la flora intestinal.[71] Com a il·lustració d'aquest punt, s'ha observat que el 60% de les espècies d'equinoderms tenen una relació simbiòtica amb bacteris.[72] En els tunicats continua l'augment de la complexitat del sistema immunitari. En l'ascidi Botryllus schlosseri, durant experiments d'empelts no compatibles, es van detectar moltes proteïnes que revelaven un complex sistema immunitari innat i algunes proteïnes amb domini immunoglobulina.[73][74] Cosa encara més sorprenent, també s'hi pot trobar un homòleg convincent de RAG1, contigu a una estructura similar a la RAG2.[75] Tanmateix, és en els cefalocordats que es troben les primeres empremtes de les immunoglobulines dels mamífers. S'han realitzat múltiples estudis l'amfiox Branchiostoma floridae, trobant unes curioses proteïnes, anomenades VCBP (V region−containing chitin-binding protein) amb grans homologies amb les regions V (variables) de les immunoglobulines, certament implicades en la resposta immunitària, però mancades de la seva variabilitat. Estudis cristal·logràfics han demostrat que probablement es tracta d'una molècula semblant a l'avantpassat de les actuals regions variables dels vertebrats.[76][77][78]
En els àgnats actuals s'hi observen alguns dels trets que identifiquen un sistema immunitari adaptatiu modern, mentre que d'altres estan absents. D'una banda, hi ha cèl·lules que ja contenen gran part de la maquinària molecular dels limfòcits; això suggereix una evolució d'aquest tipus cel·lular en els vertebrats més basals, i possiblement en un protocordat. Hi ha diverses proteïnes Ig amb dominis semblants a V, que fins i tot contenen regions V i J, encara que estan codificats en un únic exó i no són reorganitzables. Tanmateix, no tenen un sistema immunitari com el dels vertebrats, basat en els clàssics anticossos solubles, receptors de membrana, reorganització i empalmament per RAG. En comptes d'això, aquesta funció és assumida per una sèrie de proteïnes riques en repeticions de leucina, que fins i tot poden patir una complexa recombinació, mitjançant la qual s'obté una variabilitat equiparable a la dels anticossos (10¹⁴). Això constitueix un exemple exemple d'evolució paral·lela.[79]
Gnatostomats[modifica]
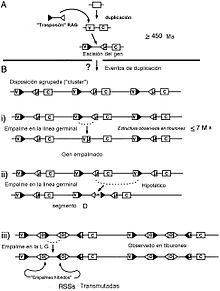
La majoria d'autors coincideixen que l'aparició del modern sistema immunitari es devia produir fa 500 milions d'anys, durant l'explosió cambriana. Probablement fou en un context en què hi havia moltes formes i combinacions de mòduls de proteïnes, moltes de les quals haurien desaparegut per les pressions selectives. En aquest sentit, una de les qüestions plantejades és que si les proves paleontològiques indiquen que els peixos mandibulats actuals procedeixen dels àgnats, i aquests últims manquen del sistema recombinació dels sistemes immunitaris actuals, segurament devia existir un avantpassat comú, un ostracoderm ancestral que presentés ambdós sistemes. Segons aquest punt de vista, el sistema de recombinació V(D)J probablement representa un desenvolupament evolutiu convergent en una branca dels ostracoderms que va precedir la línia dels gnatostoms.[80]
Pel que fa a les classes de les immunoglobulines, en peixos es troben anàlegs a la classe IgM, així com la IgD, identificada en moltes espècies de teleostis.[81] També n'hi ha moltes d'exclusives, com les que contenen les cadenes pesants ζ i τ. Possiblement són isotips evolutivament anteriors a la IgM.[82][83] En el cas dels condrictis també es troben isotips exclusius, a més d'IgM; es tracta de les IGW (IgX o IgNARC) i les IgNAR.[84]
El tipus IgG va sorgir en els amfibis i es troba en els rèptils. El tipus IgA és present en ocells i mamífers. Això significa que l'aparició de la IgA precedeix la divergència sinàpsids-diàpsids, de manera que els rèptils també l'haurien de tenir; tanmateix fins ara només s'ha descobert una molècula semblant a la IgA en un dragó.[85] Finalment, el tipus IgE sembla exclusiu dels mamífers.
Aplicacions mèdiques[modifica]
Diagnòstic de malalties[modifica]
En molts diagnòstics és habitual la detecció d'anticossos com prova per confirmar una malaltia. Per fer-ho es realitza una prova serològica.[86] Per exemple, en assajos bioquímics pel diagnòstic de malalties, s'estima l'valoració d'anticossos contra el virus d'Epstein-Barr o la malaltia de Lyme.[87] Si no es troben aquests anticossos significa que la persona no està infectada o que ho va estar fa molt de temps i els limfòcits B que generaven aquests anticossos s'han reduït de manera natural.
En immunologia clínica es valoren per nefelometria (o turbidimetria) el nivell de les diferents classes d'immunoglobulines per caracteritzar el perfil d'anticossos del pacient.[88] Per exemple, una observació elevada de la valoració de les diferents classes d'immunoglobulina pot ser útil a vegades per determinar la causa del dany hepàtic mitjançant un diagnòstic diferencial. En aquest sentit, una valoració elevada d'IgA indicaria cirrosi alcohòlica; si el que està elevat són les IgM se sospita d'hepatitis vírica i cirrosi biliar primària, mentre que la IgG està elevada en hepatitis vírica, autoimmunitària i cirrosi.
Les malalties autoimmunitàries es poden diagnosticar per anticossos que s'uneixen a epítops del mateix organisme; molts d'ells es poden detectar mitjançant una anàlisi de sang. Un exemple seria el cas dels anticossos dirigits contra els antígens de superfície dels eritròcits en l'anèmia hemolítica controlada pel sistema immunitari, que es detecten mitjançant la prova de Coombs.[89] Aquesta prova també s'utilitza per traçar anticossos en la preparació de transfusions de sang i en les dones en el període prenatal.[89]
En la pràctica existeixen molts mètodes immunodiagnòstics basats en la detecció de complexos antigen-anticòs que s'utilitzen en el diagnòstic de malalties infeccioses, com per exemple l'ELISA, la immunofluorescència, el Western blot, la immunodifusió i la immunoelectroforesi.
Tractaments terapèutics[modifica]
La teràpia d'anticossos monoclonals s'empra en el tractament de malalties com l'artritis reumatoide,[90] l'esclerosi múltiple,[91] la psoriasi,[92] i moltes formes de càncer, incloent-hi el limfoma no hodgkinià,[93] el càncer col·lorectal, el càncer de cap i coll i el càncer de mama.[94] Algunes immunodeficiències, com l'agammaglobulinèmia lligada al cromosoma X i la hipogammaglobulinèmia, consisteixen en una manca parcial o completa d'anticossos.[95] A vegades, aquestes malalties es tracten induint una immunitat a curt termini anomenada immunitat passiva, que s'adquireix a través de la infusió d'anticossos "prefabricats" en forma de sèrum humà o animal, immunoglobulina intravenosa o anticossos monoclonals en l'individu afectat (seroteràpia).[96]
Teràpia prenatal[modifica]
Les anomenades immunoglobulines Rho (D) o immunoglobulines anti-RhD són específiques de l'antigen humà Rhesus D, també conegut com a factor Rhesus.[97] D'aquests anticossos anti-RhD se'n venen dues marques comercials a Espanya: Rhophylac i Gammamglobulina anti-D Grifols. El factor Rhesus és un antigen que es troba als eritròcits. Els individus Rhesus-positius (Rh +) presenten aquest anticòs al glicocàlix dels eritròcits, mentre que els individus (Rh-) en manquen. Durant un naixement normal, la sang fetal pot passar a la mare per traumatismes en el part o complicacions de l'embaràs. En el cas d'incompatibilitat Rh entre la mare i el fill, la consegüent barreja de sangs pot sensibilitzar una mare Rh- contra l'antigen Rh del fill, cosa que fa que en embarassos posteriors corrin risc d'eritroblastosi fetal.[98] Els anti-RhD s'administren com a part del tractament prenatal per prevenir la sensibilització que podria tenir lloc. En tractar la mare amb anticossos anti-RhD abans i immediatament després del part, es destrueix l'antigen Rh del fetus al cos de la mare. Un punt important és que això succeeix abans que l'antigen pugui estimular els limfòcits B materns que més tard podrien "recordar" l'antigen Rh generant limfòcits B de memòria. Per tant, el seu sistema immunitari humoral no fabricarà anticossos anti-Rh i no atacarà els antígens Rhesus del seu nadó actual o futur.[97]
Variants d'anticossos en medicina i investigació[modifica]
A vegades cal produir anticossos específics. Per fer-ho s'injecta un antigen en un mamífer, com un ratolí, una rata o un conill si cal una quantitat reduïda; o una cabra, una ovella o un cavall si se'n requereixen grans quantitats. La sang aïllada d'aquests animals conté anticossos policlonals (múltiples anticossos que s'uneixen al mateix antigen) al sèrum sanguini, que es denomina antisèrum. També es poden injectar antígens al rovell de l'ou de gallina.[99] Tanmateix, per aplicacions analítiques cal una major especificitat, sobretot si es tracta de detectar molècules molt petites, així com quan s'utilitzen en aplicacions terapèutiques en què es vol bloquejar o detectar marcadors molt específics. Per això, la tecnologia dels anticossos ha generat algunes variants, entre les quals destaquen:
- Anticossos monoclonals
Si es desitja obtenir anticossos específics per un únic epítop d'un antigen, s'aïllen limfòcits secretors d'anticossos d'un animal i s'immortalitzen mitjançant fusions amb una línia cel·lular cancerosa. Les cèl·lules fusionades es denominen hibridomes i continuaran creixent i secretant anticossos al cultiu. S'aïllen les cèl·lules d'hibridoma individuals mitjançant una clonació per dilució per generar clons que produeixin tots el mateix anticòs. Aquests anticossos són denominats anticossos monoclonals.[100]
Els anticossos mono i policlonals generats es poden purificar utilitzant proteïna A/G o cromatografia d'afinitat a l'antigen.[101]
- Anticossos de cadena senzilla
És possible generar artificialment un anticòs que compti només amb les regions variables de la cadena lleugera i pesant, unides per un petit pèptid o un sol aminoàcid. En aquest cas s'obtindran anticossos de cadena senzilla o scFv. Actualment s'apliquen en tècniques com la citometria de flux o la immunohistoquímica.[102]
- Abzims
La majoria d'anticossos es diferencien d'altres proteïnes per no presentar catàlisi enzimàtica en la seva funció, pel que tradicionalment es consideren proteïnes de reconeixement de superfícies moleculars. Tanmateix, a la dècada del 1990 i principis del segle XXI diversos estudis d'immunologia van trobar anticossos amb propietats catalítiques. Aquests anticossos han rebut el nom d'abzims. És possible trobar-los en quantitats baixes al sèrum de persones sanes. Un exemple de l'existència dels abzims al cos humà fou la seva detecció a la llet materna.[103] Entre algunes d'aquestes activitats catalítiques detectades es troben les de peptidases inespecífiques i amilolítiques (degradació de midó). D'altra banda s'ha observat un increment en el nivell d'abzims en els pacients de malalties autoimmunitàries. Tanmateix, normalment es fabriquen de forma artificial, generant anticossos contra el compost intermediari d'una reacció per la qual es vol crear un enzim. En algunes ocasions podrien tenir aplicacions terapèutiques i industrials.[104][105]
- Nanoanticossos
Hi ha propostes per la utilització terapèutica d'anticossos monoclonals de camèlids, també anomenats nanoanticossos. Aquests són excepcionals en el regne animal per la seva mida reduïda, a causa del fet que estan compostos únicament de dues cadenes pesants.[106] Aquesta peculiaritat els permet accedir a localitzacions cel·lulars i d'antígens inaccessibles pels anticossos normals, a més de possibilitar-ne l'administració oral.[107]
- Faboteràpics
Per obtenir antídots contra verins de picades per animals com serps o artròpodes, es fabriquen antisèrums mitjançant sèrum cru o altament enriquit en immunoglobulines. Aquests procediments produeixen un gran nombre de reaccions al·lèrgiques, com anafilaxis o la malaltia del sèrum. Per evitar-ho, a les dècades del 1940 i 1950 es van fer estudis proteolítics per reduir al mínim la part de la molècula implicada en la neutralització del verí. Finalment es trobà que el fragment F (ab') 2, resultant de la digestió amb papaïna dels anticossos, i que manca de les zones efectores de la molècula, també pot neutralitzar verins. El professor Alejandro Alagón Cano va proposar per aquest enfocament terapèutic el nom de faboteràpia, observant-hi una incidència molt menor de reaccions adverses al sèrum, així com un major abast del compartiment extravascular.[108]
Aplicacions en les investigacions científiques[modifica]
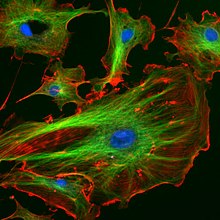
Els anticossos purificats tenen moltes aplicacions en la investigació. Són molt habituals per identificar i localitzar proteïnes intra i extracel·lulars. Els anticossos s'usen en la citometria de flux per diferenciar els tipus cel·lulars segons les proteïnes que expressen; dels diferents tipus cel·lulars s'expressen també diferents combinacions de molècules del cúmul de diferenciació (CD) a la superfície i produeixen diferents proteïnes intracel·lulars, extracel·lulars i excretables.[109] També s'utilitzen en immunoprecipitació per separar les proteïnes i qualsevol cosa que hi estigui lligada (coimmunoprecipitació) d'altres molècules en una lisi de cèl·lules,[110] en una anàlisi Western blot per identificar proteïnes separades per electroforesi,[111] i en immunohistoquímica o immunofluorescència per examinar l'expressió de proteïnes en seccions de teixits o localitzar proteïnes a l'interior de les cèl·lules amb un microscopi.[109][112] Les proteïnes també es poden detectar i quantificar amb anticossos, utilitzant tècniques ELISA i ELISPOT.[113][114]
Predicció de l'estructura[modifica]
La importància dels anticossos en la medicina i la biotecnologia exigeix un coneixement d'alta resolució de les seves estructures. Aquesta informació s'utilitza en l'enginyeria proteica, modificant l'afinitat d'unió amb l'antigen i identificant l'epítop d'un anticòs determinat. La cristal·lografia de rajos X és un mètode comú per determinar l'estructura dels anticossos. Tanmateix, la cristal·lització d'un anticòs sovint és laboriosa i requereix molt de temps. Els enfocaments computacionals poden oferir una alternativa més ràpida i barata a la cristal·lografia, però els seus resultats són més equívocs, ja que no ofereixen estructures empíriques. Servidors d'Internet com ara Web Antibody Modeling (WAM)[115] i Prediction of Immunoglobulin Structure (PIGS)[116] permeten el modelatge computacional de les regions variables dels anticossos. Rosetta Antibody és un nou servidor predictor de l'estructura de la regió FV dels anticossos, que incorpora tècniques sofisticades per minimitzar els bucles CDR i optimitzar l'orientació relativa de les cadenes lleugeres i pesants, així com models d'homologia que prediuen l'acoblament reeixit d'anticossos amb el seu antigen únic.[117]
Referències[modifica]
- ↑ Plummer, 1994, p. 186.
- ↑ «Anticòs». Gran Enciclopèdia Catalana. Barcelona: Grup Enciclopèdia Catalana.
- ↑ 3,0 3,1 3,2 3,3 Eleonora Market, F. Nina Papavasiliou (2003) V(D)J Recombination and the Evolution of the Adaptive Immune System Arxivat 2008-02-16 a Wayback Machine. PLoS Biology, 1(1): e16.
- ↑ 4,0 4,1 4,2 4,3 4,4 4,5 4,6 4,7 4,8 Janeway, C.A. [et al.].. Immunobiology.. 5a ed.. Garland Publishing, 2001. ISBN 0-8153-3642-X.
- ↑ Vegeu també Janeway, CA; Staff, VV.. Inmunobiología: el sistema inmunitario en condiciones de salud y enfermedad. Eva Sanz (trad.). Elsevier España, 2003. ISBN 978-84-458-1176-4.
- ↑ 6,0 6,1 Diaz M, Casali P «Somatic immunoglobulin hypermutation». Curr Opin Immunol, 14, 2, 2002, pàg. 235–40. DOI: 10.1016/S0952-7915(02)00327-8. PMID: 11869898.
- ↑ 7,0 7,1 7,2 7,3 7,4 7,5 Pier GB, Lyczak JB, Wetzler LM. Immunology, Infection, and Immunity. ASM Press, 2004. ISBN 1-55581-246-5.
- ↑ «nobelprize.org».
- ↑ AGN «The Late Baron Shibasaburo Kitasato». Canadian Medical Association Journal, 1931, pàg. 206.
- ↑ Winau F, Westphal O, Winau R «Paul Ehrlich--in search of the magic bullet». Microbes Infect., 6, 8, 2004, pàg. 786–9. DOI: 10.1016/j.micinf.2004.04.003. PMID: 15207826.
- ↑ Silverstein AM «Cellular versus humoral immunology: a century-long dispute». Nat. Immunol., 4, 5, 2003, pàg. 425–8. DOI: 10.1038/ni0503-425. PMID: 12719732.
- ↑ Van Epps HL «Michael Heidelberger and the demystification of antibodies». J. Exp. Med., 203, 1, 2006, pàg. 5. DOI: 10.1084/jem.2031fta. PMID: 16523537.
- ↑ Marrack, JR. Chemistry of antigens and antibodies. 2a edició. Londres: His Majesty's Stationery Office, 1938. OCLC 3220539.
- ↑ «profiles.nlm.nih.gov».
- ↑ Silverstein AM «Labeled antigens and antibodies: the evolution of magic markers and magic bullets». Nat. Immunol., 5, 12, 2004, pàg. 1211–7. Arxivat de l'original el 2007-06-16. DOI: 10.1038/ni1140. PMID: 15549122 [Consulta: 16 febrer 2009]. Arxivat 2007-06-16 a Wayback Machine.
- ↑ Edelman GM, Gally JA «The nature of Bence-Jones proteins. Chemical similarities to polypetide chains of myeloma globulins and normal gamma-globulins». J. Exp. Med., 116, 1962, pàg. 207–27. PMID: 13889153.
- ↑ Stevens FJ, Solomon A, Schiffer M «Bence Jones proteins: a powerful tool for the fundamental study of protein chemistry and pathophysiology». Biochemistry, 30, 28, 1991, pàg. 6803–5. PMID: 2069946.
- ↑ 18,0 18,1 Raju TN «The Nobel chronicles. 1972: Gerald M Edelman (b 1929) and Rodney R Porter (1917-85)». Lancet, 354, 9183, 1999, pàg. 1040. PMID: 10501404.
- ↑ Tomasi TB «The discovery of secretory IgA and the mucosal immune system». Immunol. Today, 13, 10, 1992, pàg. 416–8. PMID: 1343085.
- ↑ Preud'homme JL, Petit I, Barra A, Morel F, Lecron JC, Lelièvre E «Structural and functional properties of membrane and secreted IgD». Mol. Immunol., 37, 15, 2000, pàg. 871–87. PMID: 11282392.
- ↑ Johansson SG «The discovery of immunoglobulin E». Allergy and asthma proceedings: the official journal of regional and state allergy societies, 27, 2 Suppl 1, 2006, pàg. S3–6. PMID: 16722325.
- ↑ Raju, T N «The Nobel chronicles. 1984: Niels Kai Jerne, (1911-94); César Milstein (b 1926); and Georges Jean Franz Köhler (1946-95)». The Lancet, 355, 9197, Jan. 2000, pàg. 75. DOI: 10.1016/S0140-6736(05)72025-0. PMID: 10615922.
- ↑ Hozumi N, Tonegawa S «Evidence for somatic rearrangement of immunoglobulin genes coding for variable and constant regions». Proc. Natl. Acad. Sci. U.S.A., 73, 10, 1976, pàg. 3628–32. PMID: 824647.
- ↑ Borghesi L, Milcarek C «From B cell to plasma cell: regulation of V(D)J recombination and antibody secretion». Immunol Res, 36, 1-3, 2006, pàg. 27–32. DOI: 10.1385/IR:36:1:27. PMID: 17337763.
- ↑ Parker D «T cell-dependent B cell activation». Annu Rev Immunol, 11, 1993, pàg. 331–60. DOI: 10.1146/annurev.iy.11.040193.001555. PMID: 8476565.
- ↑ 26,0 26,1 26,2 26,3 Wintrobe, Maxwell Myer. Wintrobe's clinical hematology. John G. Greer, John Foerster, John N Lukens, George M Rodgers, Frixos Paraskevas. 11a ed.. Hagerstwon, MD: Lippincott Williams & Wilkins, 2004, p. 453-456. ISBN 0-7817-3650-1.
- ↑ Tolar P, Sohn HW, Pierce SK «Viewing the antigen-induced initiation of B-cell activation in living cells». Immunol. Rev., 221, Febrer 2008, pàg. 64–76. DOI: 10.1111/j.1600-065X.2008.00583.x. PMID: 18275475.[Enllaç no actiu]
- ↑ Underdown B, Schiff J «Immunoglobulin A: strategic defense initiative at the mucosal surface». Annual Review of Immunology, 4, 1986, pàg. 389–417. DOI: 10.1146/annurev.iy.04.040186.002133. PMID: 3518747.
- ↑ 29,0 29,1 Geisberger R, Lamers M, Achatz G «The riddle of the dual expression of IgM and IgD». Immunology, 118, 4, 2006, pàg. 429–37. PMID: 16895553.
- ↑ 30,0 30,1 30,2 Woof J, Burton D «Human antibody-Fc receptor interactions illuminated by crystal structures». Nat Rev Immunol, 4, 2, 2004, pàg. 89–99. DOI: 10.1038/nri1266. PMID: 15040582.
- ↑ Goding J «Allotypes of IgM and IgD receptors in the mouse: a probe for lymphocyte differentiation». Contemp Top Immunobiol, 8, pàg. 203–43. PMID: 357078.
- ↑ Grubb, R. i Laurell, A. B. Acta Path. Microb. Scand., 39, 390 (1956). PMID: 13381487
- ↑ Mattu T, Pleass R, Willis A, Kilian M, Wormald M, Lellouch A, Rudd P, Woof J, Dwek R «The glycosylation and structure of human serum IgA1, Fab, and Fc regions and the role of N-glycosylation on Fc alpha receptor interactions». J Biol Chem, 273, 4, 1998, pàg. 2260–72. DOI: 10.1074/jbc.273.4.2260. PMID: 9442070.
- ↑ Roux K «Immunoglobulin structure and function as revealed by electron microscopy». Int Arch Allergy Immunol, 120, 2, 1999, pàg. 85–99. DOI: 10.1159/000024226. PMID: 10545762.
- ↑ «emc.maricopa.edu». Arxivat de l'original el 2007-04-19. [Consulta: 25 febrer 2009].
- ↑ «cas.muohio.edu».
- ↑ Barclay A «Membrane proteins with immunoglobulin-like domains--a master superfamily of interaction molecules». Semin Immunol, 15, 4, 2003, pàg. 215-23. DOI: 10.1016/S1044-5323(03)00047-2. PMID: 14690046.
- ↑ Murre C, et al «The 3D structure of the immunoglobulin heavy-chain locus: implications for long-range genomic interactions». Cell, 133, 2, 2008. PMID: 18423198.
- ↑ Putnam FW, Liu YS, Low TL «Primary structure of a human IgA1 immunoglobulin. IV. Streptococcal IgA1 protease, digestion, Fab and Fc fragments, and the complete amino acid sequence of the alpha 1 heavy chain». J Biol Chem, 254, 8, 1979, pàg. 2865–74. PMID: 107164.
- ↑ Huber R «Spatial structure of immunoglobulin molecules». Klin Wochenschr, 58, 22, 1980, pàg. 1217–31. DOI: 10.1007/BF01478928. PMID: 6780722.
- ↑ Heyman B «Complement and Fc-receptors in regulation of the antibody response». Immunol Lett, 54, 2-3, 1996, pàg. 195–9. DOI: 10.1016/S0165-2478(96)02672-7. PMID: 9052877.
- ↑ 42,0 42,1 Ravetch J, Bolland S «IgG Fc receptors». Annu Rev Immunol, 19, 2001, pàg. 275–90. DOI: 10.1146/annurev.immunol.19.1.275. PMID: 11244038.
- ↑ Rus H, Cudrici C, Niculescu F «The role of the complement system in innate immunity». Immunol Res, 33, 2, 2005, pàg. 103–12. DOI: 10.1385/IR:33:2:103. PMID: 16234578.
- ↑ Mian I, Bradwell A, Olson A «Structure, function and properties of antibody binding sites». J Mol Biol, 217, 1, 1991, pàg. 133–51. DOI: 10.1016/0022-2836(91)90617-F. PMID: 1988675.
- ↑ Fanning LJ, Connor AM, Wu GE «Development of the immunoglobulin repertoire». Clin. Immunol. Immunopathol., 79, 1, 1996, pàg. 1–14. PMID: 8612345.
- ↑ 46,0 46,1 Nemazee D «Receptor editing in lymphocyte development and central tolerance». Nat Rev Immunol, 6, 10, 2006, pàg. 728–40. DOI: 10.1038/nri1939. PMID: 16998507.
- ↑ Peter Parham. The Immune System. Nova York: Garland Science, 2a ed., 2005. pàg. 47-62
- ↑ Bergman Y, Cedar H «A stepwise epigenetic process controls immunoglobulin allelic exclusion». Nat Rev Immunol, 4, 10, 2004, pàg. 753–61. DOI: 10.1038/nri1458. PMID: 15459667.
- ↑ Honjo T, Habu S «Origin of immune diversity: genetic variation and selection». Annu Rev Biochem, 54, 1985, pàg. 803–30. DOI: 10.1146/annurev.bi.54.070185.004103. PMID: 3927822.
- ↑ 50,0 50,1 Or-Guil M, Wittenbrink N, Weiser AA, Schuchhardt J «Recirculation of germinal center B cells: a multilevel selection strategy for antibody maturation». Immunol. Rev., 216, 2007, pàg. 130–41. DOI: 10.1111/j.1600-065X.2007.00507.x. PMID: 17367339.
- ↑ Neuberger M, Ehrenstein M, Rada C, Sale J, Batista F, Williams G, Milstein C «Memory in the B-cell compartment: antibody affinity maturation». Philos Trans R Soc Lond B Biol Sci, 355, 1395, 2000, pàg. 357–60. DOI: 10.1098/rstb.2000.0573. PMID: 10794054.
- ↑ Stavnezer J, Amemiya CT «Evolution of isotype switching». Semin. Immunol., 16, 4, 2004, pàg. 257–75. DOI: 10.1016/j.smim.2004.08.005. PMID: 15522624.
- ↑ Durandy A «Activation-induced cytidine deaminase: a dual role in class-switch recombination and somatic hypermutation». Eur. J. Immunol., 33, 8, 2003, pàg. 2069–73. DOI: 10.1002/eji.200324133. PMID: 12884279.
- ↑ Casali P, Zan H «Class switching and Myc translocation: how does DNA break?». Nat. Immunol., 5, 2004, p. 1101–3. DOI: 10.1038/ni1104-1101. 15496946.
- ↑ Lieber MR, Yu K, Raghavan SC «Roles of nonhomologous DNA end joining, V(D)J recombination, and class switch recombination in chromosomal translocations». DNA Repair (Amst.), 5, 9-10, 2006, pàg. 1234–45. DOI: 10.1016/j.dnarep.2006.05.013. 16793349.
- ↑ Weill, JC, et al «Somatic hyperconversion diversifies the single VH gene of the chicken with a high incidence in the D region». Cell, 59, 1989.
- ↑ Knight, KL: «Restricted VH gene usage and generation of antibody diversity in rabbit.». Annu. Rev. immunol., 10, 1992.
- ↑ Litman, G; Cannon, JP; Dishaw, LJ: «Reconstructing immune phylogeny: new perspectives». Nature, 5, novembre de 2005.
- ↑ Bateman, A; Eddy, SR; Chothia, C «Members of the immunoglobulin superfamily in bacteria». Protein Science, 5, 5, 1996. PMID: 8880921.
- ↑ Dersch P, Isberg RR. «An immunoglobulin superfamily-like domain unique to the Yersinia pseudotuberculosis invasin protein is required for stimulation of bacterial uptake via integrin receptors.». Infect Immun, 68, 5, 2000. PMID: 10768991.
- ↑ ,Matsunaga, J; Ko, AI i col·laboradors «Pathogenic Leptospira species express surface-exposed proteins belonging to the bacterial immunoglobulin superfamily». Mol Microbiol, 49, 4, 2005. PMCID PMC1237129.
- ↑ ateman A, Eddy SR, Mesyanzhinov VV «A member of the immunoglobulin superfamily in bacteriophage T4». Virus Genes, 14, 2, 1997. PMID: 9237357.
- ↑ Wojciechowicz D, Lu CF, Kurjan J, Lipke PN «Cell surface anchorage and ligand-binding domains of the Saccharomyces cerevisiae cell adhesion protein alpha-agglutinin, a member of the immunoglobulin superfamily». Mol Cell Biol, 13, 4, 1993. PMID: 8455628.
- ↑ Grigorescu A, Chen MH, Zhao H, Kahn PC, Lipke PN «A CD2-based model of yeast alpha-agglutinin elucidates solution properties and binding characteristics». IUBMB Life, 50, 2, 2000. PMID: 11185954.
- ↑ Nick Matzke. «Postulated intermediates in the molecular evolution of the Ig and TCR loci». Annotated Bibliography on the Evolutionary Origin of the Vertebrate Immune System, 28-04-2006. [Consulta: 22 agost 2008].
- ↑ Müller CI, Blumbach B, Krasko A, Schröder HC «Receptor protein-tyrosine phosphatases: origin of domains (catalytic domain, Ig-related domain, fibronectin type III module) based on the sequence of the sponge Geodia cydonium». Gene, 262, 1-2, 2001. PMID: 11179687.
- ↑ Kubrycht J, Borecký J, Soucek P, Jezek P «Sequence similarities of protein kinase substrates and inhibitors with immunoglobulins and model immunoglobulin homologue: cell adhesion molecule from the living fossil sponge Geodia cydonium. Mapping of coherent database similarities and implications for evolution of CDR1 and hypermutation». Folia Microbiol, 49, 2004. 3 PMID: 15259763.
- ↑ Brümmendorf, T; Lemmon, V «Immunoglobulin superfamily receptors: cis-interactions, intracellular adapters and alternative splicing regulate adhesion». Current opinion in cell biology, 13, 5, 2001. doi 10.1016/S0955-0674(00)00259-3.
- ↑ Strecker, G, et al «Molecular recognition between glyconectins as an adhesion self-assembly pathway to multicellularity». J Biol Chem., 279, 15, 2004. PMID: 14701844.
- ↑ «The Evolution of Adaptative Immune Systems». Cell, 124, 2006. DOI 10.1016/j.cell.2006.02.001.
- ↑ Litman, GW, et al «Genomic Insights into the Immune System of the Sea Urchin». Science, 314, 5801, 2006. DOI 10.1126/science.1134301.
- ↑ Noverr, MC; Huffnagle, GB. «Does the microbiota regulate immune responses outside the gut?». Trends Microbiol, 12. PMID.
- ↑ Oren M, Douek J, Fishelson Z, Rinkevich B «Identification of immune-relevant genes in histoincompatible rejecting colonies of the tunicate Botryllus schlosseri». Dev Comp Immunol, 31, 9, 2007. PMID: 17287019.
- ↑ Pancer Z, Diehl-Seifert B, Rinkevich B, Müller WE: «A novel tunicate (Botryllus schlosseri) putative C-type lectin features an immunoglobulin domain». DNA Cell Biol., 16, 6, 1997. PMID: 9212174.
- ↑ Kapitónov, VV; Jurka, J «RAG1 core and V(D)J recombination signal sequences were derived from Transib transposons». PLoS Biol., 3, 2005.
- ↑ Cannon JP, Haire RN, Litman GW «Identification of diversified genes that contain immunoglobulin-like variable regions in a protochordate». Nat Immunol, 3, 12, 2002. PMID: 12415263.
- ↑ Hernández Prada JA, Haire RN, Allaire M, Jakoncic J, Stojanoff V, Cannon JP, Litman GW, Ostrov DA «[16799561 Ancient evolutionary origin of diversified variable regions demonstrated by crystal structures of an immune-type receptor in amphioxus]». Nature immunology, 7, 8, 2006. PMID.
- ↑ Litman GW, Cannon JP, Dishaw LJ, Haire RN, Eason DD, Yoder JA, Prada JH, Ostrov DA «Immunoglobulin variable regions in molecules exhibiting characteristics of innate and adaptive immune receptors». Immunol Res., 38, 1-3, 2007. PMID: 17917037.
- ↑ Cooper, MD; Alder, MN «The Evolution of Adaptive Immune Systems». Cell, 124, 2006. DOI 10.1016/j.cell.2006.02.001.
- ↑ Janvier, P «Catching the first fish». Nature, 402, 1999. PMID.
- ↑ Stein Tore Solem i Jørgen Stenvik. Antibody repertoire development in teleosts--a review with emphasis on salmonids and Gadus morhua L. Developmental & Comparative Immunology, Volume 30, Issues 1-2, Antibody repertoire development, 2006, pàg.s 57-76.
- ↑ J.D. Hansen, E.D. Landis i R.B. Phillips. Discovery of a unique Ig heavy-chain isotype (IgT) in rainbow trout: Implications for a distinctive B cell developmental pathway in teleost fish. Proceedings of the National Academy of Sciences U S A. Volume 102, Issue 19, 2005, pages 6919-24.
- ↑ N. Danilova, J. Bussmann, K. Jekosch, L. A. Steiner. "The immunoglobulin heavy-chain locus in zebrafish: identification and expression of a previously unknown isotype, immunoglobulin Z." Nature Immunology, Volum 6, Issue 3, 2005, pàg. 295-302.
- ↑ H. Dooley i M.F. Flajnik. "Antibody repertoire development in cartilaginous fish". Developmental & Comparative Immunology, Volum 30, Issues 1-2, Antibody repertoire development, 2006, pàgines 43-56.
- ↑ Deza, F. G.; Espinel, C. S. & Beneitez, J. V. «A novel IgA-like immunoglobulin in the reptile Eublepharis macularius» (resum). Dev. Comp. Immunol., 31, 7, 2007. DOI: 10.1016/j.dci.2006.09.005.
- ↑ «Animated depictions of how antibodies are used in ELISA assays». Cellular Technology Ltd.—Europe. Arxivat de l'original el 2007-05-09. [Consulta: 8 maig 2007].
- ↑ «Animated depictions of how antibodies are used in ELISPOT assays». Cellular Technology Ltd.—Europe. Arxivat de l'original el 2010-11-18. [Consulta: 8 maig 2007].
- ↑ Stern P «Current possibilities of turbidimetry and nephelometry». Klin Biochem Metab, 14, 3, 2006, pàg. 146–151. Arxivat de l'original el 2007-09-26 [Consulta: 30 juny 2009]. Arxivat 2007-09-26 a Wayback Machine.
- ↑ 89,0 89,1 Dean, Laura «Blood Groups and Red Cell Antigens. Chapter 4: Hemolytic disease of the newborn». National Library of Medicine (US), [NCBI Bethesda (MD)], 2005.
- ↑ Feldmann M, Maini R «Anti-TNF alpha therapy of rheumatoid arthritis: what have we learned?». Annu Rev Immunol, 19, 2001, p. 163–96. DOI: 10.1146/annurev.immunol.19.1.163.
- ↑ Doggrell S «Is natalizumab a breakthrough in the treatment of multiple sclerosis?». Expert Opin Pharmacother, 4, 6, 2003, p. 999–1001. DOI: 10.1517/14656566.4.6.999.
- ↑ Krueger G, Langley R, Leonardi C, Yeilding N, Guzzo C, Wang Y, Dooley L, Lebwohl M «A human interleukin-12/23 monoclonal antibody for the treatment of psoriasis». N Engl J Med, 356, 6, 2007, p. 580–92. DOI: 10.1056/NEJMoa062382.
- ↑ Plosker G, Figgitt D «Rituximab: a review of its use in non-Hodgkin's lymphoma and chronic lymphocytic leukaemia». Drugs, 63, 8, 2003, p. 803–43. DOI: 10.2165/00003495-200363080-00005.
- ↑ Vogel C, Cobleigh M, Tripathy D, Gutheil J, Harris L, Fehrenbacher L, Slamon D, Murphy M, Novotny W, Burchmore M, Shak S, Stewart S «First-line Herceptin monotherapy in metastatic breast cancer». Oncology, 61 Suppl 2, 2001, p. 37–42. DOI: 10.1159/000055400.
- ↑ LeBien TW «Fates of human B-cell precursors». Blood, 96, 1, 2000, p. 9–23.
- ↑ Ghaffer A. «Immunization». Immunology - Chapter 14. University of South Carolina School of Medicine, 26-03-2006. [Consulta: 6 juny 2007].
- ↑ 97,0 97,1 Fung Kee Fung K, Eason E, Crane J, Armson A, De La Ronde S, Farine D, Keenan-Lindsay L, Leduc L, Reid G, Aerde J, Wilson R, Davies G, Désilets V, Summers A, Wyatt P, Young D «Prevention of Rh alloimmunization». J Obstet Gynaecol Can, 25, 9, 2003, p. 765–73.
- ↑ Urbaniak S, Greiss M «RhD haemolytic disease of the fetus and the newborn». Blood Rev, 14, 1, 2000, p. 44–61. DOI: 10.1054/blre.1999.0123.
- ↑ Tini M, Jewell UR, Camenisch G, Chilov D, Gassmann M «Generation and application of chicken egg-yolk antibodies». Comp. Biochem. Physiol., Part a Mol. Integr. Physiol., 131, 3, 2002, p. 569–74.
- ↑ Cole SP, Campling BG, Atlaw T, Kozbor D, Roder JC «Human monoclonal antibodies». Mol. Cell. Biochem., 62, 2, 1984, p. 109–20.
- ↑ Kabir S «Immunoglobulin purification by affinity chromatography using protein A mimetic ligands prepared by combinatorial chemical synthesis». Immunol Invest, 31, 3-4, 2002, p. 263–78. DOI: 10.1081/IMM-120016245.
- ↑ Lennard, S. Standard Protocols for the Construction of scFv Libraries. Springer protocols, 2001. DOI 10.1385/1-59259-240-6:059.
- ↑ Altria, KD. Capillary Electrophoresis Guidebook Principles, Operation, and Applications, página 226. Humana Press, 1996. ISBN 1-59259-538-3.
- ↑ Blackburn, GM et al.. Toward antibody-directed "abzyme" prodrug therapy, ADAPT: carbamate prodrug activation by a catalytic antibody and its in vitro application to human tumor cell killing. 93. PNAS, 1996. Arxivat 2019-10-16 a Wayback Machine.
- ↑ Shiro Kobayashi, Helmut Ritter, David Kaplan. Enzyme-Catalyzed Synthesis of Polymers, pàg. 206. Birkhäuser, 2006. ISBN 3-540-29212-8.
- ↑ Hamers-Casterman C, Atarhouch T, Muyldermans S, Robinson G, Hamers C, Songa EB, Bendahman N, Hamers R. "Naturally occurring antibodies devoid of light chains", Nature. 1993 Juny 3;363(6428):446-8
- ↑ «Nanobodies herald a new era in cancer therapy». Medical News, Maig 2004.
- ↑ Cano, AA. «Anticuerpos terapéuticos: El caso de los antivenenos». Sociedad Mexicana de Bioquímica. Arxivat de l'original el 2008-12-03. [Consulta: 25 agost].
- ↑ 109,0 109,1 Brehm-Stecher B, Johnson E «Single-cell microbiology: tools, technologies, and applications». Microbiol Mol Biol Rev, 68, 3, 2004, p. 538–59. DOI: 10.1128/MMBR.68.3.538-559.2004.
- ↑ Williams N «Immunoprecipitation procedures». Methods Cell Biol, 62, 2000, p. 449–53. DOI: 10.1016/S0091-679X(08)61549-6.
- ↑ Kurien B, Scofield R «Western blotting». Methods, 38, 4, 2006, p. 283–93. DOI: 10.1016/j.ymeth.2005.11.007.
- ↑ Scanziani E «Immunohistochemical staining of fixed tissues». Methods Mol Biol, 104, p. 133–40.
- ↑ Reen DJ. «Enzyme-linked immunosorbent assay (ELISA)». Methods Mol Biol., 32, 1994, p. 461–6.
- ↑ Kalyuzhny AE «Chemistry and biology of the ELISPOT assay». Methods Mol Biol., 302, 2005, p. 15–31.
- ↑ Whitelegg N.R.J., Rees A.R. «WAM: an improved algorithm for modeling antibodies on the WEB». Protein Engineering, 13, 12, 2000, pàg. 819–824. DOI: 10.1093/protein/13.12.819. PMID: 11239080.
WAM Arxivat 2011-07-17 a Wayback Machine. - ↑ Marcatili P, Rosi A,Tramontano A «PIGS: automatic prediction of antibody structures». Bioinformatics, 24, 17, 2008, pàg. 1953–1954. DOI: 10.1093/bioinformatics/btn341. PMID: 18641403.
Prediction of Immunoglobulin Structure (PIGS) Arxivat 2010-11-26 a Wayback Machine. - ↑ Sivasubramanian A, Sircar A, Chaudhury S, Gray J J «Toward high-resolution homology modeling of antibody Fv regions and application to antibody–antigen docking». Proteins, 74, 2009, pàg. 497–514. DOI: 10.1002/prot.22309.
RosettaAntibody
Bibliografia[modifica]
- Plummer, D. T. Introducció a la bioquímica pràctica. Edicions de la Universitat de Barcelona, 1994. ISBN 9788447504572.
Vegeu també[modifica]
Enllaços externs[modifica]
| A Wikimedia Commons hi ha contingut multimèdia relatiu a: Anticòs |
- Animacions sobre l'ús d'anticossos en les tècniques ELISPOT Arxivat 2007-02-22 a Wayback Machine. i ELISA Arxivat 2007-02-11 a Wayback Machine. (anglès)
