Iridi
| Iridi | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
77Ir
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Aspecte | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Blanc platejat  Línies espectrals de l'iridi | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propietats generals | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nom, símbol, nombre | Iridi, Ir, 77 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Categoria d'elements | Metalls de transició | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Grup, període, bloc | 9, 6, d | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Pes atòmic estàndard | 192,217 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Configuració electrònica | [Xe] 4f14 5d7 6s2 2, 8, 18, 32, 15, 2 
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propietats físiques | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fase | Sòlid | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Densitat (prop de la t. a.) |
22,56 g·cm−3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Densitat del líquid en el p. f. |
19 g·cm−3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Punt de fusió | 2.739 K, 2.466 °C | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Punt d'ebullició | 4.701 K, 4.428 °C | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Entalpia de fusió | 41,12 kJ·mol−1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Entalpia de vaporització | 563 kJ·mol−1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Capacitat calorífica molar | 25,10 J·mol−1·K−1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Pressió de vapor | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propietats atòmiques | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Estats d'oxidació | −3,−1, 0, 1, 2, 3, 4, 5, 6 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Electronegativitat | 2,20 (escala de Pauling) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Energies d'ionització | 1a: 880 kJ·mol−1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 2a: 1.600 kJ·mol−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Radi atòmic | 136 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Radi covalent | 141±6 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Miscel·lània | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Estructura cristal·lina | Cúbica centrada en la cara 
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ordenació magnètica | Paramagnètic[1] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Resistivitat elèctrica | (20 °C) 47,1 nΩ·m | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Conductivitat tèrmica | 147 W·m−1·K−1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dilatació tèrmica | 6,4 µm/(m·K) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Velocitat del so (barra prima) | (20 °C) 4.825 m·s−1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mòdul d'elasticitat | 528 GPa | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mòdul de cisallament | 210 GPa | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mòdul de compressibilitat | 320 GPa | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Coeficient de Poisson | 0,26 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Duresa de Mohs | 6,5 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Duresa de Vickers | 1.760 MPa | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Duresa de Brinell | 1.670 MPa | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nombre CAS | 7439-88-5 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Isòtops més estables | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Article principal: Isòtops de l'iridi | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
L'iridi és l'element químic de símbol Ir i nombre atòmic 77. Se situa en el grup 9 de la taula periòdica dels elements i en el 6è període. Es tracta d'un metall de transició, del grup del platí, dur, fràgil, pesant, de color blanc argentat. Exceptuant els gasos nobles, és l'element menys abundant a la Terra i es troba a la natura en aliatges amb platí i osmi. És l'element més resistent a la corrosió. S'empra en aliatges d'alta resistència que poden suportar altes temperatures, en contactes elèctrics, en aparells que treballen a altes temperatures, i com a agent enduridor del platí.
Història[modifica]
Durant els primers anys del segle xix una sèrie de químics treballaven en la separació dels metalls del grup del platí, entre ells s'hi trobava el químic anglès Smithson Tennant (1761-1815),[2] que seria qui acabaria separant l'iridi i també l'osmi.
Tennant, igual que d'altres químics, va experimentar dissolent platí en aigua règia, que és una barreja d'àcids nítric i clorhídric, i va observar un precipitat de color negre i lluentor metàl·lica. Aquest residu ja havia estat observat prèviament, però es considerava que el precipitat residual era grafit. L'estiu del 1803 Tennant va suggerir que probablement el precipitar era un nou metall. Durant la tardor del mateix any, el químic francès Hippolyte-Victor Collet-Descotils també va concloure que el precipitat, en el seu cas obtingut a partir de sals de platí, contenia un metall. El també químic francès Louis Nicolas Vauquelin va escalfar el residu amb un àlcali i va obtenir un òxid volàtil, i va pensar que era l'òxid del metall mencionat per Collet-Descotils.[3]
Tennant va continuar els seus experiments i durant la primavera del 1804 va comunicar a la Royal Society que el precipitat que quedava en dissoldre el platí en aigua règia contenia dos nous metalls, l'iridi i l'osmi, el residu negre era un aliatge natural d'aquests dos metalls[3] anomenat iridosmina o osmiridi, en funció de les proporcions dels dos metalls.[4] El 1805 va publicar l'article On Two Metals Found in the Black Powder Formed after Dissolution of Platinum on apareixien per primer cop els noms d'iridi i osmi.[3] El nom donat a l'iridi fa referència a la deessa grega Iris, simbolitzada per l'arc de Sant Martí, perquè les sals de l'iridi presenten una coloració diversa.[2]
Malgrat la seva aparent intractabilitat, un grup de químics, inclòs l'anglès Humphry Davy (1778-1829), van demostrar el 1813 que l'iridi es fonia igual que altres metalls. Per aconseguir-ho, l'exposaren a un potent corrent elèctric generat per un elevat nombre de bateries.[5]
Estat natural i obtenció[modifica]

L'iridi és un dels elements químics menys abundants a la Terra, ocupant la posició 84 dels 90 elements naturals, i essent el 6 següents els gasos nobles. La seva concentració mitjana a l'escorça terrestre és de només 3 ppt.[6] Malgrat la seva raresa se'l troba en uns vint-i-quatre minerals, tots ells rars, en concentracions superiors al 10 %. Els minerals que en contenen un 50 % o més són els següents, tots ells aliatges naturals dels elements natius o sulfurs: chengdeïta 91,17 %, cuproiridsita 66,71 %, kashinita 66,13 %, rutheniridosmina 63,20 %, tolovkita 55,55 % i iridi natiu 52,58 %.[7]
L'iridi als asteroides[modifica]

L'iridi és un mineral escassíssim a la Terra però tanmateix abunda en els asteroides. A la fi dels 70, el geòleg estatunidenc Walter Álvarez descobrí que la capa del límit Cretaci-Paleogen, el pas entre el Cretaci i el Terciari fa uns 66Ma, que estudiava a Gubbio, Itàlia, contenia 100 vegades més quantitat d'iridi del que és habitual. D'altres observacions coincidiren amb la mateixa anomalia.[8] Amb aquestes dades Álvarez avançà la hipòtesi que un meteorit podia haver xocat amb la Terra.[9] El 1991 es descobrí el cràter de Chicxulub de 180 km de diàmetre, al nord de la península de Yucatán i el mar Carib, sepultat per centenars de metres de sediments posteriors.[8] Segons Álvarez i d'altres autors podria ser una gran col·lisió d'un meteorit que provocà la gran extinció dels dinosaures i d'altres éssers vius.[10]
Mètode d'obtenció[modifica]
L'iridi generalment es produeix comercialment juntament amb els altres metalls platinoides com a subproducte de la producció de níquel o coure. Les mines d'on s'obté l'iridi es troben a Sud-àfrica i Alaska, EUA, així com a Birmània, Brasil, Rússia i Austràlia. A finals del segle xx, Sud-àfrica era el principal productor mundial d'iridi.[11] La producció mundial està al voltant de les tres tones/any.[6]
Una vegada retirats del mineral l'argent, l'or, el pal·ladi i el platí, el residu restant es fon amb disulfat de sodi per tal d'eliminar el rodi. El concentrat restant, que conté iridi, juntament amb ruteni i osmi, es fon amb peròxid de sodi per eliminar les sals de ruteni i d'osmi, formant-se també òxid de iridi(IV) de baixa puresa. Aquest és dissolt en aigua règia, i es pot eliminar el contingut d'oxigen produint una solució d'hexacloroiridat d'amoni . Un procés d'assecat per evaporació, seguit de la combustió amb gas hidrogen, aconsegueix finalment l'iridi pur.[12]
Característiques principals[modifica]
Propietats físiques[modifica]
L'iridi és un metall de transició del grup dels platinoides, té una densitat de 22,562 g/cm³, només lleugerament superat per l'osmi amb densitat 22,587 g/cm³; un punt de fusió de 2446 °C i un punt d'ebullició de 4428 °C. És de color blanc, semblant al platí, però presenta una lleugera coloració groga. És difícil treballar aquest metall, perquè és molt dur (6,5 en l'escala de Mohs) i trencadís.[13]
Propietats químiques[modifica]
Els estats d'oxidació de l'iridi més comuns són +1, +3 i +4. És en gran part immune als atacs atmosfèrics, a l'aigua i als àcids. En escalfar-se amb oxigen, l'iridi metall dona òxid d'iridi(IV) segons la reacció:[14]
Generalment, els elements del bloc d del 5è i 6è períodes mostren propietats químiques semblants, però en aquest cas no és així, el rodi (immediatament per sobre de l'iridi a la taula periòdica) es crema per donar òxid de rodi(III), . Si es forma òxid d'iridi(III) a la reacció anterior, acaba oxidant-se a .[14]
L'iridi metàl·lic reacciona directament amb el gas fluor per formar el fluorur d'iridi(VI) altament corrosiu, :
Aquest fluorur, amb cura, es pot escalfar per formar fluorur d'iridi(V), que té l'estructura tetramèrica de color groc . En absència d'humitat l'iridi reacciona amb els halògens per donar halogenurs d'iridi(3+):[14]
S'han descrit un nombre elevat de complexos de l'iridi, alguns d'ells emprats com a catalitzadors en síntesi orgànica.[15]
-
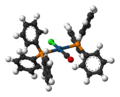
Complex de Vaska
-
Acetilacetonate d'iridi hidratat
-
Catalitzador de Brookhart
Isòtops[modifica]
L'iridi natural es presenta en forma de dos isòtops estables, iridi 191 i iridi 193, el primer representa el 37,3 % i el segon el 62,7 %. Tots dos s'utilitzen en la producció de radioisòtops. L'iridi 191 s'utilitza per a la producció d'iridi 192, radioactiu, que s'utilitza com a font de radiació en càmeres gamma que s'utilitzen per a proves no destructives. Les fonts d'iridi 192 també s'utilitzen en la braquiteràpia, tècnica de radioteràpia en la qual els materials radioactius es posen en contacte estret amb el teixit que es vol tractar. Tot i que l'iridi 192 es pot produir a partir d'iridi natural, amb els dos isòtops, l'ús d'iridi 191 enriquit dona una activitat específica molt més elevada i permet l'ús de fonts més petites. S'ha suggerit l'ús d'iridi 193 per a la producció del radioisòtop metaestable terapèutic platí 195m. Altres radioisòtops són l'iridi 188, l'iridi 189, l'iridi 190 i l'iridi 194.[14]
Aplicacions[modifica]

Indústria metal·lúrgica[modifica]
Les propietats de l'iridi, com la resistència a la corrosió i a la temperatura i la seva gran duresa, fan de la fabricació d'aliatges la principal aplicació d'aquest metall. L'iridi s'usa en la fabricació de gresols, com ara els recipients metàl·lics refractaris utilitzats en siderúrgia, en la fabricació de vidre i de pigments. També s'utilitza en la producció de tot tipus de peces que requereixin una elevada resistència a les temperatures altes.[16]
L'aliatge de platí i iridi que conté d'1 a 30 % d'iridi, s'empra per a joies i pins quirúrgics. És un aliatge molt més dur, resistent i menys reactiu que el platí pur. L'antiga norma internacional per als estàndards de longitud i de massa, el metre i el kilogram respectivament, es construïren a partir de l'aliatge que contenia el 90 per cent de platí i el 10 per cent d'iridi.[17]
Per ser tan dur, certs tremps de plomes estilogràfiques es recobreixen amb iridi per a donar-los més resistència al desgast.[16]

Medicina[modifica]
El radionúclid iridi 192, que té un temps de semidesintegració de 73,83 dies, s'usa com a font de radiació gamma per al tractament del càncer mitjançant braquiteràpia, una forma de radioteràpia on es col·loca una font de radiació segellada dins o al costat de la zona que necessita tractament. S'utilitza habitualment com a tractament eficaç per al càncer de coll uterí, de pròstata, de mama, d'esòfag i de pell i també es pot utilitzar per tractar tumors en molts altres llocs del cos.[16]
Indústria química[modifica]

L'iridi i els seus complexos tenen una àmplia activitat catalítica per catalitzar un bon nombre de transformacions orgàniques i inorgàniques. És el més prometedor metall com a biocatalitzador, catalitzador per a la fotosíntesi artificial i catalitzador per a l'oxidació d'aigua per a la producció d'hidrogen en un futur proper.[18] Actualment s'empra en el procés Cativa de producció d'àcid acètic per carbonilació del metanol.[19]
Indústria de l'automòbil[modifica]
S'utilitza en la fabricació de l'elèctrode de bugies de llarga durada, de l'ordre de 120.000 km.[16] Els metalls preciosos com el platí i l'iridi són més durs i tenen temperatures de fusió més elevades que els elèctrodes de l'aliatge de níquel que es troben a les bugies de coure tradicionals.
Referències[modifica]
- ↑ Magnetic susceptibility of the elements and inorganic compounds, a Lide, D. R. CRC Handbook of Chemistry and Physics (en anglès). 86a edició. CRC Press, 2005. ISBN 0-8493-0486-5.
- ↑ 2,0 2,1 Newton, 2010, p. 276.
- ↑ 3,0 3,1 3,2 Trifonov i Trifonov, 1982, p. 86.
- ↑ (Osmi) Gran Enciclopèdia Catalana. Volum 16. Reimpressió d'octubre de 1992. Barcelona: Gran Enciclopèdia Catalana, 1992, p. 478. ISBN 84-7739-014-2.
- ↑ «The great galvanic battery» (en anglès). Tonbridge Historical Society. [Consulta: 23 agost 2023].
- ↑ 6,0 6,1 Emsley, John.. Nature's building blocks: an A-Z guide to the elements. Oxford: Oxford University Press, 2001. ISBN 0-19-850341-5.
- ↑ «Mineral Species sorted by the element Ir Iridium». [Consulta: 5 març 2020].
- ↑ 8,0 8,1 Cáceres, P. «Los restos del meteorito que mató a los dinosaurios se pueden tocar en la costa vasca». El Mundo, 24-02-2011.
- ↑ ALVAREZ, W.; ASARO, F.; MICHEL, H. V.; ALVAREZ, L. W. «Iridium Anomaly Approximately Synchronous with Terminal Eocene Extinctions». Science, 216, 4548, 21-05-1982, pàg. 886–888. DOI: 10.1126/science.216.4548.886. ISSN: 0036-8075.
- ↑ Schulte, P.; Alegret, L.; Arenillas, I.; Arz, J. A.; Barton, P. J. «The Chicxulub Asteroid Impact and Mass Extinction at the Cretaceous-Paleogene Boundary» (en anglès). Science, 327, 5970, 05-03-2010, pàg. 1214–1218. DOI: 10.1126/science.1177265. ISSN: 0036-8075.
- ↑ «iridium | Definition, Properties, & Uses» (en anglès). Encyclopædia Britannica. Encyclopædia Britannica, inc.. [Consulta: 5 març 2020].
- ↑ Bell, Terence. «What Is Iridium? Metal Profile» (en anglès). [Consulta: 5 març 2020].
- ↑ William M. Haynes. CRC handbook of chemistry and physics: a ready-reference book of chemical and physical data.. 97. Boca Raton, Florida: CRC Press, 2016. ISBN 978-1-4987-5429-3.
- ↑ 14,0 14,1 14,2 14,3 «WebElements Periodic Table » Iridium » the essentials». [Consulta: 5 març 2020].
- ↑ Organometallic chemistry. Volume 22 : a review of the literature published during 1992. Londres: Royal Society of Chemistry, 1993. ISBN 978-1-84755-411-6.
- ↑ 16,0 16,1 16,2 16,3 Sanz Balagué, J.; Tomasa Guix, O. Elements i recursos minerals: aplicacions i reciclatge. 3a. Iniciativa Digital Politècnica, 2017. ISBN 978-84-9880-666-3.
- ↑ «Platinum–iridium | alloy» (en anglès). Encyclopædia Britannica. Encyclopædia Britannica, inc., 01-03-2018. [Consulta: 5 març 2020].
- ↑ Singh, Santosh Bahadur «IRIDIUM CHEMISTRY AND ITS CATALYTIC APPLICATIONS: A BRIEF». Green Chemistry & Technology Letters, 2, 4, 14-12-2016, pàg. 206. DOI: 10.18510/gctl.2016.247. ISSN: 2455-3611.
- ↑ Sunley, Glenn J; Watson, Derrick J «High productivity methanol carbonylation catalysis using iridium: The Cativa™ process for the manufacture of acetic acid». Catalysis Today, 58, 4, 26-05-2000, pàg. 293–307. DOI: 10.1016/S0920-5861(00)00263-7. ISSN: 0920-5861.
Bibliografia[modifica]
- Newton, David E. Chemical Elements (en anglès). Segona edició. Gale, 2010. ISBN 9781414476087.
- Trifonov, D. N.; Trifonov, V. D.. Chemical Elements - How They Were Discovered (en anglès). Moscou: MIR, 1982. ISBN 9785030007786.
| Taula periòdica | |||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| H | He | ||||||||||||||||||||||||||||||||||||||||
| Li | Be | B | C | N | O | F | Ne | ||||||||||||||||||||||||||||||||||
| Na | Mg | Al | Si | P | S | Cl | Ar | ||||||||||||||||||||||||||||||||||
| K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | ||||||||||||||||||||||||
| Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | ||||||||||||||||||||||||
| Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | ||||||||||
| Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | ||||||||||
| |||||||||||||||||||||||||||||||||||||||||
|
| |||||||||||||||||||||||||||||||||||||||||





![{\displaystyle {\ce {(NH4)2[IrCl6]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/a0bc786f93fb138bb9b3cc5822ed7756f617512e)
![{\displaystyle {\ce {Ir(s) + O2(g) -> IrO2(s) [negre]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/2717e816da59420b987adb6947e9727589ddf5d6)



![{\displaystyle {\ce {Ir(s) + 3F2(g) -> IrF6(s) [groc]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/ed1e20e374dd177ccde350dd5daa21bc546a7f80)
![{\displaystyle {\ce {[IrF5]4}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/8c145b0456f6ddc96add041e46957998de4f38b1)
![{\displaystyle {\ce {2 Ir (s) + 3 F2 (g) -> 2 IrF3 (s) [negre]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/780f7fd2ac58b07a520b524eb36f263ce477cdbe)
![{\displaystyle {\ce {2 Ir (s) + 3 Cl2 (g) -> 2 IrdCl3 (s) [vermell]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/0bd4c9ee944e03877bfbc17cc43feaf61ac1112a)
![{\displaystyle {\ce {2 Ir (s) + 3 Br2 (g) -> 2 IrBr3 (s) [bordeus]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/2061ff81916521b63fa2f2ff1d132b70d73ccecb)
![{\displaystyle {\ce {2 Ir (s) + 3 I2 (g) -> 2 IrI3 (s) [marro]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/5fc01635628af5ea12de352bd1f715fca58270ef)